下图为元素周期表的一部分。根据元素①~⑦在周期表中的位置,按要求回答下列问题。
(1)元素①~⑦的单质中氧化性最强的是___________ 。(填化学式)
(2)元素③⑤⑥的原子的半径从大到小的顺序是___________ 。(用元素符号表示)
(3)元素②的简单气态氢化物的沸点高于元素⑥的,原因是___________ 。
(4)元素②④⑦按原子数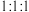 组成化合物甲,甲中所含化学键的类型是
组成化合物甲,甲中所含化学键的类型是___________ 。
(5)元素①与④组成的化合物可与水反应,写出反应的化学方程式___________ 。
(6)元款④⑥⑦的最高价氧化物对应的水化物分别为A、B、C.相同条件下。相同物质的量浓度的A、B、C的水溶液中 最大的是
最大的是___________ 。(填化学式)
(7)元素①与⑦组成的化合物为乙。用电子式表示乙的形成过程___________ 。
| 族 周期 | ⅠA | 0 | ||||||
| ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| ② | ③ | |||||||
| ④ | ⑤ | ⑥ | ⑦ |
(2)元素③⑤⑥的原子的半径从大到小的顺序是
(3)元素②的简单气态氢化物的沸点高于元素⑥的,原因是
(4)元素②④⑦按原子数
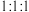 组成化合物甲,甲中所含化学键的类型是
组成化合物甲,甲中所含化学键的类型是(5)元素①与④组成的化合物可与水反应,写出反应的化学方程式
(6)元款④⑥⑦的最高价氧化物对应的水化物分别为A、B、C.相同条件下。相同物质的量浓度的A、B、C的水溶液中
 最大的是
最大的是(7)元素①与⑦组成的化合物为乙。用电子式表示乙的形成过程
更新时间:2021-07-08 22:19:33
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E、F为原子序数依次增大的六种元素,其中除F外均为短周期主族元素。常温下A、B、C的常见单质均为无色、无味的气体,D、E、F的单质均为固体,且F单质是目前世界上使用量最大的金属。A是所有元素中原子半径最小的元素,C与E同主族,且E的原子序数为C的2倍,D的最外层电子数比最内层多1个。请用化学用语回答下列问题:
(1)C的离子结构示意图为_________ ;D与E两元素的原子半径:D____ E(填“>”、“<”或“=”)。
(2)由A与碳元素组成的原子个数比3:1的最简化合物的结构简式为______________
(3)A与C形成的10电子阴离子与A与E形成的18电子阴离子反应的离子方程式为_________
(4)B的最高价氧化物的水化物与其氢化物反应生成的盐的水溶液的PH______ 7(填“>”、“<”或“=”)。化合物AB3是一种无色的液态物质,受撞击会分解成两种单质,请写出该反应的化学方程式_________
(5)已知一定条件下,D单质与氧化物Fe3O4反应时,放出大量的热且使F单质熔化。试写出该反应的化学方程式__________
(1)C的离子结构示意图为
(2)由A与碳元素组成的原子个数比3:1的最简化合物的结构简式为
(3)A与C形成的10电子阴离子与A与E形成的18电子阴离子反应的离子方程式为
(4)B的最高价氧化物的水化物与其氢化物反应生成的盐的水溶液的PH
(5)已知一定条件下,D单质与氧化物Fe3O4反应时,放出大量的热且使F单质熔化。试写出该反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、D、E、G、X、Y、Z是几种常见的短周期主族元素,其原子半径随原子序数变化如下图所示。
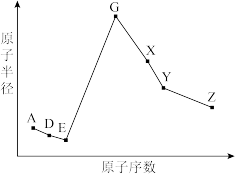
已知A的最高正价与最低负价的绝对值相等,E的单质是空气的主要成分之一;G原子和Ne原子的核外电子数相差1;X的简单离子半径在同周期中最小;Y的单质是一种常见的半导体材料;Z的原子半径在同周期中最小。
(1)A在元素周期表中的位置是___________ 。
(2)E的阴离子与G的阳离子比较,半径小的是___________ (填离子符号);G、X两者的最高价氧化物的水化物相互反应的离子方程式是___________ ;试用一个化学方程式说明A元素的非金属性强于Y元素:___________ 。
(3)Y与Z形成的化合物在一定条件下与足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是___________ 。

已知A的最高正价与最低负价的绝对值相等,E的单质是空气的主要成分之一;G原子和Ne原子的核外电子数相差1;X的简单离子半径在同周期中最小;Y的单质是一种常见的半导体材料;Z的原子半径在同周期中最小。
(1)A在元素周期表中的位置是
(2)E的阴离子与G的阳离子比较,半径小的是
(3)Y与Z形成的化合物在一定条件下与足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】下表列出了①~⑦共7种元素在元素周期表中的位置。
回答下列问题:
(1)①可以形成原子空间排列方式不同的多种单质,这些不同的单质之间互称为_______ 。
(2)①③形成的高价态化合物的电子式为_______ 。
(3)⑤的单质在工业上常用于冶炼熔点较高的金属,如用 冶炼V,该反应的化学方程式为
冶炼V,该反应的化学方程式为_______ 。
(4)③⑤⑦三种元素的简单离子半径由大到小的顺序是_______ (填离子符号)。
(5)②和⑦对应的简单氢化物能相互反应,其产物中含有的化学键有_______ 。
(6)根据元素周期律,②的非金属性比⑥强,但②的单质却比⑥的单质稳定,原因是_______ 。
(7)④⑤的最高价氧化物对应水化物反应的离子方程式为_______ 。
(8)③④可形成两种化合物,其中呈淡黄色的物质为A,另一种为B.A中,阴、阳离子个数比为_______ ;将26.4 g这两种物质的混合物投入足量水中,反应后,水溶液增重24.8 g,则A与B的物质的量之比为_______ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ |
(1)①可以形成原子空间排列方式不同的多种单质,这些不同的单质之间互称为
(2)①③形成的高价态化合物的电子式为
(3)⑤的单质在工业上常用于冶炼熔点较高的金属,如用
 冶炼V,该反应的化学方程式为
冶炼V,该反应的化学方程式为(4)③⑤⑦三种元素的简单离子半径由大到小的顺序是
(5)②和⑦对应的简单氢化物能相互反应,其产物中含有的化学键有
(6)根据元素周期律,②的非金属性比⑥强,但②的单质却比⑥的单质稳定,原因是
(7)④⑤的最高价氧化物对应水化物反应的离子方程式为
(8)③④可形成两种化合物,其中呈淡黄色的物质为A,另一种为B.A中,阴、阳离子个数比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、C、D、E、G、X、Y、Z是几种常见的短周期主族元素,其原子半径随原子序数变化如下图所示。已知C的最高正价与最低负价的绝对值相等;E的一种核素的质量数为18,中子数为10;G原子和Ne原子的核外电子数相差1;X的简单离子半径在同周期中最小;Y的单质是一种常见的半导体材料;Z的最外层有7个电子。回答下列问题:

(1)C在元素周期表中的位置_____ ,由A、E两种元素组成的18电子微粒的结构式为_________ 。
(2)E、G、Z三种元素的简单离子半径最小的是_____ (填离子符号)。
(3)元素的非金属性:C_____ Y(填“>”或“<”),其实验依据是_____ (用离子方程式表示 )
(4)X的原子结构示意图为_____ 。
(5)Y与Z形成的化合物在一定条件下与足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是_____ 。

(1)C在元素周期表中的位置
(2)E、G、Z三种元素的简单离子半径最小的是
(3)元素的非金属性:C
(4)X的原子结构示意图为
(5)Y与Z形成的化合物在一定条件下与足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).
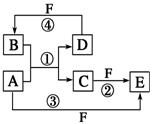
(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则A的离子结构示意图为____________ ,反应④的化学方程式为____________ ;
(2)若A是常见的变价金属的单质,D、F是气态单质,且反应①在水溶液中进行.反应②也在水溶液中进行,其离子方程式是________ ;用电子式表示化合物B的形成过程________________ 。
(3)若A、D、F都是短周期非金属元素单质,D的M层电子式L层电子的一半,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为____________ 。

(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则A的离子结构示意图为
(2)若A是常见的变价金属的单质,D、F是气态单质,且反应①在水溶液中进行.反应②也在水溶液中进行,其离子方程式是
(3)若A、D、F都是短周期非金属元素单质,D的M层电子式L层电子的一半,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D、E、F、G为6种短周期主族元素,其原子序数依次增大。A、C可形成A2C和A2C2两种化合物,B的最高正化合价与最低负化合价的绝对值之差为2,D和A同主族,E是地壳中含量最高的金属元素,F和C同主族且可形成FC2和FC3两种化合物。
(1)G的元素名称是__________ ,在元素周期表中的位置是__________ 。
(2)C、D、E、F简单离子的半径由大到小的顺序是__________ (填离子符号)。
(3)工业上冶炼E的单质反应的化学方程式是__________ 。
(4)由上述6种元素中的4种元素组成的化合物X,X既能与热的NaOH溶液反应,也能与稀盐酸反应,且均能生成无色气体,X的化学式是____________________ 。
(1)G的元素名称是
(2)C、D、E、F简单离子的半径由大到小的顺序是
(3)工业上冶炼E的单质反应的化学方程式是
(4)由上述6种元素中的4种元素组成的化合物X,X既能与热的NaOH溶液反应,也能与稀盐酸反应,且均能生成无色气体,X的化学式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E、F为短周期元素,且原子序数依次递增。A、E同主族,D、F同主族。A与其他非金属元素化合时易形成共价键,E与其他非金属元素化合时易形成离子键,且离子E+与D2-的核外电子排布相同。气态分子BD和C2具有相同的电子数,C2是空气中含量最高的物质。请回答下列问题:
(1)E位于第________ 周期______ 族;
(2)F的简单离子结构示意图为_______ ;
(3)C的电子式是_______ ;
(4)由A、D、E三种元素形成的化合物的化学式为_________ ,含有的化学键类型有_________ ,属于________ (填“共价”或“离子”)化合物;
(5)B的最高价氧化物的结构式为___________ 。
(1)E位于第
(2)F的简单离子结构示意图为
(3)C的电子式是
(4)由A、D、E三种元素形成的化合物的化学式为
(5)B的最高价氧化物的结构式为
您最近一年使用:0次
【推荐2】卤族元素的化合物在生活、医药、化工中有着重要的用途。
I.过氧化氢氧化法制备碘酸钾(KIO3)的方法如图:

(1)氧原子核外有_______ 种运动状态不同的电子;碘原子最外层电子的排布式为_______ ;K2CO3固体中含有的化学键有_______ 。
(2)合成步骤中的化学方程式为_______ 。
(3)当合成温度高于70℃,碘酸钾产率会降低,请写出可能的两种原因:_______ 。
Ⅱ.ClO2和Cl2都可以用于自来水消毒杀菌,可以通过下列方法制取:
2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
(4)该反应的氧化产物为_______ ,若反应过程中有4 mol HCl参与反应,则电子转移的数目为_______ 。
Ⅲ.目前从海水中提溴(Br2)大致有“浓缩”、“氧化”、“提取”等步骤。
(5)向浓缩的海水中通入Cl2,将海水中的Br-氧化为Br2。“氧化”时先在卤水中加入硫酸酸化,然后再通入氯气,硫酸酸化可以提高氯气的利用率,原因是_______ 。
(6)用热空气将Br2从上述溶液中吹出,并由浓Na2CO3溶液吸收,转变为NaBr、NaBrO3和CO2。吸收1 mol Br2需消耗Na2CO3_______ mol。
I.过氧化氢氧化法制备碘酸钾(KIO3)的方法如图:

(1)氧原子核外有
(2)合成步骤中的化学方程式为
(3)当合成温度高于70℃,碘酸钾产率会降低,请写出可能的两种原因:
Ⅱ.ClO2和Cl2都可以用于自来水消毒杀菌,可以通过下列方法制取:
2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
(4)该反应的氧化产物为
Ⅲ.目前从海水中提溴(Br2)大致有“浓缩”、“氧化”、“提取”等步骤。
(5)向浓缩的海水中通入Cl2,将海水中的Br-氧化为Br2。“氧化”时先在卤水中加入硫酸酸化,然后再通入氯气,硫酸酸化可以提高氯气的利用率,原因是
(6)用热空气将Br2从上述溶液中吹出,并由浓Na2CO3溶液吸收,转变为NaBr、NaBrO3和CO2。吸收1 mol Br2需消耗Na2CO3
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】(1)普鲁士蓝的化学式是KFe[Fe(CN)6],该物质的化学键有离子键、共价键和_____ 。
(2)KOCN是离子晶体;碳原子采取sp杂化,1mol该物质中含有的π键数目为____ 。
(3)H2O2常温下是液体,沸点较高(150℃),其主要原因是____ 。
(4)非金属元素 的第一电离能大于
的第一电离能大于 的第一电离能,原因是
的第一电离能,原因是______ 。
(5)V2O5溶于NaOH溶液,可得到钒酸钠(Na3VO4),该盐阴离子的立体构型为________ 。
(6)已知食盐的密度为ρ g·cm-3,其摩尔质量为M g·mol-1,阿伏加 德罗常数为NA,则在食盐晶体晶胞参数是_______ cm。
(7)1 mol SiO2晶体中含________ mol Si—O键。
(8)1 mol NH4BF4含有________ mol配位键。
(9)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为:_____________ 。
(10)体心立方结构的金属如:Na、K、Fe的晶胞的空间占有率表达式为________ (含π)。
(2)KOCN是离子晶体;碳原子采取sp杂化,1mol该物质中含有的π键数目为
(3)H2O2常温下是液体,沸点较高(150℃),其主要原因是
(4)非金属元素
 的第一电离能大于
的第一电离能大于 的第一电离能,原因是
的第一电离能,原因是(5)V2O5溶于NaOH溶液,可得到钒酸钠(Na3VO4),该盐阴离子的立体构型为
(6)已知食盐的密度为ρ g·cm-3,其摩尔质量为M g·mol-1,阿伏加 德罗常数为NA,则在食盐晶体晶胞参数是
(7)1 mol SiO2晶体中含
(8)1 mol NH4BF4含有
(9)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为:
(10)体心立方结构的金属如:Na、K、Fe的晶胞的空间占有率表达式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】短周期主族元素X、Y、Z、W原子序数依次增大,X的单质是空气中含量最高的气体,Y的焰色反应现象为黄色。Z为金属元素,由Z制得的容器常温下可盛装浓硫酸。W原子最外层比X原子最外层多2个电子。
(1)X在元素周期表中的位置为___________ ,X单质的结构式为___________ 。
(2)W的简单气态氢化物电子式是___________ ,该气态氢化物溶于水时,破坏的化学键是___________ 。
(3)Y、Z、W的原子半径从大到小的顺序是___________ (用元素符号表示)。Y的最高价氧化物的水化物和Z的最高价氧化物的水化物反应的离子方程式是___________ 。
(1)X在元素周期表中的位置为
(2)W的简单气态氢化物电子式是
(3)Y、Z、W的原子半径从大到小的顺序是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】亚硝酰氯( ,熔点:
,熔点: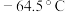 ,沸点:
,沸点: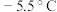 )是一种黄色气体,遇水易水解生成
)是一种黄色气体,遇水易水解生成 和
和 。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组的同学拟制备原料气 和
和 ,制备装置如图所示:
,制备装置如图所示:
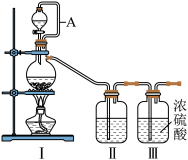
为制备纯净干燥的气体,补充表中缺少的药品
(2)乙组同学利用甲组制得的 和
和 制备
制备 ,装置如图所示:
,装置如图所示:
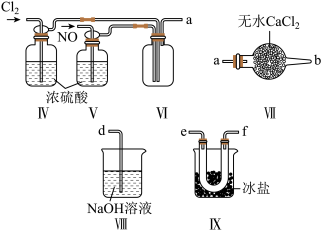
① 分子中各原子均满足8电子稳定结构,则
分子中各原子均满足8电子稳定结构,则 的电子式为
的电子式为_______ ;
②装置连接顺序为a→_______ (按气流自左向右方向,用小写字母表示);
③装置Ⅳ、Ⅴ除了可进一步干燥 、
、 外,另一作用是
外,另一作用是_______ ;
④装置Ⅷ中吸收尾气时, 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
 ,熔点:
,熔点: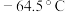 ,沸点:
,沸点: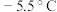 )是一种黄色气体,遇水易水解生成
)是一种黄色气体,遇水易水解生成 和
和 。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。(1)甲组的同学拟制备原料气
 和
和 ,制备装置如图所示:
,制备装置如图所示:
为制备纯净干燥的气体,补充表中缺少的药品
| 装置I | 装置Ⅱ | ||
| 烧瓶中 | 分液漏斗中 | ||
制备纯净的 |  | ①浓盐酸 | ② |
制备纯净的 |  | ③ | ④水 |
 和
和 制备
制备 ,装置如图所示:
,装置如图所示:
①
 分子中各原子均满足8电子稳定结构,则
分子中各原子均满足8电子稳定结构,则 的电子式为
的电子式为②装置连接顺序为a→
③装置Ⅳ、Ⅴ除了可进一步干燥
 、
、 外,另一作用是
外,另一作用是④装置Ⅷ中吸收尾气时,
 发生反应的化学方程式为
发生反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】镍是一种常用的有机合成催化剂。某工厂以含镍废料(主要成分为NiO,还含有少量 、
、 、
、 和
和 等)为原料制备镍的流程如图:
等)为原料制备镍的流程如图:

回答下列问题:
(1)滤渣1的主要成分是_______ (填化学式)。
(2)“氧化”过程中加入 或
或 ,发现氧化效率相等时,实际用量与理论用量的质量差(实际用量大于理论用量):
,发现氧化效率相等时,实际用量与理论用量的质量差(实际用量大于理论用量):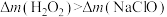 ,可能的原因是
,可能的原因是_______ 。
(3)滤渣2经过一系列操作可得到 ,将
,将 和
和 按物质的量比1:1共热反应可得到无水
按物质的量比1:1共热反应可得到无水 ,并放出两种酸性气体,其中一种能使品红溶液褪色,则总反应的化学方程式为
,并放出两种酸性气体,其中一种能使品红溶液褪色,则总反应的化学方程式为_______ 。
(4)“还原”过程中使用的试剂为 和
和 氧化产物为
氧化产物为 。
。 的电子式为
的电子式为_______ ;“还原”过程中发生反应的离子方程式为_______ 。
(5)若电解某粗镍(含Zn、Fe、Cu、Ag等杂质)提纯镍的装置如图所示。

已知氧化性: 。
。
下列说法错误的是_______ (填字母)。
A.X极为纯镍,Y极为粗镍
B.M可能是
C.X极净增质量等于Y极净减质量
D.X极的电极反应式为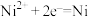
(6)测定镍样品的纯度:取wg镍样品完全溶于稀硫酸,加入 的EDTA溶液,使
的EDTA溶液,使 完全反应,煮沸,加入几滴PAN作指示剂,趁热用
完全反应,煮沸,加入几滴PAN作指示剂,趁热用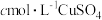 溶液滴定过量的EDTA,当滴定至溶液呈紫红色时,达到滴定终点,消耗
溶液滴定过量的EDTA,当滴定至溶液呈紫红色时,达到滴定终点,消耗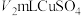 溶液(假设杂质不参与反应),则该镍样品的纯度为
溶液(假设杂质不参与反应),则该镍样品的纯度为_______ %(已知: ,
, )。如果滴定管用蒸馏水洗涤后未用待装溶液润洗,则测定结果
)。如果滴定管用蒸馏水洗涤后未用待装溶液润洗,则测定结果_______ (填“偏高”“偏低”或“无影响”)。
 、
、 、
、 和
和 等)为原料制备镍的流程如图:
等)为原料制备镍的流程如图:
回答下列问题:
(1)滤渣1的主要成分是
(2)“氧化”过程中加入
 或
或 ,发现氧化效率相等时,实际用量与理论用量的质量差(实际用量大于理论用量):
,发现氧化效率相等时,实际用量与理论用量的质量差(实际用量大于理论用量):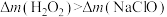 ,可能的原因是
,可能的原因是(3)滤渣2经过一系列操作可得到
 ,将
,将 和
和 按物质的量比1:1共热反应可得到无水
按物质的量比1:1共热反应可得到无水 ,并放出两种酸性气体,其中一种能使品红溶液褪色,则总反应的化学方程式为
,并放出两种酸性气体,其中一种能使品红溶液褪色,则总反应的化学方程式为(4)“还原”过程中使用的试剂为
 和
和 氧化产物为
氧化产物为 。
。 的电子式为
的电子式为(5)若电解某粗镍(含Zn、Fe、Cu、Ag等杂质)提纯镍的装置如图所示。

已知氧化性:
 。
。下列说法错误的是
A.X极为纯镍,Y极为粗镍
B.M可能是

C.X极净增质量等于Y极净减质量
D.X极的电极反应式为
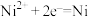
(6)测定镍样品的纯度:取wg镍样品完全溶于稀硫酸,加入
 的EDTA溶液,使
的EDTA溶液,使 完全反应,煮沸,加入几滴PAN作指示剂,趁热用
完全反应,煮沸,加入几滴PAN作指示剂,趁热用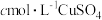 溶液滴定过量的EDTA,当滴定至溶液呈紫红色时,达到滴定终点,消耗
溶液滴定过量的EDTA,当滴定至溶液呈紫红色时,达到滴定终点,消耗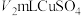 溶液(假设杂质不参与反应),则该镍样品的纯度为
溶液(假设杂质不参与反应),则该镍样品的纯度为 ,
, )。如果滴定管用蒸馏水洗涤后未用待装溶液润洗,则测定结果
)。如果滴定管用蒸馏水洗涤后未用待装溶液润洗,则测定结果
您最近一年使用:0次



