卤族元素的化合物在生活、医药、化工中有着重要的用途。
I.过氧化氢氧化法制备碘酸钾(KIO3)的方法如图:

(1)氧原子核外有_______ 种运动状态不同的电子;碘原子最外层电子的排布式为_______ ;K2CO3固体中含有的化学键有_______ 。
(2)合成步骤中的化学方程式为_______ 。
(3)当合成温度高于70℃,碘酸钾产率会降低,请写出可能的两种原因:_______ 。
Ⅱ.ClO2和Cl2都可以用于自来水消毒杀菌,可以通过下列方法制取:
2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
(4)该反应的氧化产物为_______ ,若反应过程中有4 mol HCl参与反应,则电子转移的数目为_______ 。
Ⅲ.目前从海水中提溴(Br2)大致有“浓缩”、“氧化”、“提取”等步骤。
(5)向浓缩的海水中通入Cl2,将海水中的Br-氧化为Br2。“氧化”时先在卤水中加入硫酸酸化,然后再通入氯气,硫酸酸化可以提高氯气的利用率,原因是_______ 。
(6)用热空气将Br2从上述溶液中吹出,并由浓Na2CO3溶液吸收,转变为NaBr、NaBrO3和CO2。吸收1 mol Br2需消耗Na2CO3_______ mol。
I.过氧化氢氧化法制备碘酸钾(KIO3)的方法如图:

(1)氧原子核外有
(2)合成步骤中的化学方程式为
(3)当合成温度高于70℃,碘酸钾产率会降低,请写出可能的两种原因:
Ⅱ.ClO2和Cl2都可以用于自来水消毒杀菌,可以通过下列方法制取:
2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
(4)该反应的氧化产物为
Ⅲ.目前从海水中提溴(Br2)大致有“浓缩”、“氧化”、“提取”等步骤。
(5)向浓缩的海水中通入Cl2,将海水中的Br-氧化为Br2。“氧化”时先在卤水中加入硫酸酸化,然后再通入氯气,硫酸酸化可以提高氯气的利用率,原因是
(6)用热空气将Br2从上述溶液中吹出,并由浓Na2CO3溶液吸收,转变为NaBr、NaBrO3和CO2。吸收1 mol Br2需消耗Na2CO3
2021·上海青浦·二模 查看更多[2]
更新时间:2021-04-11 11:18:24
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】铁、铝、铜、银是生活中常见的金属请按要求回答下列问题。
(1)某FeCl2、FeCl3的混合液,现欲检验Fe2+的存在,最佳检验试剂是_______ (填写试剂名称)。
(2)银镜反应后的试管内壁附着的一层银单质,用传统的洗涤方法容易产生氮氧化物污染,写出用FeCl3溶液洗涤银镜的化学方程式_______ 。
(3)向NaOH溶液中逐滴滴加AlCl3溶液,反应现象是_______ 。
(4)氧化铝坩埚不能用来灼烧碳酸钠固体,试用方程式解释其原理_______ 。
(5)足量的铜与一定量的浓硝酸反应,得到硝酸铜溶液和NO2、NO、N2O4的混合气体,将全部气体收集起来再和3.36L氧气(标准状况下)混合通入水中,气体刚好全部消失,若向所得的硝酸铜溶液中加入5mol/LNaOH溶液至铜离子恰好沉淀,则需加入的NaOH溶液体积为_______ L。
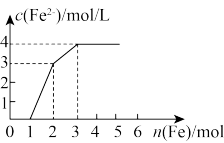
(6)某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,向其中逐渐加入铁粉,溶液中Fe2+的浓度与加入铁粉的物质的量之间的关系如图所示。则溶液中Fe(NO3)3、Cu(NO3)2、HNO3的物质的量浓度之比为_______ 。
(1)某FeCl2、FeCl3的混合液,现欲检验Fe2+的存在,最佳检验试剂是
(2)银镜反应后的试管内壁附着的一层银单质,用传统的洗涤方法容易产生氮氧化物污染,写出用FeCl3溶液洗涤银镜的化学方程式
(3)向NaOH溶液中逐滴滴加AlCl3溶液,反应现象是
(4)氧化铝坩埚不能用来灼烧碳酸钠固体,试用方程式解释其原理
(5)足量的铜与一定量的浓硝酸反应,得到硝酸铜溶液和NO2、NO、N2O4的混合气体,将全部气体收集起来再和3.36L氧气(标准状况下)混合通入水中,气体刚好全部消失,若向所得的硝酸铜溶液中加入5mol/LNaOH溶液至铜离子恰好沉淀,则需加入的NaOH溶液体积为
(6)某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,向其中逐渐加入铁粉,溶液中Fe2+的浓度与加入铁粉的物质的量之间的关系如图所示。则溶液中Fe(NO3)3、Cu(NO3)2、HNO3的物质的量浓度之比为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】燃煤烟气中含有大量NOx、CO2、CO和SO2,经处理可获得重要的化工原料。
(1)用CH4催化还原NOx可以消除氮氧化物的污染。
CH4(g)+4NO2(g)⇌4NO(g)+CO2(g)+2H2O(g) ΔH1=-574.0kJ∙mol-1
CH4(g)+4NO(g)⇌2N2(g)+CO2(g)+2H2O(g) ΔH2=+1160.0kJ∙mol-1
若反应中还原NOx至N2,消耗标准状况下4.48LCH4,则反应过程中转移的电子总数为______ 。
(2)利用烟气中分离所得的CO2、CO与H2按一定比例混合在催化剂的作用下合成甲醇,发生的主要反应如下:
反应1:CO(g)+2H2(g)⇌CH3OH(g) ΔH1=-99.0kJ∙mol-1
反应2:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH2=+83.0kJ∙mol-1
反应3:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH3=+384.0kJ∙mol-1
反应体系中CO平衡转化率(α)与温度和压强的关系如图所示。
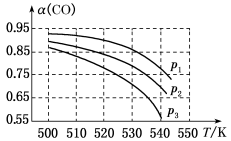
①α(CO)随温度升高而减小的原因是______ 。
②图中的p1、p2、p3由大到小的顺序为______ 。
(3)一定温度下,利用烟气中分离所得的CO2和H2在催化剂作用下合成甲醇,发生的反应为:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),如图关闭K,向A容器中充入1molCO2和4mol H2,向B容器中充入1.2molCO2和4.8molH2,两容器分别发生上述反应。已知起始时容器A和B的体积均为aL,反应达到平衡时容器B的体积为0.9aL,维持其他条件不变,若打开K一段时间后重新达到平衡,容器B的体积为______ L(不考虑温度的变化,P为可自由滑动活塞,不考虑活塞的摩擦力)。

(4)亚氯酸钠(NaClO2)和次氯酸钠(NaClO)混合液呈碱性,作为复合吸收剂可脱除烟气中的NOx、SO2,使其转化为 、
、 。
。
①写出NO与NaClO2反应的离子方程式:______ 。
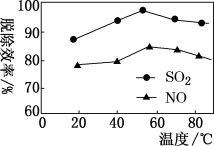
②如图表示在一定条件下温度与复合吸收剂对烟气中SO2、NO脱除效率的关系。图中SO2比NO脱除效率高的原因可能是______ 。
(1)用CH4催化还原NOx可以消除氮氧化物的污染。
CH4(g)+4NO2(g)⇌4NO(g)+CO2(g)+2H2O(g) ΔH1=-574.0kJ∙mol-1
CH4(g)+4NO(g)⇌2N2(g)+CO2(g)+2H2O(g) ΔH2=+1160.0kJ∙mol-1
若反应中还原NOx至N2,消耗标准状况下4.48LCH4,则反应过程中转移的电子总数为
(2)利用烟气中分离所得的CO2、CO与H2按一定比例混合在催化剂的作用下合成甲醇,发生的主要反应如下:
反应1:CO(g)+2H2(g)⇌CH3OH(g) ΔH1=-99.0kJ∙mol-1
反应2:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH2=+83.0kJ∙mol-1
反应3:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH3=+384.0kJ∙mol-1
反应体系中CO平衡转化率(α)与温度和压强的关系如图所示。

①α(CO)随温度升高而减小的原因是
②图中的p1、p2、p3由大到小的顺序为
(3)一定温度下,利用烟气中分离所得的CO2和H2在催化剂作用下合成甲醇,发生的反应为:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),如图关闭K,向A容器中充入1molCO2和4mol H2,向B容器中充入1.2molCO2和4.8molH2,两容器分别发生上述反应。已知起始时容器A和B的体积均为aL,反应达到平衡时容器B的体积为0.9aL,维持其他条件不变,若打开K一段时间后重新达到平衡,容器B的体积为

(4)亚氯酸钠(NaClO2)和次氯酸钠(NaClO)混合液呈碱性,作为复合吸收剂可脱除烟气中的NOx、SO2,使其转化为
 、
、 。
。①写出NO与NaClO2反应的离子方程式:
②如图表示在一定条件下温度与复合吸收剂对烟气中SO2、NO脱除效率的关系。图中SO2比NO脱除效率高的原因可能是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】氨气广泛应用于化工、轻工、化肥、制药、合成纤维等领域。如用于制造氨水、氮肥、复合肥料、硝酸、铵盐、纯碱等,含氮无机盐及有机物中间体、磺胺药、聚氨酯、聚酰胺纤维和丁腈橡胶等都需直接以氨为原料,此外液氨常用作制冷剂,氨还可以作为生物燃料来提供能源。某化学兴趣小组欲利用如图所示装置制备并探究氨气的性质,请回答下列问题:
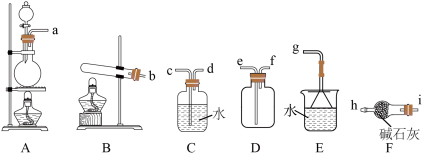
Ⅰ.制备氨气并探究氨水的酸碱性
(1)该小组选用氯化铵固体与氢氧化钙固体共热的方法制备氨气,其反应的化学方程式为_______ ,制取气体的发生装置应选用装置_______ (填“A”或“B”),若要制取并收集一瓶干燥的氨气,再进行尾气处理,则接口的连接顺序为_______ (按气流方向填写,部分装置可重复使用)。
(2)装置E的作用是_______ ,反应结束后向装置E中滴入数滴酚酞试剂,则装置E中的现象为_______ ,氨水呈_______ (填“酸”或“碱”)性。
Ⅱ.探究氨气的还原性
小组成员查阅文献发现若将生成的氨气与氧气混合通入装有催化剂的试管中,并对试管进行加热,可能生成、 、
、 ,还有可能生成
,还有可能生成 。
。
(3)经查阅资料知 在某催化剂作用下生成
在某催化剂作用下生成 的过程(部分物质未标出)如下,ad表示吸附状态,则在最后一步生成
的过程(部分物质未标出)如下,ad表示吸附状态,则在最后一步生成 的反应中氧化剂与还原剂的物质的量之比为
的反应中氧化剂与还原剂的物质的量之比为_______ 。

(4)该小组选用 作为催化剂,通过信息化的手段,利用产物分析仪检测到了中间产物
作为催化剂,通过信息化的手段,利用产物分析仪检测到了中间产物 ,
, 的来源可能是
的来源可能是_______ ,其后续的变化是_______ 。

Ⅰ.制备氨气并探究氨水的酸碱性
(1)该小组选用氯化铵固体与氢氧化钙固体共热的方法制备氨气,其反应的化学方程式为
(2)装置E的作用是
Ⅱ.探究氨气的还原性
小组成员查阅文献发现若将生成的氨气与氧气混合通入装有催化剂的试管中,并对试管进行加热,可能生成、
 、
、 ,还有可能生成
,还有可能生成 。
。(3)经查阅资料知
 在某催化剂作用下生成
在某催化剂作用下生成 的过程(部分物质未标出)如下,ad表示吸附状态,则在最后一步生成
的过程(部分物质未标出)如下,ad表示吸附状态,则在最后一步生成 的反应中氧化剂与还原剂的物质的量之比为
的反应中氧化剂与还原剂的物质的量之比为
(4)该小组选用
 作为催化剂,通过信息化的手段,利用产物分析仪检测到了中间产物
作为催化剂,通过信息化的手段,利用产物分析仪检测到了中间产物 ,
, 的来源可能是
的来源可能是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】丙烯是一种重要的化工原料。可由丙烷催化脱氢制备。
主反应:①C3H8(g)=C3H6(g)+H2(g) ΔH1
副反应:②C3H8(g)=C2H4(g)+CH4(g)
③C2H4(g)+H2(g)=C2H6(g)
④C3H8(g)+H2(g)=C2H6(g)+CH4(g)
回答下列问题:
(1)已知:C3H8(g)+ O2(g)=C3H6(g)+H2O(g) ΔH2=-117kJ/mol
O2(g)=C3H6(g)+H2O(g) ΔH2=-117kJ/mol
H2(g)+ O2(g)=H2O(g) ΔH3=-242kJ/mol。反应①的ΔH1=
O2(g)=H2O(g) ΔH3=-242kJ/mol。反应①的ΔH1=___ 。
(2)某温度下,在体积不变的密闭容器内发生反应①,起始总压强为105Pa,平衡时总压增加了20%。则C3H8的转化率为___ ;该反应的平衡常数Kp=___ Pa。若提高C3H8的平衡转化率,可采取的措施有___ (填标号)。
A.增大C3H8的浓度
B.提高温度
C.恒容下通入惰性气体
D.使用高效催化剂
(3)工业生产中常采用恒压下充入高温水蒸气的条件。如图表示常压下反应①C3H8的平衡转化率与温度及水烃比(M)的关系,M2___ 5(填“>”或“<”)。___ 。反应气中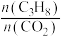 的配比对催化剂活性的影响如表所示。其中C3H6收率最高时
的配比对催化剂活性的影响如表所示。其中C3H6收率最高时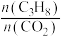 的配比是
的配比是___ 。
主反应:①C3H8(g)=C3H6(g)+H2(g) ΔH1
副反应:②C3H8(g)=C2H4(g)+CH4(g)
③C2H4(g)+H2(g)=C2H6(g)
④C3H8(g)+H2(g)=C2H6(g)+CH4(g)
回答下列问题:
(1)已知:C3H8(g)+
 O2(g)=C3H6(g)+H2O(g) ΔH2=-117kJ/mol
O2(g)=C3H6(g)+H2O(g) ΔH2=-117kJ/molH2(g)+
 O2(g)=H2O(g) ΔH3=-242kJ/mol。反应①的ΔH1=
O2(g)=H2O(g) ΔH3=-242kJ/mol。反应①的ΔH1=(2)某温度下,在体积不变的密闭容器内发生反应①,起始总压强为105Pa,平衡时总压增加了20%。则C3H8的转化率为
A.增大C3H8的浓度
B.提高温度
C.恒容下通入惰性气体
D.使用高效催化剂
(3)工业生产中常采用恒压下充入高温水蒸气的条件。如图表示常压下反应①C3H8的平衡转化率与温度及水烃比(M)的关系,M2
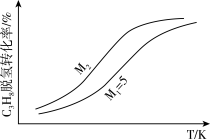
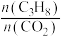 的配比对催化剂活性的影响如表所示。其中C3H6收率最高时
的配比对催化剂活性的影响如表所示。其中C3H6收率最高时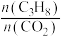 的配比是
的配比是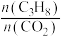 | C3H8转换率(%) | C3H6选择性(%) | C3H6收率(%) |
| 1:1.3 | 14.8 | 85.1 | 12.6 |
| 1:2.4 | 23.2 | 82.8 | |
| 1:3.6 | 22.8 | 83.5 | |
| 1:6.8 | 18.0 | 60.3 | 10.9 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】CO一直是化学家研究的热点载体,也是一种重要的化工产品。回答下列问题:
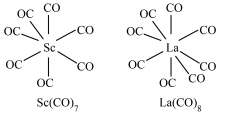
(1)我国科学家发现七配位金属羰基化合物 和八配位金属羰基化合物
和八配位金属羰基化合物 (TM=Y、La),为设计具有独特性质的化合物提供了新思路。它们的结构如图所示,CO作配体,配位原子为C,而不是O,其原因是
(TM=Y、La),为设计具有独特性质的化合物提供了新思路。它们的结构如图所示,CO作配体,配位原子为C,而不是O,其原因是___________ , 含
含___________  键。
键。
(2)工业上用CO合成 :
:
 。
。
①该反应在较低温度下能自发进行,推测该反应是___________ (填标号)
A.熵增、焓减反应 C.熵减、焓增反应
B.熵增、焓增反应 D.熵减、焓减反应
②一定温度下,向一恒容密闭容器中充入1molCO和 ,下列情况表明净反应速率(净反应速率等于正、逆反应速率之差)一定等于0的是
,下列情况表明净反应速率(净反应速率等于正、逆反应速率之差)一定等于0的是___________ (填标号)。
A.混合气体密度不随时间变化
B.混合气体中CO的体积分数不随时间变化
C.混合气体总压强不随时间变化
D. 的正反应速率等于
的正反应速率等于 的逆反应速率的3倍
的逆反应速率的3倍
(3)工业上常用天然气制备CO,原理如下:
①

②

则

___________ 。(用含 、
、 的代数式表示)
的代数式表示)
(4)光气 (COCl2)是一种有机中间体,常用于合成杀虫剂、黏合剂。CO合成光气的原理是
 。在甲、乙起始体积均为2L的密闭容器中均分别投入2molCO和
。在甲、乙起始体积均为2L的密闭容器中均分别投入2molCO和 ,在不同条件下发生上述反应,测得
,在不同条件下发生上述反应,测得 与时间关系如图所示。
与时间关系如图所示。
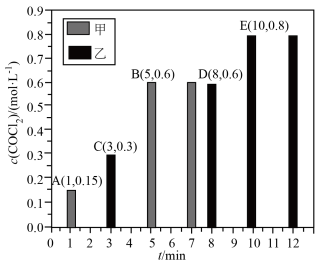
①相对甲,乙仅改变一个条件,可能是___________ (填标号)。
a.减小压强 b.加催化剂 c.降低温度
②若在恒容条件下反应,前10min内乙容器中CO的平均反应速率为___________  。甲容器中CO的平衡转化率为
。甲容器中CO的平衡转化率为___________ 。乙容器中平衡常数K为___________  。
。
(1)我国科学家发现七配位金属羰基化合物
 和八配位金属羰基化合物
和八配位金属羰基化合物 (TM=Y、La),为设计具有独特性质的化合物提供了新思路。它们的结构如图所示,CO作配体,配位原子为C,而不是O,其原因是
(TM=Y、La),为设计具有独特性质的化合物提供了新思路。它们的结构如图所示,CO作配体,配位原子为C,而不是O,其原因是 含
含 键。
键。
(2)工业上用CO合成
 :
:
 。
。①该反应在较低温度下能自发进行,推测该反应是
A.熵增、焓减反应 C.熵减、焓增反应
B.熵增、焓增反应 D.熵减、焓减反应
②一定温度下,向一恒容密闭容器中充入1molCO和
 ,下列情况表明净反应速率(净反应速率等于正、逆反应速率之差)一定等于0的是
,下列情况表明净反应速率(净反应速率等于正、逆反应速率之差)一定等于0的是A.混合气体密度不随时间变化
B.混合气体中CO的体积分数不随时间变化
C.混合气体总压强不随时间变化
D.
 的正反应速率等于
的正反应速率等于 的逆反应速率的3倍
的逆反应速率的3倍(3)工业上常用天然气制备CO,原理如下:
①


②


则


 、
、 的代数式表示)
的代数式表示)(4)光气 (COCl2)是一种有机中间体,常用于合成杀虫剂、黏合剂。CO合成光气的原理是

 。在甲、乙起始体积均为2L的密闭容器中均分别投入2molCO和
。在甲、乙起始体积均为2L的密闭容器中均分别投入2molCO和 ,在不同条件下发生上述反应,测得
,在不同条件下发生上述反应,测得 与时间关系如图所示。
与时间关系如图所示。
①相对甲,乙仅改变一个条件,可能是
a.减小压强 b.加催化剂 c.降低温度
②若在恒容条件下反应,前10min内乙容器中CO的平均反应速率为
 。甲容器中CO的平衡转化率为
。甲容器中CO的平衡转化率为 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】氢能作为一种清洁、高效、安全、可持续的新能源,被视为21世纪最具发展潜力的清洁能源,是人类的战略能源发展方向。目前,制备氢气有多种途径:途径一:甲醇产生氢气的反应为:
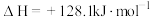
(1)已知相关物质的标准熵数值如下表:
该反应能自发进行的最低温度为___________ K。(保留小数点后1位)
途径二:乙酸制氢的反应为:
反应I: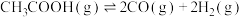
反应Ⅱ: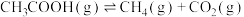
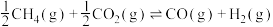

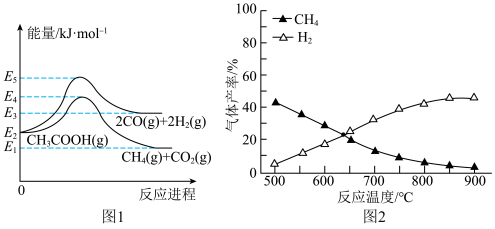
①由图1可得,
___________ kJ·mol-1;
②恒温恒容下发生上述反应,下列说法正确的是___________ 。
A.混合气体密度不变时,反应达到平衡
B.充入CO2,可提高CH4的转化率
C.加入催化剂,可提高H2的平衡产率
D.充入Ar,对H2的产率不产生影响
(3)一定条件下,在密闭容器中加入一定量的乙酸,只发生反应I和反应Ⅱ。
①在相同时间,测得温度与气体产率的关系如上图2所示。约650℃之前,氢气产率低于甲烷的可能原因是___________ 。
②设达到平衡时,体系总压强为p,乙酸体积分数为20%,反应I消耗的乙酸占投入量的20%,则反应Ⅱ的平衡常数 为
为___________ 。(用平衡分压代替平衡浓度计算)
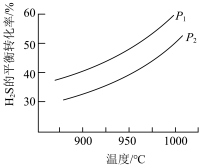
途径三:热分解H2S制氢的反应为: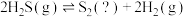
(4)不同温度和压强下,H2S的平衡转化率变化如图。生成物S2的状态为___________ (填“气态”或“非气态”),P1___________ P2(填“>”或“<”)。

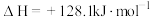
(1)已知相关物质的标准熵数值如下表:
| 化学式 |  |  |  |
标准熵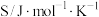 | 126.8 | 130.7 | 197.7 |
途径二:乙酸制氢的反应为:
反应I:
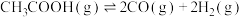
反应Ⅱ:
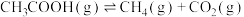
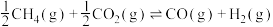

①由图1可得,

②恒温恒容下发生上述反应,下列说法正确的是
A.混合气体密度不变时,反应达到平衡
B.充入CO2,可提高CH4的转化率
C.加入催化剂,可提高H2的平衡产率
D.充入Ar,对H2的产率不产生影响
(3)一定条件下,在密闭容器中加入一定量的乙酸,只发生反应I和反应Ⅱ。
①在相同时间,测得温度与气体产率的关系如上图2所示。约650℃之前,氢气产率低于甲烷的可能原因是
②设达到平衡时,体系总压强为p,乙酸体积分数为20%,反应I消耗的乙酸占投入量的20%,则反应Ⅱ的平衡常数
 为
为途径三:热分解H2S制氢的反应为:
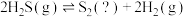
(4)不同温度和压强下,H2S的平衡转化率变化如图。生成物S2的状态为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】几种短周期元素的原子半径及主要化合价如下表:已知X是短周期中最活泼的金属,且与R同周期。(请用化学用语答题)
(1)R的元素符号为___ ,M在元素周期表中的位置为___ 。
(2)X与Y按原子个数比1∶1构成的物质的电子式为___ ,所含化学键类型___ 。
(3)X+、Y2-、M2-离子半径大小顺序为___ 。
(4)将YM2通入FeCl3溶液中的离子方程式:___ 。
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6 -2 | +5 -3 | -2 | +3 |
(2)X与Y按原子个数比1∶1构成的物质的电子式为
(3)X+、Y2-、M2-离子半径大小顺序为
(4)将YM2通入FeCl3溶液中的离子方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】自然界中存在一种天然硅铝酸盐,它们具有筛选分子、吸附、离子交换和催化作用。这种天然物质称为沸石,人工合成的沸石也被称为分子筛。回答下列问题:
(1)某同学写出了铝原子的4种不同状态的电子排布图:
A.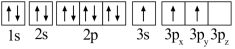 B.
B.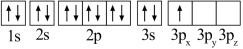
C.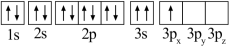 D.
D.
其中能量最低的是_____ (填字母),状态A中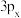 的电子云轮廓图为
的电子云轮廓图为_____ ,状态C电子排布图有错误,主要不符合_____ 。
(2)沸石分子筛“SAPO-34”是一种高性能催化剂,该催化剂可将乙醇催化转化为丙烯。
①分子筛中存在 ,该化合物中存在的化学键类型为
,该化合物中存在的化学键类型为_____ (填字母),该化合物阴离子的空间构型是___________ 。
A.配位键 B.氢键 C.非极性键 D.离子键 E.金属键
②丙烯中碳原子的杂化类型为___________ ,0.5mol丙烯中含___________ mol 键。
键。
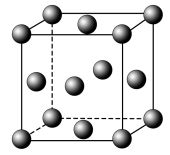
(3)金属铝的晶胞结构如图所示,其晶胞参数为0.405nm。金属铝的堆积方式为___________ ,铝原子的半径为___________ nm(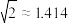 ,结果保留3位小数),铝单质的密度为
,结果保留3位小数),铝单质的密度为___________  (阿伏加德罗常数用
(阿伏加德罗常数用 表示,只列出算式即可)。
表示,只列出算式即可)。
(1)某同学写出了铝原子的4种不同状态的电子排布图:
A.
 B.
B.
C.
 D.
D.
其中能量最低的是
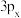 的电子云轮廓图为
的电子云轮廓图为(2)沸石分子筛“SAPO-34”是一种高性能催化剂,该催化剂可将乙醇催化转化为丙烯。
①分子筛中存在
 ,该化合物中存在的化学键类型为
,该化合物中存在的化学键类型为A.配位键 B.氢键 C.非极性键 D.离子键 E.金属键
②丙烯中碳原子的杂化类型为
 键。
键。(3)金属铝的晶胞结构如图所示,其晶胞参数为0.405nm。金属铝的堆积方式为
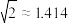 ,结果保留3位小数),铝单质的密度为
,结果保留3位小数),铝单质的密度为 (阿伏加德罗常数用
(阿伏加德罗常数用 表示,只列出算式即可)。
表示,只列出算式即可)。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】A、B、C、D、E、F、G为短周期元素,原子序数依次增大。A、B两元素最高正价和最低负价代数和为零;D是地壳中含量最高的非金属元素;E和A同主族,G与D同主族;E、F、G的最高价氧化物的水化物两两之间可以反应。
(1)G元素的名称是__________ ,其在周期表中的位置是_____________ ,其离子结构示意图为_____________ 。
(2) 的电子式
的电子式_____________ ;由A、C原子个数比为5∶1组成的一种化合物,其中各原子均达到稳定结构,该化合物中所含化学键类型为_____________ 。
(3)B、C形成的最高价氧化物的水化物,酸性由强到弱的顺序为_____________ (用分子式表示,下同);D和G的简单氢化物沸点的由高到低的顺序为_____________ 。
(4)E和F分别对应的最高价氧化物的水化物相互反应的离子方程式________________ 。
(5)由C、E组成的一种离子化合物的化学式为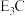 ,该化合物中两种离子的半径由大到小的顺序是(用离子符号表示)
,该化合物中两种离子的半径由大到小的顺序是(用离子符号表示)_________________________ ;该化合物遇水剧烈反应,有刺激性气味的气体生成,该反应的化学方程式为___________________________ 。
(1)G元素的名称是
(2)
 的电子式
的电子式(3)B、C形成的最高价氧化物的水化物,酸性由强到弱的顺序为
(4)E和F分别对应的最高价氧化物的水化物相互反应的离子方程式
(5)由C、E组成的一种离子化合物的化学式为
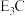 ,该化合物中两种离子的半径由大到小的顺序是(用离子符号表示)
,该化合物中两种离子的半径由大到小的顺序是(用离子符号表示)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为1。元素Y基态原子的3p轨道上有5个电子。元素Z的原子最外层电子数是其内层的3倍。元素W基态原子核外电子共有16种运动状态。
⑴①在元素周期表中,元素Y位于第___________ 周期第___________ 族,元素X位于___________ 区;
②Z所在周期中,第一电离能最大的元素是___________ ;(填元素名称)
③X+的核外电子排布式为___________ ;与X同一周期的副族元素的基态原子中最外层电子数与铜原子相同的元素有___________ (填元素符号)
④Y和W两元素所形成的最高价氧化物对应的水化物酸性较强的是___________ (填化学式)
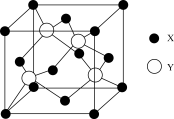
⑵X与Y所形成化合物晶体的晶胞如图所示。
①在1个晶胞中,X离子的数目为___________
②该化合物的化学式为___________
⑶X与W的最高价含氧酸的浓溶液反应的化学方程式为___________
⑷①在乙醇中的溶解度:Z的氢化物(H2Z)大于H2W,其主要原因是___________
②稳定性:H2Z___________ H2W(填“<”、“>”或“=”),其主要原因是___________
⑴①在元素周期表中,元素Y位于第
②Z所在周期中,第一电离能最大的元素是
③X+的核外电子排布式为
④Y和W两元素所形成的最高价氧化物对应的水化物酸性较强的是
⑵X与Y所形成化合物晶体的晶胞如图所示。

①在1个晶胞中,X离子的数目为
②该化合物的化学式为
⑶X与W的最高价含氧酸的浓溶液反应的化学方程式为
⑷①在乙醇中的溶解度:Z的氢化物(H2Z)大于H2W,其主要原因是
②稳定性:H2Z
您最近一年使用:0次
【推荐2】X、T、Y、Z为1-36号元素,且原子序数依次增大,四种元素的性质或结构信息如表。请根据信息回答下列问题。
(1)写出元素T原子外围电子的轨道表示式____ ;写出元素X的气态氢化物的电子式____ ;写出Z元素原子的外围电子排布式____ ;元素Y的原子核外共有____ 种形状不同的电子云。
(2)Y元素原子的第一电离能____ 镁(填“>”“<”“=”),从结构上分析,其理由是:___ 。
(3)元素T与氟元素相比,非金属性较强的是____ (用元素符号表示),下列表述中能证明这一事实的是____ (填序号字母)。
a.常温下氟气的颜色比T单质的颜色深
b.氟气与T的氢化物剧烈反应,产生T的单质
c.氟与T形成的化合物中T元素呈正价态
d.比较两元素的单质与氢气化合时得电子的数目
| 元素 | T | X | Y | Z |
| 性质结构信息 | 人体内含量最多的 元素,且其单质是 最常见的助燃剂 | 单质为双原子分子,分子中含有3对共用电子对,常温下单质性质稳定,但其原子较活泼 | 第3周期元素的简单离子中半径最小 | 第4周期元素,M电子层为全充满状态,最外层只有二个电子的原子 |
(2)Y元素原子的第一电离能
(3)元素T与氟元素相比,非金属性较强的是
a.常温下氟气的颜色比T单质的颜色深
b.氟气与T的氢化物剧烈反应,产生T的单质
c.氟与T形成的化合物中T元素呈正价态
d.比较两元素的单质与氢气化合时得电子的数目
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】磷化硼是一种典型的超硬无机材料,常以 、
、 为原料制备。回答下列问题:
为原料制备。回答下列问题:
(1)基态 原子与
原子与 原子中未成对电子数之比为
原子中未成对电子数之比为______ 。
(2) 分子的空间结构为
分子的空间结构为______ , 的沸点
的沸点______ (填“高于”或“低于”) ,理由是
,理由是______ 。
(3) 、
、 和
和 三种分子中键角由大到小的顺序为
三种分子中键角由大到小的顺序为______ 。
(4) 可转化为硼酸,硼酸为一元弱酸的原因是
可转化为硼酸,硼酸为一元弱酸的原因是______ 。(用离子方程表示)
(5)磷化硼晶胞的示意图如图甲所示,其中实心球表示P原子,空心球表示B原子。若磷化硼晶胞沿着体对角线方向的投影如图乙所示(虚线圆圈表示P原子的投影),请在图乙中用实线圆圈画出B原子的投影位置______ (注意原子体积的相对大小)。

 、
、 为原料制备。回答下列问题:
为原料制备。回答下列问题:(1)基态
 原子与
原子与 原子中未成对电子数之比为
原子中未成对电子数之比为(2)
 分子的空间结构为
分子的空间结构为 的沸点
的沸点 ,理由是
,理由是(3)
 、
、 和
和 三种分子中键角由大到小的顺序为
三种分子中键角由大到小的顺序为(4)
 可转化为硼酸,硼酸为一元弱酸的原因是
可转化为硼酸,硼酸为一元弱酸的原因是(5)磷化硼晶胞的示意图如图甲所示,其中实心球表示P原子,空心球表示B原子。若磷化硼晶胞沿着体对角线方向的投影如图乙所示(虚线圆圈表示P原子的投影),请在图乙中用实线圆圈画出B原子的投影位置

您最近一年使用:0次



