元素X、Y、Z、M、W在周期表中的位置如图:
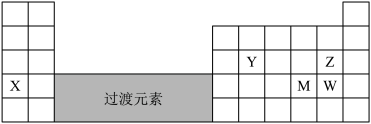
(1)X的元素符号是_________ 。
(2)YO2是玻璃的成分之一,是酸性氧化物。实验室盛装NaOH溶液的试剂瓶不能用玻璃塞的原因是:_________ +_________ OH-=_________ +_________ 。
(3)元素Z和元素W中,非金属性比较弱的是_________ (填元素符号)。在Z和W形成的原子个数比为1:1的化合物中,W的化合价是_________ 。
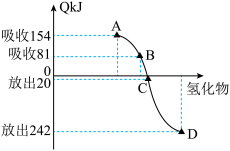
(4)元素M(Se)是人体必需的微量元素。Se能与H2反应生成H2Se,用原子结构解释原因_________ 。298K、1.01×105pa时,O2、S、Se、Te分别与H2化合生成1 mol气态氢化物时的热量的变化数据(Q)如下图所示。图中表示Se与H2化合的点是_________ (填字母)。

(1)X的元素符号是
(2)YO2是玻璃的成分之一,是酸性氧化物。实验室盛装NaOH溶液的试剂瓶不能用玻璃塞的原因是:
(3)元素Z和元素W中,非金属性比较弱的是
(4)元素M(Se)是人体必需的微量元素。Se能与H2反应生成H2Se,用原子结构解释原因

更新时间:2019-06-13 00:06:14
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某化学兴趣小组用如图实验装置和试剂,设计实验比较硫和氯的非金属性强弱,并收集纯净干燥的氯气,回答下列问题:(已知: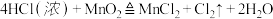 )
)

A B C D E F
(1)仪器a的名称为____________
(2)浓盐酸在A装置的反应中,既表现出酸性又表现出____________ 性(填“氧化性”或“还原性”)
(3)装置连接顺序为A-____________ -C-D
(4)F中反应的离子方程式为____________
(5)E装置的作用是____________ ,D装置中的试剂是____________
(6)从实验可知非金属性:硫______ 氯(填“>”或“<”)
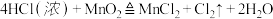 )
)
A B C D E F
(1)仪器a的名称为
(2)浓盐酸在A装置的反应中,既表现出酸性又表现出
(3)装置连接顺序为A-
(4)F中反应的离子方程式为
(5)E装置的作用是
(6)从实验可知非金属性:硫
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表为八种短周期主族元素的部分性质(已知铍的原子半径为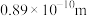 ):
):
(1)元素Z在元素周期表中的位置为___________ ,元素Y为___________ (填元素符号)。
(2)写出Q与J两种元素最高价氧化物对应的水化物之间反应的离子方程式:___________ 。
(3)R与T相比,非金属性较强的是___________ (填元素符号),下列事实能证明这一结论的是___________ (填标号)。
a.常温下T的单质呈固态,R的单质呈气态
b.稳定性: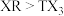
c.最高价氧化物对应水化物的酸性:
(4)J与Q相比,金属性较强的是___________ (填元素符号),能证明这一结论的依据是___________ 。
(5)根据表中数据推测,M的原子半径的最小范围是___________ 。
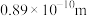 ):
):| 元素代号 | X | Y | Z | M | R | J | Q | T |
原子半径 | 0.74 | 0.75 | r | 0.99 | 1.86 | 1.43 | 1.10 | |
| 主要化合价 |  |  、 、 |  、 、 |  、 、 |  |  |  、 、 | |
| 其他 | 原子核内无中子 | 重要的半导体材料 | 有两种氧化物 |
(2)写出Q与J两种元素最高价氧化物对应的水化物之间反应的离子方程式:
(3)R与T相比,非金属性较强的是
a.常温下T的单质呈固态,R的单质呈气态
b.稳定性:
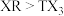
c.最高价氧化物对应水化物的酸性:

(4)J与Q相比,金属性较强的是
(5)根据表中数据推测,M的原子半径的最小范围是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】为验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如图实验,请回答下列问题:

(1)装置B中盛放的试剂是___ (填选项),实验现象为___ ,化学反应方程式是___ 。
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(2)装置C中盛放烧碱稀溶液,目的是___ 。反应的离子方程式是___ 。
(3)能证明氯元素比硫元素非金属性强的依据为___ 。(填序号)
①氯原子比硫原子更容易获得电子形成离子
②次氯酸的氧化性比稀硫酸强
③S2-比Cl-还原性强
④HCl比H2S稳定
(4)若B瓶中盛放KI溶液和CCl4试剂,实验后,振荡、静置,会出现分层,下层呈紫红色的实验现象,若B瓶中通入标准状况下44.8L氯气全部参加反应,则转移的电子数目是___ 。

(1)装置B中盛放的试剂是
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(2)装置C中盛放烧碱稀溶液,目的是
(3)能证明氯元素比硫元素非金属性强的依据为
①氯原子比硫原子更容易获得电子形成离子
②次氯酸的氧化性比稀硫酸强
③S2-比Cl-还原性强
④HCl比H2S稳定
(4)若B瓶中盛放KI溶液和CCl4试剂,实验后,振荡、静置,会出现分层,下层呈紫红色的实验现象,若B瓶中通入标准状况下44.8L氯气全部参加反应,则转移的电子数目是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表的一部分,表中所列的数字代表某一化学元素,请回答下列问题:
(1)③在元素周期表中的位置是第二周期_______ 族,该元素的一种核素含8个中子,其原子符号为_______ ,元素⑩的原子结构示意图为_______ 。
(2)编号的10种元素中化学性质最不活泼的是_______ (填元素符号);最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式)。
(3)②⑥⑧三种元素中,离子半径从大到小的顺序为_______ (填离子符号)。
(4)元素⑤对应简单氢化物在常温下与⑩构成的单质发生反应的化学方程式为_______ 。元素⑦的氧化物与元素②的最高价氧化物对应的水化物发生反应的离子方程式是_______ 。
族 周期 | ||||||||||||||||||
| 1 | ① | |||||||||||||||||
| 2 | ③ | ④ | ⑤ | |||||||||||||||
| 3 | ② | ⑥ | ⑦ | ⑧ | ⑨ | |||||||||||||
| 4 | ⑩ |
(2)编号的10种元素中化学性质最不活泼的是
(3)②⑥⑧三种元素中,离子半径从大到小的顺序为
(4)元素⑤对应简单氢化物在常温下与⑩构成的单质发生反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为____________ 。
(2)用电子式表示②与④形成化合物的过程_____________ 。
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是______ ,碱性最强的是________________ ,呈两性的氢氧化物是________________ 。
(4)写出⑤的氢氧化物与氢氧化钠溶液反应的离子方程式:_____________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
四 | ⑨ | ⑩ |
(2)用电子式表示②与④形成化合物的过程
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是
(4)写出⑤的氢氧化物与氢氧化钠溶液反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】现有短周期元素A、B、C、D。A元素M层上有2对成对电子,D与A在周期表中同一主族。由A、B与D组成的化合物的浓溶液是常见的干燥剂,常温下C单质为双原子分子,其氢化物水溶液呈碱性,是一种重要肥料。
(1)A的原子最外层共有___ 种不同运动状态的电子,该原子共有___ 种不同能量的电子,能量最高的电子占有___ 个轨道,其电子云形状为____ 。
(2)元素A、B与D组成的化合物的浓溶液是常见干燥剂,该化合物在实验室制备乙酸乙酯时所起的作用:_____ 。
(3)B与C元素形成带一个单位正电荷的离子,写出该微粒的电子式____ 。
(4)元素A与元素D相比,非金属性较强的是____ (用元素符号表示),下列表述中能表明这一事实的是____ 。
①比较最高价氧化物对应水化物的酸性
②比较对应气态氢化物的稳定性
③一定条件下D能从A的氢化物水溶液中置换出A单质
④A单质的熔沸点明显高于D单质
从原子结构分析A和D非金属强弱的原因_____ 。
(5)C原子的原子结构示意图:_____ ,C的氢化物固态时属于____ 晶体。
(1)A的原子最外层共有
(2)元素A、B与D组成的化合物的浓溶液是常见干燥剂,该化合物在实验室制备乙酸乙酯时所起的作用:
(3)B与C元素形成带一个单位正电荷的离子,写出该微粒的电子式
(4)元素A与元素D相比,非金属性较强的是
①比较最高价氧化物对应水化物的酸性
②比较对应气态氢化物的稳定性
③一定条件下D能从A的氢化物水溶液中置换出A单质
④A单质的熔沸点明显高于D单质
从原子结构分析A和D非金属强弱的原因
(5)C原子的原子结构示意图:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】如表列出了A~R9种元素在周期表中的位置,用化学用语回答:
(1)这九种元素中化学性质最不活泼的是___ 。
(2)D元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是__ 。
(3)A、B、C三种元素按原子半径由大到小的顺序排列为__ 。
(4)F、G、H三种元素简单氢化物沸点由高到低的顺序__ 。
(5)E元素氧化物的电子式是__ ,F的氢化物在常温下跟B反应的化学方程式是__ 。
(6)下列事实能用元素周期律解释的是(填字母序号)__ 。
A.D的最高价氧化物对应水化物的碱性弱于Mg(OH)2
B.G的气态氢化物的稳定性弱于HF
C.FeG3的溶液可用于刻蚀铜制的印刷电路板
(7)G的单质可以从NaBr溶液中置换出Br2单质,从原子结构的角度解释其原因:_____ 。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |  |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H |
(2)D元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是
(3)A、B、C三种元素按原子半径由大到小的顺序排列为
(4)F、G、H三种元素简单氢化物沸点由高到低的顺序
(5)E元素氧化物的电子式是
(6)下列事实能用元素周期律解释的是(填字母序号)
A.D的最高价氧化物对应水化物的碱性弱于Mg(OH)2
B.G的气态氢化物的稳定性弱于HF
C.FeG3的溶液可用于刻蚀铜制的印刷电路板
(7)G的单质可以从NaBr溶液中置换出Br2单质,从原子结构的角度解释其原因:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】W、X、Y、Z为1~18号元素内除稀有气体外的4种元素,它们的原子序数依次增大,其中只有Y为金属元素。Y和W的最外层电子数相等。Y、Z两元素原子的质子数之和为W、X两元素质子数之和的3倍。
(1)写出元素符号:W为____ ,X为____ ,Y为____ ,Z为____ 。
(2)X的原子结构示意图为__________ ,Y___________ (填“得到”或“失去”)电子时,形成的离子结构示意图为________________ ;Z得到电子,形成的阴离子的电子式为_____________ .
(3)由X、Y、Z形成的一种化合物的电离方程式______________________ .
(1)写出元素符号:W为
(2)X的原子结构示意图为
(3)由X、Y、Z形成的一种化合物的电离方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成共价化合物XH3、H2Z和HW;Y与氧元素可组成离子化合物Y2O和Y2O2。
(1)写出Y2O2的电子式___________ ;其中含有的化学键是___________ ;
(2)X、Z、W三种元素的最高价氧化物对应的水化物酸性最强的是___________ (填化学式);
(3)XH3、H2Z和HW三种化合物,其中一种与另外两种都能反应的是___________ ;生成物属于_______ (填“离子”或“共价”)化合物;
(4)写出下列物质的电子式:
①XW3:___________ ;②Y3Z:___________ ;
(5)X的气态氢化物的结构式:___________ 。
(1)写出Y2O2的电子式
(2)X、Z、W三种元素的最高价氧化物对应的水化物酸性最强的是
(3)XH3、H2Z和HW三种化合物,其中一种与另外两种都能反应的是
(4)写出下列物质的电子式:
①XW3:
(5)X的气态氢化物的结构式:
您最近一年使用:0次



