现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A与D同主族,C与E同主族,D、E、F同周期,A、B的最外层电子数之和与C的最外层电子数相等,A能分别与B、C形成电子数相等的分子,且A与C形成的化合物常温下为液态,A能分别与E、F形成电子总数相等的气体分子.请回答下列问题(题中字母只代表元素代号,与实际元素符号无关):
(1)B、F可形成三角锥形分子,其电子式为______________
(2)B、C、E的气态氢化物沸点由高到低的顺序为:___________________
(3)C、E形成的化合物通入F的单质的水溶液中,可形成两种强电解质,则该反应的离子方程式为:__________________________________________ 。
(4)A、B、C可形成常见的化合物H,足量的H的稀溶液与a g Fe完全反应,被还原的H的物质的量为:________________ 。
(1)B、F可形成三角锥形分子,其电子式为
(2)B、C、E的气态氢化物沸点由高到低的顺序为:
(3)C、E形成的化合物通入F的单质的水溶液中,可形成两种强电解质,则该反应的离子方程式为:
(4)A、B、C可形成常见的化合物H,足量的H的稀溶液与a g Fe完全反应,被还原的H的物质的量为:
9-10高一下·湖南长沙·期末 查看更多[1]
(已下线)09~10年长沙同升湖实验学校高一下学期期末考试化学卷
更新时间:2016-12-09 00:44:43
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】我们通过高中化学课的学习已经掌握了元素周期律、周期表部分的相关内容,下面我们试着检测一下自己的学习效果吧。如表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语 回答下列问题:
(1)④、⑤、⑥的原子半径由大到小的顺序为____ 。
(2)②、③、⑧的最高价含氧酸的酸性由强到弱的顺序是____ 。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式____ 。
(4)由表中两种元素的原子按1︰1组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号)____ 。
a.MnO2 b.Na2SO3 c.KMnO4
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:____ ,N→⑥的单质的化学方程式为____ 。
(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由上表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L 2.2mol/L NaOH溶液和1mol O2,则两种气体分子式及物质的量分别为____ 。
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)②、③、⑧的最高价含氧酸的酸性由强到弱的顺序是
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式
(4)由表中两种元素的原子按1︰1组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号)
a.MnO2 b.Na2SO3 c.KMnO4
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:

(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由上表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L 2.2mol/L NaOH溶液和1mol O2,则两种气体分子式及物质的量分别为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫及铁的化合物。工业流程图如下:

(1)冶炼铜的总反应可看做:8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2,若CuFeS2中Fe的化合价为+2,反应中被还原的元素是
8Cu+4FeO+2Fe2O3+16SO2,若CuFeS2中Fe的化合价为+2,反应中被还原的元素是_____ (填元素符号),1molCuFeS2参与反应转移电子的物质的量为____ mol;
(2)上述冶炼过程产生大量气体A。下列处理方案中合理的是____ (填代号);
A.高空排放
B.用于制备硫酸
C.用纯碱溶液吸收制Na2SO4
D.用浓硫酸吸收
验证气体A的主要成分是SO2的方法是____________________________________ ;
(3)炉渣B(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。
A.加入H2O2发生反应的离子方程式是______________________________________ ;
B.除去Al3+的离子方程式是____________________________________ ;
(4)选用提供的试剂,设计实验验证炉渣B中含有FeO。
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水
所选试剂为______________________________ ;
证明炉渣中含有FeO的实验现象为___________________________________ 。

(1)冶炼铜的总反应可看做:8CuFeS2+21O2
 8Cu+4FeO+2Fe2O3+16SO2,若CuFeS2中Fe的化合价为+2,反应中被还原的元素是
8Cu+4FeO+2Fe2O3+16SO2,若CuFeS2中Fe的化合价为+2,反应中被还原的元素是(2)上述冶炼过程产生大量气体A。下列处理方案中合理的是
A.高空排放
B.用于制备硫酸
C.用纯碱溶液吸收制Na2SO4
D.用浓硫酸吸收
验证气体A的主要成分是SO2的方法是
(3)炉渣B(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。
A.加入H2O2发生反应的离子方程式是
B.除去Al3+的离子方程式是
(4)选用提供的试剂,设计实验验证炉渣B中含有FeO。
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水
所选试剂为
证明炉渣中含有FeO的实验现象为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】高铁酸钠(Na2FeO4)易溶于水,是一种新型多功能水处理剂。已知Na2FeO4在强碱性溶液中会析出沉淀。其生产工艺流程如图所示:
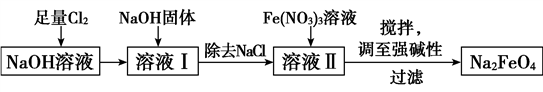
(1)写出向NaOH溶液中通入足量Cl2发生反应的离子方程式:_______________________________ 。
(2)向溶液Ⅱ中加入Fe(NO3)3溶液发生反应,该反应的氧化剂是____________ ,每制得49.8 g Na2FeO4,理论上消耗氧化剂的物质的量为____________ mol。
(3)从环境保护的角度看,制备Na2FeO4较好的方法为电解法,其装置如图甲所示。
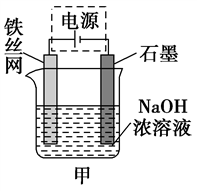
①电解过程中阳极的电极反应式为___________________________________________ 。
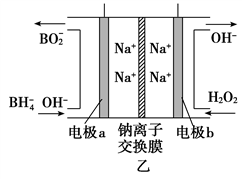
②图甲装置中的电源采用NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,电源工作原理如图乙所示。工作过程中该电源的正极反应式为______________ ,Na+由____________ (填“a”或“b”,下同)极区移向____________ 极区。

(1)写出向NaOH溶液中通入足量Cl2发生反应的离子方程式:
(2)向溶液Ⅱ中加入Fe(NO3)3溶液发生反应,该反应的氧化剂是
(3)从环境保护的角度看,制备Na2FeO4较好的方法为电解法,其装置如图甲所示。

①电解过程中阳极的电极反应式为
②图甲装置中的电源采用NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,电源工作原理如图乙所示。工作过程中该电源的正极反应式为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下表为九种主族元素在周期表中的位置:
请回答下列问题:
(1)I元素的位置是第________ 周期,第______ 族。
(2)C、B、D 三种元素的金属性由强到弱的顺序为_______ (填元素符号)。
(3)E、F两种元素对应的最简单氢化物的稳定性:________________ (填化学式)。
(4)C的单质与水反应的离子方程式为_______ 。
(5)用电子式表示A和G形成化合物的过程:____ 。
| A | |||||||
| E | F | ||||||
| B | D | I | G | ||||
| C | H | ||||||
请回答下列问题:
(1)I元素的位置是第
(2)C、B、D 三种元素的金属性由强到弱的顺序为
(3)E、F两种元素对应的最简单氢化物的稳定性:
(4)C的单质与水反应的离子方程式为
(5)用电子式表示A和G形成化合物的过程:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E都是短周期的主族元素,原子序数依次增大,A、B处于同周期,C、D、E同处另一周期,C、A可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙,D是地壳中含量最高的金属元素,E的最高价氧化物对应的水化物是酸性最强的含氧酸。回答下列问题:
(1)B和E分别对应的氢化物的化学式为HB、HE,氢化物的沸点HB_______ HE(填“>”、“<”、“=”,下同),氢化物的稳定性HB_______ HE。
(2)物质乙的电子式为_______ ;物质乙可用于呼吸面具作供氧剂,写出乙与CO2反应的化学方程式:_______ 。
(3)1mol单质B的气体与1molC的氢氧化物在一定条件下恰好完全反应,生成一种盐、水及另一种气体,则所得气体的化学式为:_______ 。
(1)B和E分别对应的氢化物的化学式为HB、HE,氢化物的沸点HB
(2)物质乙的电子式为
(3)1mol单质B的气体与1molC的氢氧化物在一定条件下恰好完全反应,生成一种盐、水及另一种气体,则所得气体的化学式为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
真题
解题方法
【推荐3】a、b、c、d、e是短周期元素,周期表中a与b、b与c相邻,c与e同族;a与c的最外层电子数之比为2∶3,b的最外层电子数比c的最外层电子数少1个;常见化合物d2c2与水反应生成c的单质,且溶液使酚酞试液变红。
(1)e的元素符号是_____________
(2)a、b、c的氢化物稳定性顺序为(用分子式表示)_____________ ;b的氢化物和b的最高价氧化物的水化物反应生成Z,则Z中的化学键类型为___________ ,Z的晶体类型为__________ ;ab-离子的电子式为____________
(3)由a、c、d形成化合物的水溶液显碱性,其原因是(用离子方程式表示)________
(4)一定量的d2c2与ac2反应后的固体物质,恰好与0.8mol稀盐酸溶液完全反应,并收集到0.25mol气体,则用物质的量表示该固体物质的组成为_________ .
(1)e的元素符号是
(2)a、b、c的氢化物稳定性顺序为(用分子式表示)
(3)由a、c、d形成化合物的水溶液显碱性,其原因是(用离子方程式表示)
(4)一定量的d2c2与ac2反应后的固体物质,恰好与0.8mol稀盐酸溶液完全反应,并收集到0.25mol气体,则用物质的量表示该固体物质的组成为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】D、E、X、Y、Z为原子序数依次增大的短周期主族元素,它们的简单氢化物分子的空间结构依次是正四面体形、三角锥形、正四面体形、V形、直线形。回答下列问题:
(1)Y的最高价氧化物的化学式为_______ 。
(2)上述五种元素中,能形成酸性最强的含氧酸的元素是_______ ,该元素的任意3种含氧酸的化学式为_______ 。
(3)D和Y形成的化合物,其分子的空间结构为_______ 。
(4)D和X形成的化合物,其化学键类型属于_______ (填“共价键”或“离子键”)。
(5)金属镁和E的单质在高温下反应得到的产物是_______ (写化学式)。该产物与水反应生成两种碱,反应的化学方程式是_______ 。
(1)Y的最高价氧化物的化学式为
(2)上述五种元素中,能形成酸性最强的含氧酸的元素是
(3)D和Y形成的化合物,其分子的空间结构为
(4)D和X形成的化合物,其化学键类型属于
(5)金属镁和E的单质在高温下反应得到的产物是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】几种元素的主要化合价如下表所示。
已知B、C、D位于同周期。
请回答下列问题:
(1)C的简单离子的结构示意图为_______ 。A是_______ (填元素名称)。
(2)D的简单氢化物的电子式为_______ 。
(3)D的简单氢化物与D的氧化物能发生氧化还原反应,在该反应中氧化产物与还原产物的物质的量之比为2:1,该反应的化学方程式为_______ 。
(4)已知:化合物BA在熔融状态下能导电,则化合物BA是_______ (填“共价”或“离子”)化合物。
(5)B的单质在O2中燃烧的产物能和A的简单氧化物反应,其离子方程式为_______ 。
(6)设计实验证明B元素原子的失电子能力比C的强:_______ (简要叙述实验过程、现象)。
| 元素代号 | A | B | C | D |
| 原子半径/nm | 0.030 | 0.186 | 0.143 | 0.106 |
| 主要化合价 | +1,—1 | +1 | +3 | +6,—2 |
请回答下列问题:
(1)C的简单离子的结构示意图为
(2)D的简单氢化物的电子式为
(3)D的简单氢化物与D的氧化物能发生氧化还原反应,在该反应中氧化产物与还原产物的物质的量之比为2:1,该反应的化学方程式为
(4)已知:化合物BA在熔融状态下能导电,则化合物BA是
(5)B的单质在O2中燃烧的产物能和A的简单氧化物反应,其离子方程式为
(6)设计实验证明B元素原子的失电子能力比C的强:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】短周期主族元素X、Y、Z、M、R、W的原子序数依次增大。X原子是周期表中半径最小的原子,Y原子的最外层电子数是其内层电子数的2倍,Z是地壳中含量最高的元素,M+、R2+与Z2-具有相同的电子层结构,W与M组成的化合物是生活中必备的调味品。根据题给信息按要求回答下列问题。
(1)元素Y在元素周期表中的位置为____________________ 。
(2)M、W各自的最高价氧化物对应水化物相互反应的离子方程式为_____ 。
(3)为比较M、R的活泼性,将其单质分别投入______ (试剂)中,根据反应的剧烈程度,可证明活泼性强的是_______ (填元素符号)。
(4)由Y与X组成的质量比为5∶1的有机物的化学式为__________ ,写出其所有分子的结构简式________________________________________________ 。
(1)元素Y在元素周期表中的位置为
(2)M、W各自的最高价氧化物对应水化物相互反应的离子方程式为
(3)为比较M、R的活泼性,将其单质分别投入
(4)由Y与X组成的质量比为5∶1的有机物的化学式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
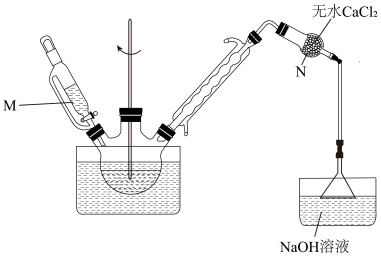
【推荐1】邻乙酰水杨酰氯(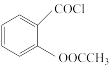 )是制备贝诺酯(一种非甾体抗风湿解热镇痛药)的中间产物。实验室制备邻乙酰水杨酰氯的装置如下图所示:
)是制备贝诺酯(一种非甾体抗风湿解热镇痛药)的中间产物。实验室制备邻乙酰水杨酰氯的装置如下图所示:
步骤1:取18.0g阿司匹林(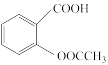 )置于三颈烧瓶中,加入2~3滴DMF;
)置于三颈烧瓶中,加入2~3滴DMF;
步骤2:向三颈烧瓶中滴加氯化亚砜(SOCl2);
步骤3:70℃下充分反应后,除去过量的SOCl2,经一系列操作即可得到邻乙酰水杨酰氯。
已知:①反应原理为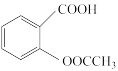 +SOCl2
+SOCl2
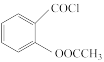 +SO2↑+HCl↑
+SO2↑+HCl↑
②有关物质的沸点如下表所示:
③氯化亚砜和邻乙酰水杨酰氯均易水解。
回答下列问题:
(1)仪器M的名称是_____ ,在本实验中使用它的原因是______ 。
(2)三颈烧瓶宜采用水浴加热,该加热方式的优点是_____ 。
(3)实验中选用球形冷凝管而不选用直形冷凝管的原因是_____ ;干燥管中的无水CaCl2若更换为_____ 试剂,则可省去尾气吸收的NaOH溶液及其装置。
(4)反应物SOCl2的空间结构名称是______ 。
(5)阿司匹林的沸点高于邻乙酰水杨酰氯的原因可能是______ 。
(6)反应温度适宜选取70℃的原因是___ ;除去过量SOCl2宜采用____ 方法。
 )是制备贝诺酯(一种非甾体抗风湿解热镇痛药)的中间产物。实验室制备邻乙酰水杨酰氯的装置如下图所示:
)是制备贝诺酯(一种非甾体抗风湿解热镇痛药)的中间产物。实验室制备邻乙酰水杨酰氯的装置如下图所示:
步骤1:取18.0g阿司匹林(
 )置于三颈烧瓶中,加入2~3滴DMF;
)置于三颈烧瓶中,加入2~3滴DMF;步骤2:向三颈烧瓶中滴加氯化亚砜(SOCl2);
步骤3:70℃下充分反应后,除去过量的SOCl2,经一系列操作即可得到邻乙酰水杨酰氯。
已知:①反应原理为
 +SOCl2
+SOCl2
 +SO2↑+HCl↑
+SO2↑+HCl↑②有关物质的沸点如下表所示:
| 物质 | SOCl2 | 阿司匹林 | 邻乙酰水杨酰氯 |
| 沸点/℃ | 79 | 321 | 107~110 |
回答下列问题:
(1)仪器M的名称是
(2)三颈烧瓶宜采用水浴加热,该加热方式的优点是
(3)实验中选用球形冷凝管而不选用直形冷凝管的原因是
(4)反应物SOCl2的空间结构名称是
(5)阿司匹林的沸点高于邻乙酰水杨酰氯的原因可能是
(6)反应温度适宜选取70℃的原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】短周期元素X、Y、W的原子序数依次增大,元素X的一种单质有杀菌消毒的作用,Y与X的某种化合物A可以作潜水艇的供氧剂。 W质子数为偶数,室温下W单质为黄色固体。生活中常见元素M的一种氧化物有磁性,回答下列问题:
(1)W元素位于周期表中的第________ 周期、_________ 族。
(2)写出化合物A的电子式____________ 。用电子式表示W元素气态氢化物的形成过程____________ 。
(3)X的简单氢化物与M的单质在高温下反应的化学方程式为__________
(4)X的氢化物沸点高于W的氢化物沸点,原因是___________
(1)W元素位于周期表中的第
(2)写出化合物A的电子式
(3)X的简单氢化物与M的单质在高温下反应的化学方程式为
(4)X的氢化物沸点高于W的氢化物沸点,原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】回答下列问题
(1)Sn为ⅣA族元素,单质Sn与干燥Cl2反应生成SnCl4.常温常压下SnCl4为无色液体,SnCl4空间构型为___________ ,其固体的晶体类型为___________ 。
(2)NH3、PH3、AsH3的沸点由高到低的顺序为___________ (填化学式,下同),还原性由强到弱的顺序为___________ ,键角由大到小的顺序为___________ 。
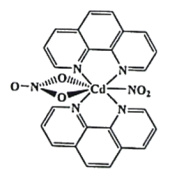
(3)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种Cd2+配合物的结构如图所示,1mol该配合物中通过螯合作用形成的配位键有___________ mol,该螯合物中N的杂化方式有___________ 种。
(1)Sn为ⅣA族元素,单质Sn与干燥Cl2反应生成SnCl4.常温常压下SnCl4为无色液体,SnCl4空间构型为
(2)NH3、PH3、AsH3的沸点由高到低的顺序为
(3)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种Cd2+配合物的结构如图所示,1mol该配合物中通过螯合作用形成的配位键有

您最近一年使用:0次



