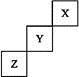
下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:___________ (填元素符号)。
(2)在最高价氧化物对应的水化物中,酸性最强的化合物的分子_________ ,碱性最强的化合物的电子式是:____________ 。
(3)用电子式表示元素④与⑥的化合物的形成过程:______________ 。
(4)表示①与⑦的化合物的电子式__________ ,该化合物是由__________ (填“极性”或“非极性”)键形成的。
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是___________ (用化学式表示)。
(提示:一般认为,粒子半径与粒子的电子层数及核内质子数有关,当电子层数不同时,电子层数越多,粒子半径越大,当电子层数相同时,质子数越多,粒子半径越小,所以建议先画出粒子结构示意图,再进行比较)
(6)元素③的简单氢化物的结构式__________ ,在常温下和元素⑦的单质反应的离子方程式_________ 。
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 |
| 第二周期 | ① | ② | ③ | |||||
| 第三周期 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 第四周期 | ⑨ | ⑩ |
(1)在这些元素中,化学性质最不活泼的是:
(2)在最高价氧化物对应的水化物中,酸性最强的化合物的分子
(3)用电子式表示元素④与⑥的化合物的形成过程:
(4)表示①与⑦的化合物的电子式
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是
(提示:一般认为,粒子半径与粒子的电子层数及核内质子数有关,当电子层数不同时,电子层数越多,粒子半径越大,当电子层数相同时,质子数越多,粒子半径越小,所以建议先画出粒子结构示意图,再进行比较)
(6)元素③的简单氢化物的结构式
更新时间:2020-08-19 15:27:25
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】有A、B、C、D、E五种元素,其中A、B、C位于同周期,A原子最外层p轨道电子数等于次外层的电子总数,B元素可分别与A、C、D、E生成 型化合物,已知在
型化合物,已知在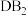 和
和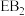 中,D与B的质量比为7:8,E与B的质量比为1:1。根据以上条件,回答下列问题:
中,D与B的质量比为7:8,E与B的质量比为1:1。根据以上条件,回答下列问题:
(1)画出C的原子结构示意图:______ 。
(2)写出D原子的价电子排布式:______ 。
(3)写出A元素的单质在B中完全燃烧的化学方程式:____________ 。
(4)指出E元素在周期表中的位置:______ 。
(5)A、B、C三种元素的第一电离能由大到小的顺序为______ (用元素符号表示)。
(6)比较元素D和E电负性的大小:______ (用元素符号表示)。
 型化合物,已知在
型化合物,已知在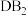 和
和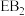 中,D与B的质量比为7:8,E与B的质量比为1:1。根据以上条件,回答下列问题:
中,D与B的质量比为7:8,E与B的质量比为1:1。根据以上条件,回答下列问题:(1)画出C的原子结构示意图:
(2)写出D原子的价电子排布式:
(3)写出A元素的单质在B中完全燃烧的化学方程式:
(4)指出E元素在周期表中的位置:
(5)A、B、C三种元素的第一电离能由大到小的顺序为
(6)比较元素D和E电负性的大小:
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】I.金属在生活中有着广泛的应用,人们甚至根据使用材料的种类,将人类漫长的历史分为了三个大的时代,分别是石器时代、青铜器时代,而后是铁器时代,直到19世纪早期,戴维组装了一个特别大的电池用于实验,先后发现了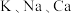 等许多金属。
等许多金属。
(1)造成上述人们利用金属先后顺序事实的最主要因素是_______。
(2)1827年维勒用金属钾还原熔融的无水氯化铝得到较纯的金属铝单质,但今天人们早已舍弃这种制备金属铝的方法,你认为可能的原因有_______ (写出一种合理原因即可)。写出现代工业上获得金属铝的化学反应方程式_______ 。
(3)已知铍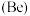 与铝的性质相似。则下列判断正确的是_______。
与铝的性质相似。则下列判断正确的是_______。
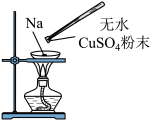
(4)钠是一种活泼的金属,将绿豆大的钠块投入如图所示的烧杯中,可能出现的现象_______。

(5)在蒸发皿中放一小块钠,加热至熔化成小球时,用玻璃棒蘸取少量无水 粉末与其接触,瞬间产生耀眼的火花,同时有红色物质生成。下列说法错误的是_______。
粉末与其接触,瞬间产生耀眼的火花,同时有红色物质生成。下列说法错误的是_______。
(6)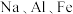 都是重要的金属元素。下列说法正确的是_______。
都是重要的金属元素。下列说法正确的是_______。
(7)类推的思维方法在化学学习中有时会产生错误结论,因此结论最终要经过实践的检验,才能决定其正确与否,下列几种关于金属的类推结论中,错误的是_______。
①钠与水反应生成 和
和 ;所有金属与水反应都生成碱和
;所有金属与水反应都生成碱和
②铁露置在空气中一段时间后就会生锈;性质更活泼的铝不能稳定存在于空气中
③ 与S直接化合时可得到
与S直接化合时可得到 ;
; 与S直接化合时也可得到
与S直接化合时也可得到
④ 受热易分解,
受热易分解,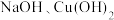 受热也易分解
受热也易分解
(8)单质A的燃烧热大。已知A为短周期元素,其气态原子逐个失去1~4个电子所需吸收能量如表所示。若该原子核外电子有三层,则该元素位于周期表_______ 族,写出A燃烧后形成的氧化物的电子式:_______ 。
Ⅱ.炼铁的主要原理之一是赤铁矿。它的主要成分在一定条件下有下列反应: 。在反应形成的固体混合物(
。在反应形成的固体混合物( 、
、 )中,元素铁和氧的质量比用
)中,元素铁和氧的质量比用 表示。
表示。
(9)根据上述反应,固体质量每减轻 ,将产生
,将产生
_______ L(S.T.P)。
(10)上述反应形成的固体混和物中, 不可能是_______。
不可能是_______。
(11) 也是铁重要的氧化物之一,其在高温下与金属铝反应,也能获得单质铁,写出相关的化学反应方程式
也是铁重要的氧化物之一,其在高温下与金属铝反应,也能获得单质铁,写出相关的化学反应方程式_______ 。
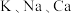 等许多金属。
等许多金属。(1)造成上述人们利用金属先后顺序事实的最主要因素是_______。
| A.地壳中金属元素的含量 | B.金属的延展性 |
| C.金属的导电性 | D.金属活泼性的差异 |
(3)已知铍
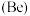 与铝的性质相似。则下列判断正确的是_______。
与铝的性质相似。则下列判断正确的是_______。| A.铍遇冷水剧烈反应 | B.氧化铍的化学式为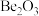 |
| C.氢氧化铍能与氢氧化钠溶液反应 | D. 能置换出 能置换出 中的镁单质 中的镁单质 |

| A.钠块在煤油、水两液体界面处反应,上下跳动,水层变红 |
| B.钠块只在煤油层中游动,并放出气体 |
| C.钠块只在水层中游动,钠块熔化,水层变红 |
| D.钠块在四氯化碳、水两液体界面处反应,熔化成小球并上下跳动,水层变红 |
 粉末与其接触,瞬间产生耀眼的火花,同时有红色物质生成。下列说法错误的是_______。
粉末与其接触,瞬间产生耀眼的火花,同时有红色物质生成。下列说法错误的是_______。
| A.钠受热易熔成小球说明其熔点低 |
B.钠与 粉末反应时放出大量热 粉末反应时放出大量热 |
C.一定条件下, 可与 可与 反应生成 反应生成 |
D.将无水 粉末改为 粉末改为 溶液,反应现象相同 溶液,反应现象相同 |
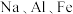 都是重要的金属元素。下列说法正确的是_______。
都是重要的金属元素。下列说法正确的是_______。| A.三者的最高价氧化物对应水化物均为碱性 | B.三者的氢氧化物都是白色固体 |
| C.三者的氯化物都可用化合反应制得 | D.三者的单质在空气中最终都生成氧化物 |
①钠与水反应生成
 和
和 ;所有金属与水反应都生成碱和
;所有金属与水反应都生成碱和
②铁露置在空气中一段时间后就会生锈;性质更活泼的铝不能稳定存在于空气中
③
 与S直接化合时可得到
与S直接化合时可得到 ;
; 与S直接化合时也可得到
与S直接化合时也可得到
④
 受热易分解,
受热易分解,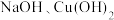 受热也易分解
受热也易分解| A.①② | B.③④ | C.①②③ | D.①②③④ |
 |  |  |  | …后续省略 | |
电离能( ) ) | 738 | 1451 | 7733 | 10540 | … |
Ⅱ.炼铁的主要原理之一是赤铁矿。它的主要成分在一定条件下有下列反应:
 。在反应形成的固体混合物(
。在反应形成的固体混合物( 、
、 )中,元素铁和氧的质量比用
)中,元素铁和氧的质量比用 表示。
表示。(9)根据上述反应,固体质量每减轻
 ,将产生
,将产生
(10)上述反应形成的固体混和物中,
 不可能是_______。
不可能是_______。| A.21∶9 | B.21∶7.5 | C.21∶5 | D.21∶8 |
 也是铁重要的氧化物之一,其在高温下与金属铝反应,也能获得单质铁,写出相关的化学反应方程式
也是铁重要的氧化物之一,其在高温下与金属铝反应,也能获得单质铁,写出相关的化学反应方程式
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】下表是元素周期表一部分,列出了十种元素在周期表中的位置:
请回答下列问题:
(1)在上述元素中,非金属性最强的是________ (填元素名称),原子半径最大的是_____ (填元素符号),⑧与⑩两者核电荷数之差是_____________ 。
(2)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是_______________ (填物质化学式)。
(3)⑤和⑦可以形成一种温室气体,用电子式表示其形成过程____________________________ 。
(4)表中元素①和⑦可以形成一种淡黄色物质X,写出X的电子式:___________ ,该物质所含化学键类型为__________________ ,写出X与水反应的离子方程式_____________________ 0.1mol X与水反应转移电子数为 _______________ 。
(5)表中元素⑥和⑧可形成一种相对分子量为66的共价化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的结构式为________________________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 3 | ① | ③ | ④ | ⑨ | ||||
| 4 | ② | ⑩ |
(1)在上述元素中,非金属性最强的是
(2)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是
(3)⑤和⑦可以形成一种温室气体,用电子式表示其形成过程
(4)表中元素①和⑦可以形成一种淡黄色物质X,写出X的电子式:
(5)表中元素⑥和⑧可形成一种相对分子量为66的共价化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的结构式为
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】0.15mol某金属单质与足量的稀硫酸充分作用后,在标准状况下生成5.04L氢气和25.65g该金属的硫酸盐,若该金属原子核内的质子数比中子数少1个,试通过计算推导出该元素的原子序数___________ ,并指出其在周期表中的位置______________ 。
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】五种短周期主族元素W、M、X、X、Z原子序数依次增大,请结合表中信息回答下列问题:
(1)M元素在周期表中的位置为____________ 。
(2)M、X、Z元素所对应简单离子半径由大到小的顺序为__________ (用离子符号表示)。
(3)W最高价含氧酸与其气态氢化物发生化合反应生成的物质中含有的化学键类型为_____ 。
(4)下列可作为比较M和Z的非金属性强弱的依据是_______ (填序号)。
A.单质与H2反应的难易程度 B.氢化物的稳定性
C.最高价氧化物的水化物酸性强弱 D.将M的单质通入Z的钠盐溶液观察是否有Z逸出
(5)常温下,4.6gX单质在空中燃烧,再恢复到常温,放出QkJ能量,该反应的热化学方程式为_______________ 。
(6)W能形成多种氢化物,其中-种氢化物可作为火箭燃料,该物质中W与氢元素的质量比为7:1,写出该氢化物的电子式___________ 。该氢化物和O2在碱性条件下可形成燃料电池,产生两种无毒物质,写出其负极的电极反应式____________ 。
(7)Y元素和W元素形成的化合物YW一种新型无机材料,可与过量烧碱溶液反应产生使湿润的红色石蕊试纸变蓝的气体,写出有关的化学方程式___________________ 。
| 元素 | W | M | X | Y | Z |
| 结构或性质 | 最高价含氧酸与其气态氢化物能发生化合反应 | 氢化物的水溶液能刻蚀玻璃 | 焰色反应呈火焰黄色 | 同周期主族元素形成的简单离子中,其离子半径最小 | 最高正价与最低负价代数和为6 |
(1)M元素在周期表中的位置为
(2)M、X、Z元素所对应简单离子半径由大到小的顺序为
(3)W最高价含氧酸与其气态氢化物发生化合反应生成的物质中含有的化学键类型为
(4)下列可作为比较M和Z的非金属性强弱的依据是
A.单质与H2反应的难易程度 B.氢化物的稳定性
C.最高价氧化物的水化物酸性强弱 D.将M的单质通入Z的钠盐溶液观察是否有Z逸出
(5)常温下,4.6gX单质在空中燃烧,再恢复到常温,放出QkJ能量,该反应的热化学方程式为
(6)W能形成多种氢化物,其中-种氢化物可作为火箭燃料,该物质中W与氢元素的质量比为7:1,写出该氢化物的电子式
(7)Y元素和W元素形成的化合物YW一种新型无机材料,可与过量烧碱溶液反应产生使湿润的红色石蕊试纸变蓝的气体,写出有关的化学方程式
您最近半年使用:0次