由三种常见元素组成的化合物A,按如图流程进行实验。气体B、C、D均无色、无臭,B、D是纯净物;浓硫酸增重3.60g,碱石灰增重17.60g;溶液F焰色反应呈黄色。

请回答:
(1)组成A的非金属元素是___ ,气体B的结构简式___ 。
(2)固体A与足量水反应的化学方程式是___ 。
(3)一定条件下,气体D可能和FeO发生氧化还原反应,试写出一个可能的化学方程___ 。

请回答:
(1)组成A的非金属元素是
(2)固体A与足量水反应的化学方程式是
(3)一定条件下,气体D可能和FeO发生氧化还原反应,试写出一个可能的化学方程
更新时间:2020-08-18 14:53:30
|
相似题推荐
【推荐1】化学研究源于实验与理论的结合,得益于科学的推断与探究。
(1)一个体重 的健康人含铁
的健康人含铁 ,这
,这 铁在人体中以
铁在人体中以 和
和 的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。
的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。
①服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收,以下为常见铁元素的几种微粒,其中既有氧化性又有还原性的是___________ 。
A. B.
B. C.
C.
②工业盐的主要成分是 ,曾多次发生过因误食
,曾多次发生过因误食 而中毒的事件,其原因是将人体内的
而中毒的事件,其原因是将人体内的 转化为
转化为 而失去了与
而失去了与 结合的能力,这说明
结合的能力,这说明 具有
具有___________ 性。
③工业盐中毒后,可服用维生素C来缓解中毒症状,这说明维生素C具有___________ 性。
(2)常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性铁粉。脱氧中的一步主要反应为: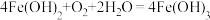 ,该脱氧反应中还原剂是
,该脱氧反应中还原剂是___________ 。
(3)某化学兴趣小组用食品脱氧剂( 铁粉、
铁粉、 活性炭、
活性炭、 氯化钠)进行如图两个实验。
氯化钠)进行如图两个实验。
实验Ⅰ:

请回答:
①溶液丙中一定含有的金属阳离子是___________ (写离子符号)。
②检验溶液丙中 的方案是
的方案是___________ 。
③实验Ⅱ:将乙烘干后进行如图实验,物质之间的转化关系如图(部分产物路法)
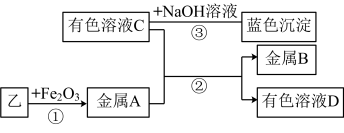
写出反应②的离子方程式___________ ,若反应消耗 金属A,转移电子的数目为
金属A,转移电子的数目为___________ 。
(1)一个体重
 的健康人含铁
的健康人含铁 ,这
,这 铁在人体中以
铁在人体中以 和
和 的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。
的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。①服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收,以下为常见铁元素的几种微粒,其中既有氧化性又有还原性的是
A.
 B.
B. C.
C.
②工业盐的主要成分是
 ,曾多次发生过因误食
,曾多次发生过因误食 而中毒的事件,其原因是将人体内的
而中毒的事件,其原因是将人体内的 转化为
转化为 而失去了与
而失去了与 结合的能力,这说明
结合的能力,这说明 具有
具有③工业盐中毒后,可服用维生素C来缓解中毒症状,这说明维生素C具有
(2)常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性铁粉。脱氧中的一步主要反应为:
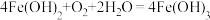 ,该脱氧反应中还原剂是
,该脱氧反应中还原剂是(3)某化学兴趣小组用食品脱氧剂(
 铁粉、
铁粉、 活性炭、
活性炭、 氯化钠)进行如图两个实验。
氯化钠)进行如图两个实验。实验Ⅰ:

请回答:
①溶液丙中一定含有的金属阳离子是
②检验溶液丙中
 的方案是
的方案是③实验Ⅱ:将乙烘干后进行如图实验,物质之间的转化关系如图(部分产物路法)

写出反应②的离子方程式
 金属A,转移电子的数目为
金属A,转移电子的数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)钠与氧气的反应会因条件不同而导致现象不同,产物不同,反应的实质也不同。据此回答下列问题:
①常温下,在空气中切开金属钠,钠的断面由银白色逐渐变暗而失去金属光泽,请用化学方程式解释这种现象产生的原因:__________________ 。
②钠在空气中受热所发生反应的化学方程式是__________________ 。
③将4.6克钠投入足量水中,标况下生成气体的体积是__________ 。
(2)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。
①用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为____________ 。
②如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为___________________________________ 。
③实验室制备Al(OH)3的常用方法是向Al2(SO4)3溶液中逐滴滴加氨水至过量,请写出对应的化学方程式:___________________________________ 。
(3)铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列问题。
①中国古代四大发明之一的指南针是由天然磁石制成的,其主要成分是_______ 。
②写出磁石的主要成分和盐酸反应的离子方程式______________ 。
①常温下,在空气中切开金属钠,钠的断面由银白色逐渐变暗而失去金属光泽,请用化学方程式解释这种现象产生的原因:
②钠在空气中受热所发生反应的化学方程式是
③将4.6克钠投入足量水中,标况下生成气体的体积是
(2)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。
①用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为
②如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为
③实验室制备Al(OH)3的常用方法是向Al2(SO4)3溶液中逐滴滴加氨水至过量,请写出对应的化学方程式:
(3)铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列问题。
①中国古代四大发明之一的指南针是由天然磁石制成的,其主要成分是
②写出磁石的主要成分和盐酸反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】“探险队员”——盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫里有许多“吃人的野兽”(既能与盐酸反应的物质),盐酸必须避开它们,否则就无法通过。
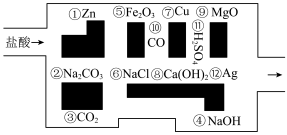
(1)请你帮助它走出迷宫:___________ 。(请用图中物质前的序号连接起来表示所走的路线)。
(2)在能“吃掉”盐酸的化学反应中,属于酸碱中和的反应有___________ 个,其中能“吃掉”盐酸的盐是___________ ,写出该反应的化学方程式:___________ 。
(3)在不能与盐酸反应的物质中,属于氧化物的是___________ (填序号,下同),属于单质的是___________ 。

(1)请你帮助它走出迷宫:
(2)在能“吃掉”盐酸的化学反应中,属于酸碱中和的反应有
(3)在不能与盐酸反应的物质中,属于氧化物的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】按题给要求填空
(1)按官能团的不同,可将有机物分为:A.烷烃 B.烯烃 C.炔烃 D.醚 E.酚 F.醛 G.羧酸 H.苯的同系物 I.酯 J.卤代烃 K.醇等,请指出下列有机物的种类(填写字母)。
①CH3CH2CH2CHO___________ ; ②
___________ ; ③
___________ ;④
___________ ;⑤
___________ ; ⑥
___________ 。
(2)分子式为C6H12的某烃的所有碳原子都在同一平面上,则该烃的结构简式为___________ ,若分子式为C4H6的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为___________ 。
(1)按官能团的不同,可将有机物分为:A.烷烃 B.烯烃 C.炔烃 D.醚 E.酚 F.醛 G.羧酸 H.苯的同系物 I.酯 J.卤代烃 K.醇等,请指出下列有机物的种类(填写字母)。
①CH3CH2CH2CHO





(2)分子式为C6H12的某烃的所有碳原子都在同一平面上,则该烃的结构简式为
您最近一年使用:0次
【推荐2】石油是工业的血液,与我们的生产、生活息息相关。完成下列填空:
(1)由重油制得汽油的方法是___ 。
(2)乙烯是重要的石油化工产品。与乙烯互为同系物的是___ 。(选填编号)
A.CH3CH=CH2 B.CH2=CHCH=CH2
C.CH≡CH D.CH3CH3
(3)聚乙烯安全无毒,可用于制食品包装袋。聚乙烯的结构简式为___ 。
(4)聚氯乙烯用途广泛,其单体的结构简式为___ 。请写出由乙炔制取聚氯乙烯的化学方程式___ 。乙炔还可聚合得到另一种高分子化合物——聚乙炔,聚乙炔___ 导电(选填“能”或“不能”)。
(5)乙炔在不同的催化条件下加氢可得到不同的产物。请写出乙炔的电子式:___ 。
下列物质与乙炔加氢得到的某种产物互为同系物的是___ 多(选填编号)。
A.C2H4 B.C3H8 C.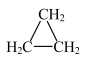 D.CH2=CHCH3
D.CH2=CHCH3
(6)乙炔能使溴水褪色、说明乙炔能发生___ 反应(填反应类型);乙炔能使酸性高锰酸钾溶液褪色,说明乙炔容易被___ 。
(7)乙炔在一定条件下三聚得到CH2=CH—C≡C—CH=CH2,写出与该三聚物具有相同化学式且不易发生加成反应的物质的结构简式___ 。该物质的同系物中苯环上一氯代物只有一种的物质的结构简式为___ (举一例):。
(1)由重油制得汽油的方法是
(2)乙烯是重要的石油化工产品。与乙烯互为同系物的是
A.CH3CH=CH2 B.CH2=CHCH=CH2
C.CH≡CH D.CH3CH3
(3)聚乙烯安全无毒,可用于制食品包装袋。聚乙烯的结构简式为
(4)聚氯乙烯用途广泛,其单体的结构简式为
(5)乙炔在不同的催化条件下加氢可得到不同的产物。请写出乙炔的电子式:
下列物质与乙炔加氢得到的某种产物互为同系物的是
A.C2H4 B.C3H8 C.
 D.CH2=CHCH3
D.CH2=CHCH3(6)乙炔能使溴水褪色、说明乙炔能发生
(7)乙炔在一定条件下三聚得到CH2=CH—C≡C—CH=CH2,写出与该三聚物具有相同化学式且不易发生加成反应的物质的结构简式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求填空:
(1)羟基的电子式_______ 。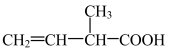 含氧官能团的名称是
含氧官能团的名称是_______ 。
(2)顺-2-丁烯的结构简式为_______ 。
(3)用系统命名法命名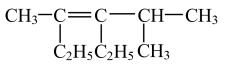
_______ ;
(4)写出由甲苯制备 TNT 方程式_______ ;
(5)分子式为 C3H7OCl,能与钠反应产生氢气的有机物共有(不含立体异构)_______ 种
(6)由乙烯和乙醇蒸气组成的混和气体中,若碳元素的质量百分含量为 60%,则氧元素的质量百分含量为_______ (保留三位有效数字)
(7)两种气态烃组成的混合气体 0.1 mol,完全燃烧得到 7.04 g CO2和 3.6 g H2O,下列说法错误的是
(8)由碘乙烷制取乙二醇(HOCH2CH2OH),依次发生的反应类型是
(1)羟基的电子式
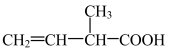 含氧官能团的名称是
含氧官能团的名称是(2)顺-2-丁烯的结构简式为
(3)用系统命名法命名
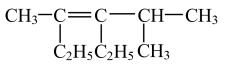
(4)写出由甲苯制备 TNT 方程式
(5)分子式为 C3H7OCl,能与钠反应产生氢气的有机物共有(不含立体异构)
(6)由乙烯和乙醇蒸气组成的混和气体中,若碳元素的质量百分含量为 60%,则氧元素的质量百分含量为
(7)两种气态烃组成的混合气体 0.1 mol,完全燃烧得到 7.04 g CO2和 3.6 g H2O,下列说法错误的是
| A.一定有 C2H4 | B.一定有 CH4 | C.一定没有 C2H6 | D.可能是 CH4和 C2H4 |
| A.取代-加成- 水解 | B.消去- 加成 -取代 | C.水解- 消去- 加成 | D.消去- 水解- 取代 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有A、B、C、D四种烃,其球棍模型如图所示, 代表H原子,
代表H原子, 代表C原子,请回答下列问题:
代表C原子,请回答下列问题:

(1)写出D的结构简式:_______ ;为了鉴别C和D,可选用,_______ (填试剂名称)。
(2)写出一个A与Cl2反应的化学方程式_______ 。
(3)工业上用B与水反应可制得乙醇。
①上述反应的化学方程式为_______ ,反应类型为_______ 。
②利用下图装置(部分夹持装置略)进行乙醇的催化氧化实验来制取乙醛。甲装置常常浸在70~80°C的水浴中,目的是_______ ;写出乙醇催化氧化制取乙醛的化学反应方程式_______ 。

(4)上述四种烃中在120°C、1.01×105Pa条件下,与足量的O2混合点燃,完全燃烧前后气体体积没有变化的烃是_______ (填分子式)。
 代表H原子,
代表H原子, 代表C原子,请回答下列问题:
代表C原子,请回答下列问题:
(1)写出D的结构简式:
(2)写出一个A与Cl2反应的化学方程式
(3)工业上用B与水反应可制得乙醇。
①上述反应的化学方程式为
②利用下图装置(部分夹持装置略)进行乙醇的催化氧化实验来制取乙醛。甲装置常常浸在70~80°C的水浴中,目的是

(4)上述四种烃中在120°C、1.01×105Pa条件下,与足量的O2混合点燃,完全燃烧前后气体体积没有变化的烃是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】I.分别取一定质量的甲烷、乙炔、苯、己烯、甲苯,完全燃烧后都生成m molCO2和nmolH2O。
(1)若m=n,该烃是____ ;
(2)若m=2n,该烃是____ ;
(3)若4m=7n,该烃是____ ;
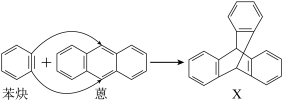
II.蒽(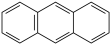 )与苯炔(
)与苯炔( )反应生成化合物X(立体对称图形),如图所示:
)反应生成化合物X(立体对称图形),如图所示:
(1)蒽与X都属于(填字母)________
a.环烃 b.苯的同系物 c.不饱和烃
(2)苯炔不具有的性质是(填字母)_______
a.能溶于水 b.能发生氧化反应 c.能发生加成反应 d.常温常压下为气体
(3)下列物质中,能发生加成反应,也能发生取代反应,同时能使溴水因加成反应而褪色,还能使酸性高锰酸钾溶液褪色的是____
A.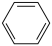 B.C6H14
B.C6H14
C.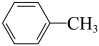 D.
D.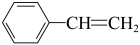
(1)若m=n,该烃是
(2)若m=2n,该烃是
(3)若4m=7n,该烃是
II.蒽(
 )与苯炔(
)与苯炔( )反应生成化合物X(立体对称图形),如图所示:
)反应生成化合物X(立体对称图形),如图所示:
(1)蒽与X都属于(填字母)
a.环烃 b.苯的同系物 c.不饱和烃
(2)苯炔不具有的性质是(填字母)
a.能溶于水 b.能发生氧化反应 c.能发生加成反应 d.常温常压下为气体
(3)下列物质中,能发生加成反应,也能发生取代反应,同时能使溴水因加成反应而褪色,还能使酸性高锰酸钾溶液褪色的是
A.
 B.C6H14
B.C6H14C.
 D.
D.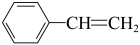
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】Ⅰ.食品添加剂能改善食物色香味、延长保质期、调整营养结构。我国对食品添加剂的品种、适用范围、最大用量及残留量都制定了严格的标准。
(1)下列关天食品添加剂的说法正确的是________ 。
A制作豆腐时,加入石膏做凝固剂
B.制作糕点时,加入小苏打做防腐剂
C.生产加碘食盐时,加入碘单质作补碘剂
Ⅱ.SO2是葡萄、荔枝等水果储存时常用的保鲜剂,能降低水果腐烂率,提高维生素C留存率。
(2)硫原子的结构示意图为________ 。
(3)与SO2所含化学键类型相同的是________。
(4)硫与硅为同一周期元素,通过下列事实能比较两者非金属性强弱的是________(双选)。
(5)保鲜时若SO2不慎用量过大,会使水果表面明显褪色,上述现象说明SO2________ 。
A.易溶于水B.是酸性氧化物C.具有漂白作用
Ⅲ.《食品安全国家标准·食品添加剂使用标准》(GB 2760-2014)中规定,水果中SO2残留量不得高于0.05g/kg。某种测定水果中残留SO2的方法所涉及的主要反应有:SO2+ H2O2=H2SO4、 +Ba2+=BaSO4↓。
+Ba2+=BaSO4↓。
已知:ω(SO2残留量) =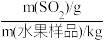 。
。
(6)称取某水果样品2 kg,经过一系列处理后,最终得到BaSO4,沉淀的质量为0.233 g。通过计算,判断该水果样品中SO2残留量是否超标______ (写出计算过程)。
(1)下列关天食品添加剂的说法正确的是
A制作豆腐时,加入石膏做凝固剂
B.制作糕点时,加入小苏打做防腐剂
C.生产加碘食盐时,加入碘单质作补碘剂
Ⅱ.SO2是葡萄、荔枝等水果储存时常用的保鲜剂,能降低水果腐烂率,提高维生素C留存率。
(2)硫原子的结构示意图为
(3)与SO2所含化学键类型相同的是________。
| A.NH4Cl | B.CaCl2 | C.AlCl3 | D.NaOH |
| A.热稳定性:H2S>SiH4 | B.溶解度:SO2> SiO2 |
| C.单质的熔点:Si > S | D.酸性:H2SO4> H2SiO3 |
A.易溶于水B.是酸性氧化物C.具有漂白作用
Ⅲ.《食品安全国家标准·食品添加剂使用标准》(GB 2760-2014)中规定,水果中SO2残留量不得高于0.05g/kg。某种测定水果中残留SO2的方法所涉及的主要反应有:SO2+ H2O2=H2SO4、
 +Ba2+=BaSO4↓。
+Ba2+=BaSO4↓。已知:ω(SO2残留量) =
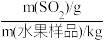 。
。(6)称取某水果样品2 kg,经过一系列处理后,最终得到BaSO4,沉淀的质量为0.233 g。通过计算,判断该水果样品中SO2残留量是否超标
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化合物X是一种常见的脱叶剂,某兴趣小组对X开展探究实验。
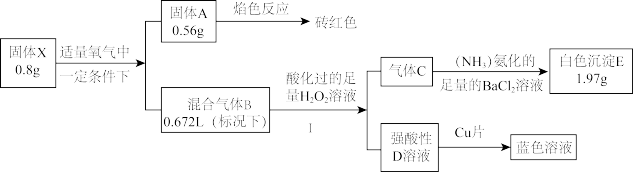
其中:X是一种正盐,由3种常见元素组成;无色混合气体B只含有两种成分,遇空气变红棕色。
请回答:
(1)组成X的3种元素是___ (填元素符号),X的化学式是___ 。
(2)步骤Ⅰ,发生反应的离子方程式是___ 。
(3)在潮湿环境中X与水(物质的量1:1)水解,产物中含有一种酸式盐,该反应的化学反应方程式___ 。
(4)强酸性溶液D也可以溶解铁,请设计实验证明反应后溶液中铁元素的存在形式___ 。

其中:X是一种正盐,由3种常见元素组成;无色混合气体B只含有两种成分,遇空气变红棕色。
请回答:
(1)组成X的3种元素是
(2)步骤Ⅰ,发生反应的离子方程式是
(3)在潮湿环境中X与水(物质的量1:1)水解,产物中含有一种酸式盐,该反应的化学反应方程式
(4)强酸性溶液D也可以溶解铁,请设计实验证明反应后溶液中铁元素的存在形式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某溶液中可能含有下列6种离子中的某几种:Cl−、SO 、NH
、NH 、CO
、CO 、K+、Na+。为确认溶液组成进行如下实验:
、K+、Na+。为确认溶液组成进行如下实验:
①200 mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30 g,向沉淀中加入过量的盐酸,有2.33 g沉淀不溶。
②向①的滤液中加入足量的NaOH溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12 L(已换算成标准状况,假定产生的气体全部逸出)。
(1)溶液一定存在的离子有____ ,可能存在的离子有______ ;
(2)原溶液中c(CO )为
)为____ ,c(NH )
)____ c(SO ) (填“>、<或=”);
) (填“>、<或=”);
(3)如果上述6种离子都存在,则c(Cl−)__ c(SO ) (填“>、<或=”)。
) (填“>、<或=”)。
 、NH
、NH 、CO
、CO 、K+、Na+。为确认溶液组成进行如下实验:
、K+、Na+。为确认溶液组成进行如下实验:①200 mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30 g,向沉淀中加入过量的盐酸,有2.33 g沉淀不溶。
②向①的滤液中加入足量的NaOH溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12 L(已换算成标准状况,假定产生的气体全部逸出)。
(1)溶液一定存在的离子有
(2)原溶液中c(CO
 )为
)为 )
) ) (填“>、<或=”);
) (填“>、<或=”);(3)如果上述6种离子都存在,则c(Cl−)
 ) (填“>、<或=”)。
) (填“>、<或=”)。
您最近一年使用:0次

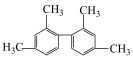 中,在同一平面上的碳原子至少有
中,在同一平面上的碳原子至少有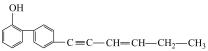 中共线的碳原子最多有
中共线的碳原子最多有

