砷(As)广泛分布于自然界,其原子结构示意图是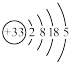
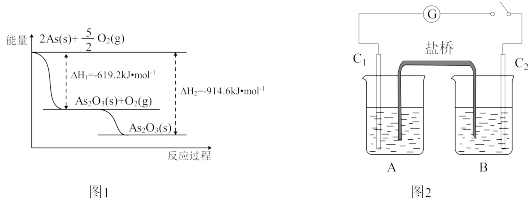
(1)砷位于元素周期表中________ 族,其气态氢化物的稳定性比NH3________ (填“强”或“弱”).
(2)砷的常见氧化物有As2O3和As2O5,其中As2O5热稳定性差.根据图1写出As2O5分解为As2O3的热化学方程式:________
(3)砷酸盐可发生如下反应:AsO +2I﹣+2H+⇌AsO
+2I﹣+2H+⇌AsO +I2+H2O.图2装置中,C1、C2是石墨电极.A中盛有棕色的KI和I2的混合溶液,B中盛有无色的Na3AsO4和Na3AsO3的混合溶液,当连接开关K,并向B中滴加浓盐酸时发现灵敏电流计G的指针向右偏转.此时C2上发生的电极反应是
+I2+H2O.图2装置中,C1、C2是石墨电极.A中盛有棕色的KI和I2的混合溶液,B中盛有无色的Na3AsO4和Na3AsO3的混合溶液,当连接开关K,并向B中滴加浓盐酸时发现灵敏电流计G的指针向右偏转.此时C2上发生的电极反应是 ________
(4)利用(3)中反应可测定含As2O3和As2O5的试样中的各组分含量(所含杂质对测定无影响),过程如下:
①将试样mg溶于NaOH溶液,得到含AsO 和AsO
和AsO 的混合溶液.As2O5与NaOH溶液反应的离子方程式是
的混合溶液.As2O5与NaOH溶液反应的离子方程式是________ .
②上述混合液用0.02500mol•L﹣1的I2溶液滴定,用________ 做指示剂,滴定至________ ,停止滴定,记录数据.重复滴定2次,平均消耗I2溶液20.00mL.则试样中As2O3的质量分数是________
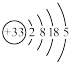
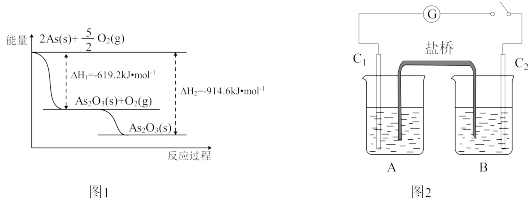
(1)砷位于元素周期表中
(2)砷的常见氧化物有As2O3和As2O5,其中As2O5热稳定性差.根据图1写出As2O5分解为As2O3的热化学方程式:
(3)砷酸盐可发生如下反应:AsO
 +2I﹣+2H+⇌AsO
+2I﹣+2H+⇌AsO +I2+H2O.图2装置中,C1、C2是石墨电极.A中盛有棕色的KI和I2的混合溶液,B中盛有无色的Na3AsO4和Na3AsO3的混合溶液,当连接开关K,并向B中滴加浓盐酸时发现灵敏电流计G的指针向右偏转.此时C2上发生的电极反应是
+I2+H2O.图2装置中,C1、C2是石墨电极.A中盛有棕色的KI和I2的混合溶液,B中盛有无色的Na3AsO4和Na3AsO3的混合溶液,当连接开关K,并向B中滴加浓盐酸时发现灵敏电流计G的指针向右偏转.此时C2上发生的电极反应是 (4)利用(3)中反应可测定含As2O3和As2O5的试样中的各组分含量(所含杂质对测定无影响),过程如下:
①将试样mg溶于NaOH溶液,得到含AsO
 和AsO
和AsO 的混合溶液.As2O5与NaOH溶液反应的离子方程式是
的混合溶液.As2O5与NaOH溶液反应的离子方程式是②上述混合液用0.02500mol•L﹣1的I2溶液滴定,用
更新时间:2020-08-28 09:35:33
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】1909年,化学家哈伯用N2和H2在高温高压条件下首次合成了氨气,反应原理为N2(g)+3H2(g) 2NH3(g),该反应的能量变化如图1所示(a、b均大于零),回答下列问题:
2NH3(g),该反应的能量变化如图1所示(a、b均大于零),回答下列问题:

(1)根据图1写出生成2molNH3时的热化学方程式:___________ 。
(2)在500°C、30MPa下,断裂1 molH—H键、1molN—H键、1 molN≡N键需要吸收的能量分别为436 kJ、391kJ、946kJ。
①每消耗0.5molN2该反应放出的热量为___________ 。
②向某一密闭容器中充入1.5molH2(g)和0.5molN2(g),在催化剂条件下进行上述反应,此时断裂的H—H键吸收的热量___________ (填“>”,“<”或“=”)436×1.5=654(kJ)。
(3)一种用电化学法合成氨的原理装置如图2所示:

①电极B的名称是___________ (填“阴极”或“阳极”)。
②图2中阳极的电极反应式为___________ 。
③若图2中支持电解质改为质子导体陶瓷膜,则阴极的电极反应式为___________
 2NH3(g),该反应的能量变化如图1所示(a、b均大于零),回答下列问题:
2NH3(g),该反应的能量变化如图1所示(a、b均大于零),回答下列问题:
(1)根据图1写出生成2molNH3时的热化学方程式:
(2)在500°C、30MPa下,断裂1 molH—H键、1molN—H键、1 molN≡N键需要吸收的能量分别为436 kJ、391kJ、946kJ。
①每消耗0.5molN2该反应放出的热量为
②向某一密闭容器中充入1.5molH2(g)和0.5molN2(g),在催化剂条件下进行上述反应,此时断裂的H—H键吸收的热量
(3)一种用电化学法合成氨的原理装置如图2所示:

①电极B的名称是
②图2中阳极的电极反应式为
③若图2中支持电解质改为质子导体陶瓷膜,则阴极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】我国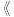 车用燃料甲醇国家标准
车用燃料甲醇国家标准 的实施拉开了车用燃料低碳革命的大幕,一些省市正在陆续试点与推广使用甲醇汽油。甲醇可通过
的实施拉开了车用燃料低碳革命的大幕,一些省市正在陆续试点与推广使用甲醇汽油。甲醇可通过 和
和 在一定条件下发生如下反应制得:
在一定条件下发生如下反应制得: 图Ⅰ、图Ⅱ是关于该反应进行情况的图示。
图Ⅰ、图Ⅱ是关于该反应进行情况的图示。
请根据图示回答下列问题:
(1)图 是反应时
是反应时 和
和 的浓度随时间的变化情况,从反应开始到平衡,用
的浓度随时间的变化情况,从反应开始到平衡,用 浓度变化表示平均反应速率v(CO)=
浓度变化表示平均反应速率v(CO)=___________ 。
(2)图Ⅱ表示该反应进行过程中能量的变化,曲线 表示不使用催化剂时反应的能量变化,在图Ⅱ中画出使用催化剂后的能量变化曲线b
表示不使用催化剂时反应的能量变化,在图Ⅱ中画出使用催化剂后的能量变化曲线b________________
(3)写出该反应的热化学方程式___________ 。
(4)该反应的平衡常数 的表达式为
的表达式为___________ ;当温度升高时,该平衡常数 将
将___________ (填“增大”、“减小”或“不变”)
(5)恒容条件下,下列措施中能使 增大的有___________。
增大的有___________。
(6)若在一体积可变的密闭容器中充入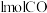 、
、 和
和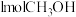 ,达到平衡时测得混合气体的密度是同温同压下起始的
,达到平衡时测得混合气体的密度是同温同压下起始的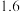 倍,则该反应向
倍,则该反应向___________ (填“正”、“逆”)反应方向移动,理由是___________ 。
 车用燃料甲醇国家标准
车用燃料甲醇国家标准 的实施拉开了车用燃料低碳革命的大幕,一些省市正在陆续试点与推广使用甲醇汽油。甲醇可通过
的实施拉开了车用燃料低碳革命的大幕,一些省市正在陆续试点与推广使用甲醇汽油。甲醇可通过 和
和 在一定条件下发生如下反应制得:
在一定条件下发生如下反应制得: 图Ⅰ、图Ⅱ是关于该反应进行情况的图示。
图Ⅰ、图Ⅱ是关于该反应进行情况的图示。
请根据图示回答下列问题:
(1)图
 是反应时
是反应时 和
和 的浓度随时间的变化情况,从反应开始到平衡,用
的浓度随时间的变化情况,从反应开始到平衡,用 浓度变化表示平均反应速率v(CO)=
浓度变化表示平均反应速率v(CO)=(2)图Ⅱ表示该反应进行过程中能量的变化,曲线
 表示不使用催化剂时反应的能量变化,在图Ⅱ中画出使用催化剂后的能量变化曲线b
表示不使用催化剂时反应的能量变化,在图Ⅱ中画出使用催化剂后的能量变化曲线b(3)写出该反应的热化学方程式
(4)该反应的平衡常数
 的表达式为
的表达式为 将
将(5)恒容条件下,下列措施中能使
 增大的有___________。
增大的有___________。| A.升高温度 | B.充入 气 气 | C.再充入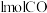 和 和 | D.使用催化剂 |
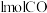 、
、 和
和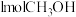 ,达到平衡时测得混合气体的密度是同温同压下起始的
,达到平衡时测得混合气体的密度是同温同压下起始的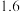 倍,则该反应向
倍,则该反应向
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
某用活性炭还原处理氮氧化物,有关反应为C(s)+2NO(g) N2(g)+CO2(g)。
N2(g)+CO2(g)。
(1)写出上述反应的平衡常数表达式___________ 。
(2)在2L恒容密闭容器中加入足量C与NO发生反应,所得数据如表,回答下列问题。
①结合表中数据,判断该反应的ΔH___________ 0(填“>”或“<”),理由是___________ (请从K变化角度分析)。
②判断该反应达到平衡的依据是___________ (填字母)。
A.容器内气体密度恒定B.容器内各气体浓度恒定
C.容器内压强恒定D.2v正(NO)=v逆(N2)
(3)合成氨反应常使用铁触媒提高反应速率。如图为有、无铁触媒时,反应的能量变化示意图。写出该反应的热化学方程式:___________ 。
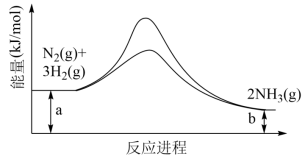
某用活性炭还原处理氮氧化物,有关反应为C(s)+2NO(g)
 N2(g)+CO2(g)。
N2(g)+CO2(g)。(1)写出上述反应的平衡常数表达式
(2)在2L恒容密闭容器中加入足量C与NO发生反应,所得数据如表,回答下列问题。
| 实验编号 | 温度/℃ | 起始时NO的物质的量/mol | 平衡时N2的物质的量/mol |
| 1 | 700 | 0.40 | 0.09 |
| 2 | 800 | 0.24 | 0.08 |
②判断该反应达到平衡的依据是
A.容器内气体密度恒定B.容器内各气体浓度恒定
C.容器内压强恒定D.2v正(NO)=v逆(N2)
(3)合成氨反应常使用铁触媒提高反应速率。如图为有、无铁触媒时,反应的能量变化示意图。写出该反应的热化学方程式:

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】短周期元素X、Y、Z、W的原子序数依次增大,且四种元素分别位于不同的主族,它们的单质常温下均呈气态。X、Y、W处于不同周期,且在一定条件下其单质能发生反应:X2+Y2→甲,X2+W2→乙,已知,甲、乙常温下均为气态,且两者在空气中相遇时可化合成丙。试回答下列问题:
⑴ Y和Z对应的氢化物比较稳定的是:_______________ 。(填化学式)
⑵ 化合物丙属于_____________ 晶体(填晶体类型),其水溶液显酸性,用离子方程式 表示其原因:_________________________________________ 。
⑶ X、Z可组成四原子化合物丁,丁中所含的化学键类型为:____________ 键,请说出化合物丁的一种常见用途:___________________________________ ;
⑷ X、Y组成的液态化合物Y2X4 16 g与足量丁反应生成Y2和液态水,放出QkJ的热量,写出该反应的热化学方程式 :______________________________ ;
Y2X4还可以和Z2构成清洁高效的燃料电池,若电解质溶液为NaOH溶液,则负极 的电极反应式为:________________________________________ 。
⑸ 一定条件下,取 3.4 g甲气体 置于1 L恒容的容器中,4分钟后,容器内的压强变为原来的1.2倍,且不再变化,该反应中甲气体的转化率 为:__________ 。
⑴ Y和Z对应的氢化物比较稳定的是:
⑵ 化合物丙属于
⑶ X、Z可组成四原子化合物丁,丁中所含的化学键类型为:
⑷ X、Y组成的液态化合物Y2X4 16 g与足量丁反应生成Y2和液态水,放出QkJ的热量,写出该反应的
Y2X4还可以和Z2构成清洁高效的燃料电池,若电解质溶液为NaOH溶液,则
⑸ 一定条件下,取 3.4 g
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】2020年9月22日,国家主席习近平在第75届联合国大会上宣布:中国二氧化碳排放力争2030年前达到峰值,2060年前实现“碳中和”。为达成这一目标,要尽量减少不可避免的碳排放。
(1)工业上,常用水蒸气通过炽热的焦炭制得水煤气(主要成分为CO和 ),其反应的化学方程式为
),其反应的化学方程式为 ,该反应的能量变化图像如图所示。
,该反应的能量变化图像如图所示。_______ 。
A.铝粉与氧化铁的反应
B.氯化铵与 的反应
的反应
C.锌片与稀硫酸的反应
D.钠与冷水的反应
②一定温度下,在2L的恒容密闭容器中,加入0.02molC(s)和0.01mol 发生反应:
发生反应: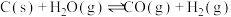 ,充分反应5min时,测得容器中CO的物质的量有0.008mol。以
,充分反应5min时,测得容器中CO的物质的量有0.008mol。以 表示的化学反应速率
表示的化学反应速率 为
为_______ 。
③我国科学家使用双功能催化剂(能吸附不同粒子)催化水煤气变换反应:
 反应放热。在低温下获得高产率。反应过程示意图如下图:
反应放热。在低温下获得高产率。反应过程示意图如下图:_______ 。
A.据图可知起始时的2个 分子最终都参与了反应
分子最终都参与了反应
B.过程Ⅰ、过程Ⅱ均为吸热过程,
C.过程Ⅲ只生成了极性共价键
D.使用催化剂缩小反应物和生成物的能量差
(2)以 为催化剂的光热化学循环分解
为催化剂的光热化学循环分解 反应为减少“碳排放”提供了一个新途径,该反应各分子化学键完全断裂时的能量变化如图所示:
反应为减少“碳排放”提供了一个新途径,该反应各分子化学键完全断裂时的能量变化如图所示: 完全分解生成CO(g)和
完全分解生成CO(g)和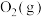 需要
需要_______ (填“吸收”或“放出”)_______ kJ的能量。
(3) 分解产生的CO和
分解产生的CO和 可以作为
可以作为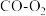 燃料电池的原料。下图为
燃料电池的原料。下图为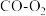 燃料电池的构造示意图,根据电子运动方向,可知氧气从
燃料电池的构造示意图,根据电子运动方向,可知氧气从_______ 口通入(填“a”或“b”);X极为电池的_______ (填“正”或“负”)极,电极反应为_______ , 向
向_______ 极移动(填“X”或“Y”);若两极共消耗气体3.36L(标准状况下),则通过导线的电子数为_______ 。
(1)工业上,常用水蒸气通过炽热的焦炭制得水煤气(主要成分为CO和
 ),其反应的化学方程式为
),其反应的化学方程式为 ,该反应的能量变化图像如图所示。
,该反应的能量变化图像如图所示。
A.铝粉与氧化铁的反应
B.氯化铵与
 的反应
的反应C.锌片与稀硫酸的反应
D.钠与冷水的反应
②一定温度下,在2L的恒容密闭容器中,加入0.02molC(s)和0.01mol
 发生反应:
发生反应: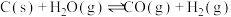 ,充分反应5min时,测得容器中CO的物质的量有0.008mol。以
,充分反应5min时,测得容器中CO的物质的量有0.008mol。以 表示的化学反应速率
表示的化学反应速率 为
为③我国科学家使用双功能催化剂(能吸附不同粒子)催化水煤气变换反应:
 反应放热。在低温下获得高产率。反应过程示意图如下图:
反应放热。在低温下获得高产率。反应过程示意图如下图:
A.据图可知起始时的2个
 分子最终都参与了反应
分子最终都参与了反应B.过程Ⅰ、过程Ⅱ均为吸热过程,
C.过程Ⅲ只生成了极性共价键
D.使用催化剂缩小反应物和生成物的能量差
(2)以
 为催化剂的光热化学循环分解
为催化剂的光热化学循环分解 反应为减少“碳排放”提供了一个新途径,该反应各分子化学键完全断裂时的能量变化如图所示:
反应为减少“碳排放”提供了一个新途径,该反应各分子化学键完全断裂时的能量变化如图所示:
 完全分解生成CO(g)和
完全分解生成CO(g)和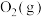 需要
需要(3)
 分解产生的CO和
分解产生的CO和 可以作为
可以作为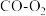 燃料电池的原料。下图为
燃料电池的原料。下图为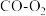 燃料电池的构造示意图,根据电子运动方向,可知氧气从
燃料电池的构造示意图,根据电子运动方向,可知氧气从 向
向
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】FeCl3可作印刷电路钢板腐蚀剂,反应的方程式为:2FeCl3+Cu=2FeCl2+CuCl2
(1)将上述反应设计成的原电池如图所示

请回答下列问题:
①电极X的材料是___________ ;电解质溶液Y是___________ 。
②X电极上发生的电极反应式为___________ 。
(2)腐蚀钢板后的废腐蚀液中,含有FeCl3、FeCl2、CuCl2等物质,用电解法可回收铜且得到FeCl2溶液,其工作原理如图所示,请回答下列问题:

①该电解槽阴极的反应式是___________
②阴离子交换膜中通过的离子主要是___________ ,FeCl3溶液从出口___________ (填写“A”或“B”)导出,FeCl2溶液从出口___________ (填写“A”或“B”)导出。
(1)将上述反应设计成的原电池如图所示

请回答下列问题:
①电极X的材料是
②X电极上发生的电极反应式为
(2)腐蚀钢板后的废腐蚀液中,含有FeCl3、FeCl2、CuCl2等物质,用电解法可回收铜且得到FeCl2溶液,其工作原理如图所示,请回答下列问题:

①该电解槽阴极的反应式是
②阴离子交换膜中通过的离子主要是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】完成下列问题。
(1)上表中的实线是元素周期表部分边界,请在表中用粗实线补全元素周期表边界_______ 。
(2)制冷剂是一种易被压缩、液化的气体,液化后在管内循环,蒸发时吸收热量,使环境温度降低,达到制冷目的。人们曾采用过乙醚、NH3、CH3Cl等作制冷剂,但它们不是有毒,就是易燃、于是科学家根据元素性质的递变规律来开发新的制冷剂。据现有知识,某些元素化合物的易燃性、毒性变化趋势如下:
①氢化物的易燃性:第二周期____ >____ >H2O>HF;第三周期SiH4>PH3>____ >____ 。
②化合物的毒性:PH3>NH3,H2S_____ H2O,CS2____ CO2,CCl4_____ CF4(选填>或=)。
(3)已知CCl4的沸点为76.8℃,CF4的沸点为-128℃,新制冷剂的沸点范围应介于其间。经过较长时间反复试验,一种新的制冷剂氟利昂CF2Cl2终于诞生了,其它类似的还可以是_______ 。
(4)然而,这种制冷剂造成了当今的某一环境问题是______ 。但求助于周期表中元素及其化合物的_____ 变化趋势来开发制冷剂的科学思维方法是值得借鉴的(填写字母)。
①毒性②沸点③易燃性④水溶性⑤颜色
a.①②③ b.②④⑤ c.②③④
(1)上表中的实线是元素周期表部分边界,请在表中用粗实线补全元素周期表边界
(2)制冷剂是一种易被压缩、液化的气体,液化后在管内循环,蒸发时吸收热量,使环境温度降低,达到制冷目的。人们曾采用过乙醚、NH3、CH3Cl等作制冷剂,但它们不是有毒,就是易燃、于是科学家根据元素性质的递变规律来开发新的制冷剂。据现有知识,某些元素化合物的易燃性、毒性变化趋势如下:
①氢化物的易燃性:第二周期
②化合物的毒性:PH3>NH3,H2S
(3)已知CCl4的沸点为76.8℃,CF4的沸点为-128℃,新制冷剂的沸点范围应介于其间。经过较长时间反复试验,一种新的制冷剂氟利昂CF2Cl2终于诞生了,其它类似的还可以是
(4)然而,这种制冷剂造成了当今的某一环境问题是
①毒性②沸点③易燃性④水溶性⑤颜色
a.①②③ b.②④⑤ c.②③④
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】表中列出了第三周期几种元素的部分性质:
请按要求回答下列问题:
(1)表中元素原子半径最大的是(写元素符号)___________ 。
(2)a、b、c三种元素形成的氢化物中,其稳定性由强到弱的顺序是(用化学式表示)___________ 。
(3)d、e最高价氧化物对应水化物相互反应的离子方程式为___________ 。
(4)某化学兴趣小组为探究元素性质的递变规律,设计了以下系列实验。
①甲同学为探究同主族元素金属性的递变规律,取绿豆粒大小的钠、钾分别放入到盛有水的烧杯(滴有几滴酚酞溶液)中,通过观察现象得出的结论是___________ 。
②乙同学利用现有药品: 溶液、
溶液、 固体、浓盐酸、
固体、浓盐酸、 ,设计如图装置探究第三周期部分元素非金属性的递变规律。M中所装药品为
,设计如图装置探究第三周期部分元素非金属性的递变规律。M中所装药品为___________ ,装置N中的实验现象为有淡黄色沉淀生成,离子方程式为___________ ,所得结论为___________ 。

| 元素编号 | a | b | c | d | e |
| 电负性 | 3.0 | 2.5 | 2.1 | 1.5 | 0.9 |
| 主要化合价 | -1,+7 | -2,+6 | -3,+5 | +3 | +1 |
(1)表中元素原子半径最大的是(写元素符号)
(2)a、b、c三种元素形成的氢化物中,其稳定性由强到弱的顺序是(用化学式表示)
(3)d、e最高价氧化物对应水化物相互反应的离子方程式为
(4)某化学兴趣小组为探究元素性质的递变规律,设计了以下系列实验。
①甲同学为探究同主族元素金属性的递变规律,取绿豆粒大小的钠、钾分别放入到盛有水的烧杯(滴有几滴酚酞溶液)中,通过观察现象得出的结论是
②乙同学利用现有药品:
 溶液、
溶液、 固体、浓盐酸、
固体、浓盐酸、 ,设计如图装置探究第三周期部分元素非金属性的递变规律。M中所装药品为
,设计如图装置探究第三周期部分元素非金属性的递变规律。M中所装药品为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】(1)A、B两元素,A的原子序数为x,A和B所在周期包含元素种类分别为m、n。如果A和B同在ⅠA族,当B在A的上一周期时,B的原子序数为____________ ;当B在A的下一周期时,B的原子序数为____________ 。如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为__________ ;当B在A的下一周期时,B的原子序数为___________ 。
(2) A、B两元素同周期,A位于ⅡA族,B位于ⅢA族,A的原子序数为x,B的原子序数为y,则y-x=_________ 或_________ 或_________ 。
(2) A、B两元素同周期,A位于ⅡA族,B位于ⅢA族,A的原子序数为x,B的原子序数为y,则y-x=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】二氧化氯(ClO2) 作为一种高效强氧化剂,已被联合国世界卫生组织(WHO)列为AI级安全消毒剂。某研究小组设计如图所示装置制备ClO2和NaClO2。已知: ClO2熔点一59℃、沸点11℃,常温下ClO2为黄绿色或橘黄色气体,ClO2浓度过高或受热易分解,甚至会爆炸。NaClO2高于60℃时分解生成NaClO3和NaCl。

(1)装置连接好后,加入药品前需进行的操作是____________________________________ 。
(2)使用恒压分液漏斗的目的是_________________ ;仪器B 的作用是_________________ 。
(3)A 中反应为2NaClO3+H2O2+H2SO4=2C1O2↑+O2↑+Na2SO4+2H2O。
C 中反应的化学方程式是_______________ , 冷水浴的目的是_________________________ 。
(4) 实验中持续通入空气能稀释生成的ClO2并将其排到C处。若空气的流速太慢可能造成的后果是_______________________________________ 。
(5)已知: ClO2被I-还原为ClO2-、Cl-的转化率与溶液pH 的关系如图所示。当pH≤2.0 时,ClO2-也能被I-完全还原为Cl-。反应生成的I2与Na2S2O3反应的方程式: 2Na2S2O3+ I2= Na2S4O6 + 2NaI。

用ClO2消毒的饮用水中含有ClO2、ClO2-。测定饮用水中ClO2、ClO2-的含量,分两步进行:
①用紫外分光光度法测得水样中ClO2的含量为amol/L。
②用滴定法测量ClO2-的含量。请完成相应的实验步骤:
步骤1: 准确量取VmL 上述水样加入锥形瓶中。
步骤2: 调节水样的pH________ 。
步骤3: 加入足量的KI 晶体,充分反应。
步骤4: 加入少量淀粉溶液,用cmol/L Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V1mL。
根据上述分析数据,测得该饮用水中ClO2-的浓度为____ mol/L( 用含字母的代数式表示)。

(1)装置连接好后,加入药品前需进行的操作是
(2)使用恒压分液漏斗的目的是
(3)A 中反应为2NaClO3+H2O2+H2SO4=2C1O2↑+O2↑+Na2SO4+2H2O。
C 中反应的化学方程式是
(4) 实验中持续通入空气能稀释生成的ClO2并将其排到C处。若空气的流速太慢可能造成的后果是
(5)已知: ClO2被I-还原为ClO2-、Cl-的转化率与溶液pH 的关系如图所示。当pH≤2.0 时,ClO2-也能被I-完全还原为Cl-。反应生成的I2与Na2S2O3反应的方程式: 2Na2S2O3+ I2= Na2S4O6 + 2NaI。

用ClO2消毒的饮用水中含有ClO2、ClO2-。测定饮用水中ClO2、ClO2-的含量,分两步进行:
①用紫外分光光度法测得水样中ClO2的含量为amol/L。
②用滴定法测量ClO2-的含量。请完成相应的实验步骤:
步骤1: 准确量取VmL 上述水样加入锥形瓶中。
步骤2: 调节水样的pH
步骤3: 加入足量的KI 晶体,充分反应。
步骤4: 加入少量淀粉溶液,用cmol/L Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V1mL。
根据上述分析数据,测得该饮用水中ClO2-的浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】碱式碳酸镁有多种不同的组成,如:Mg2(OH)2CO3、Mg4(OH)2(CO3)3、Mg5(OH)2(CO3)4等。某研究性学习小组的同学们为了确定某碱式碳酸镁的组成,设下图所示的实验装置。

(1)实验步骤:
①按上图(夹持仪器未画出)组装好置后,首先进行的操作是___________ 。E处干燥管盛放的药品是___________ 。
②称取碱式碳酸镁样品m1g,并将其放入硬质玻璃管中;
称量:装浓硫酸的洗气瓶C的质量为m2g;装碱石灰的U形管D的质量为m3g
③打开活塞___________ ,关闭___________ 缓缓鼓入空气数分钟。
④关闭活塞___________ ,打开___________ ,点燃酒精灯加热,待不再产生气体为止。
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,称得洗气瓶C的质量为m4g;U形管D的质量为m5g.实验测得数据如下:m1=31g ,m2=87.6g ,m3= 74.7g,m4= 89.4g,m5= 87.9g,计算推导:该碱式碳酸镁的化学式为___________ 。
(2)关于该实验方案,以下说法你认为正确的是___________ (填字母)
A.硬质玻璃管中有水凝结对测定结果有较大影响
B.不称量碱式碳酸镁样品的质量无法确定碱式碳酸镁的组成
C.该实验装置也可用于确定天然碱[aNa2CO3·bNaHCO3·cH2O(a、b、c为正整数)]的化学组成

(1)实验步骤:
①按上图(夹持仪器未画出)组装好置后,首先进行的操作是
②称取碱式碳酸镁样品m1g,并将其放入硬质玻璃管中;
称量:装浓硫酸的洗气瓶C的质量为m2g;装碱石灰的U形管D的质量为m3g
③打开活塞
④关闭活塞
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,称得洗气瓶C的质量为m4g;U形管D的质量为m5g.实验测得数据如下:m1=31g ,m2=87.6g ,m3= 74.7g,m4= 89.4g,m5= 87.9g,计算推导:该碱式碳酸镁的化学式为
(2)关于该实验方案,以下说法你认为正确的是
A.硬质玻璃管中有水凝结对测定结果有较大影响
B.不称量碱式碳酸镁样品的质量无法确定碱式碳酸镁的组成
C.该实验装置也可用于确定天然碱[aNa2CO3·bNaHCO3·cH2O(a、b、c为正整数)]的化学组成
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】磷化氢(PH3)常用于有机合成、粮仓杀虫等。实验室用白磷(P4)与浓 NaOH加热制备 PH3,同时得到次磷酸钠(NaH2PO2),装置如图。
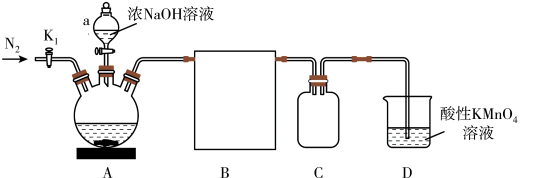
(已知:PH3是无色有毒气体,有强还原性,易自燃;丁醇沸点 117.7℃)
(1)实验室少量白磷保存于______ 。
(2)仪器 a 的名称为______ ,B 应选用图中装置______ 。

(3)实验操作步骤如下:
① 打开 K1,通入 N2一段时间;
② 检查装置气密性;
③ 关闭 K1,打开磁力加热搅拌器加热至 50℃~60℃,滴加烧碱溶液;
④ 在 A 中加入丁醇和白磷。
则正确的操作顺序是______ 。
(4)装置A中发生反应的化学方程式为______ ,使用丁醇作为反应物的分散剂,目的是______ 。
(5)装置C、D的作用分别是______ 、______ 。
(6)测定NaH2PO2纯度。分离提纯A中反应后的混合物,得到NaH2PO2(M=88g·mol-1)粗品,并取1.00g配成100mL溶液。取20.00mL于锥形瓶中,酸化后加入30.00mL0.100mol·L-1碘水,充分反应,以淀粉溶液作指示剂,用0.100mol·L-1Na2S2O3溶液滴定至终点,平均消耗20.00mL。则产品纯度为______ 。(相关反应为:H2PO +H2O+I2=H2PO
+H2O+I2=H2PO +2H++2I-,2S2O
+2H++2I-,2S2O +I2=S4O
+I2=S4O +2I-)
+2I-)

(已知:PH3是无色有毒气体,有强还原性,易自燃;丁醇沸点 117.7℃)
(1)实验室少量白磷保存于
(2)仪器 a 的名称为

(3)实验操作步骤如下:
① 打开 K1,通入 N2一段时间;
② 检查装置气密性;
③ 关闭 K1,打开磁力加热搅拌器加热至 50℃~60℃,滴加烧碱溶液;
④ 在 A 中加入丁醇和白磷。
则正确的操作顺序是
(4)装置A中发生反应的化学方程式为
(5)装置C、D的作用分别是
(6)测定NaH2PO2纯度。分离提纯A中反应后的混合物,得到NaH2PO2(M=88g·mol-1)粗品,并取1.00g配成100mL溶液。取20.00mL于锥形瓶中,酸化后加入30.00mL0.100mol·L-1碘水,充分反应,以淀粉溶液作指示剂,用0.100mol·L-1Na2S2O3溶液滴定至终点,平均消耗20.00mL。则产品纯度为
 +H2O+I2=H2PO
+H2O+I2=H2PO +2H++2I-,2S2O
+2H++2I-,2S2O +I2=S4O
+I2=S4O +2I-)
+2I-)
您最近一年使用:0次



