下列说法正确的是( )
| A.水气化和水分解两个变化过程中都需破坏共价键 |
| B.在O2、CO2和SiO2中,都存在共价键,它们均由分子构成 |
| C.NH3和H2O可以形成氢键,这也是氮极易溶于水的原因之一 |
| D.CCl4、BF3分子中每个原子的最外层都具有8电子稳定结构 |
更新时间:2020-08-31 14:46:38
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】2023年是门捷列夫发现元素周期律154周年,如图为元素周期表的一部分。门捷列夫预言了多种当时未知的元素,T为其中之一。L在地壳中含量排第二位,广泛应用于信息技术等领域。
(1)写出J的原子结构示意图:___________ 。
(2)下列说法不正确的是___________。
(3)LZ2属于___________ (填“共价化合物”或“离子化合物”)。
(4)非金属性:Q___________ M(填“<”、“=”或“>”),判断依据是(试用一个化学方程式来表示)________________ 。
| Y | Z | ||
| L | J | Q | |
| T | M |
(2)下列说法不正确的是___________。
| A.T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ2 |
| B.Q、J的氧化物的水化物酸性:J<Q |
| C.用pH试纸测得Q单质的水溶液pH=3 |
| D.原子半径大小:L>J>Z |
(4)非金属性:Q
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】固体 A 的化学式为 NH5,它的所有原子的最外层都符合相应稀有气体原子的最外层电子结构,与H2O反应生成H2下列说法错误的是
| A.1 molNH5 中含有 4NA个N—H 键(NA表示阿伏加 德罗常数) |
| B.NH5中既有共价键又有离子键 |
| C.NH5中的氢离子的电子层排布与Li+不相同 |
| D.它与水反应的化学方程式为:NH5+H2O=NH3·H2O+H2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
A.电负性大小顺序: | B.稳定性:甲烷>乙烯 |
| C.所有非金属元素都分布在p区 | D. 的熔沸点比 的熔沸点比 的熔沸点高是因为H—O比H—S更稳定 的熔沸点高是因为H—O比H—S更稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】黄砷(As4)与白磷(P4)的结构类似,下列说法正确的是
| A.两者都是共价化合物 | B.黄砷的熔点高于白磷 |
| C.黄砷中共价键键能大于白磷 | D.分子中共价键键角均为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】氨的常见氢化物有氨 和肼
和肼 。
。 与水反应可产生
与水反应可产生 ,液氨发生微弱电离产生
,液氨发生微弱电离产生 ,液氨能与碱金属(如
,液氨能与碱金属(如 、K)反应产生
、K)反应产生 。
。 中一个H被
中一个H被 取代可得
取代可得 ,常温下
,常温下 为液体,具有很高的燃烧热
为液体,具有很高的燃烧热 。以硫酸为电解质,通过催化电解可将
。以硫酸为电解质,通过催化电解可将 转化为
转化为 ;碱性条件下,
;碱性条件下, 氧化
氧化 也可制备
也可制备 。下列物质结构与性质或物质性质与用途
。下列物质结构与性质或物质性质与用途不 具有对应关系的是
 和肼
和肼 。
。 与水反应可产生
与水反应可产生 ,液氨发生微弱电离产生
,液氨发生微弱电离产生 ,液氨能与碱金属(如
,液氨能与碱金属(如 、K)反应产生
、K)反应产生 。
。 中一个H被
中一个H被 取代可得
取代可得 ,常温下
,常温下 为液体,具有很高的燃烧热
为液体,具有很高的燃烧热 。以硫酸为电解质,通过催化电解可将
。以硫酸为电解质,通过催化电解可将 转化为
转化为 ;碱性条件下,
;碱性条件下, 氧化
氧化 也可制备
也可制备 。下列物质结构与性质或物质性质与用途
。下列物质结构与性质或物质性质与用途A. 分子间存在氢键, 分子间存在氢键, 极易溶于水 极易溶于水 |
| B.液氨汽化时吸收大量的热,可用作制冷剂 |
C. 中N原子能与 中N原子能与 形成配位键, 形成配位键, 的水溶液呈碱性 的水溶液呈碱性 |
D. 具有还原性,可用作燃料电池的燃料 具有还原性,可用作燃料电池的燃料 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】短周期主族元素X、Y、Z、W原子序数依次增大,四种元素组成的一种食品添加剂结构如图所示,Z的原子半径在短周期主族元素中最大,W基态原子的s能级电子总数是p能级电子总数的 。下列说法正确的是
。下列说法正确的是
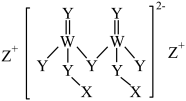
 。下列说法正确的是
。下列说法正确的是
| A.电负性:Y>X>W |
| B.Y、Z形成的简单离子半径:Y<Z |
| C.W、Y形成的简单氢化物沸点:Y<W |
| D.Z分别与X、Y形成的化合物与水反应得到相同的溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列推论正确的是
| A.SiH4的沸点高于CH4,可推测PH3 的沸点也高于NH3 |
| B.CO2 晶体是分子晶体,可推测SiO2 晶体也是分子晶体 |
| C.PCl3 为三角锥形,可推测NF3 也为三角锥形结构 |
| D.C2H6的碳链是直线形的,可推测C3H8 的碳链也是直线形的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.分子内共价键越强,分子越稳定,其形成的晶体的熔沸点也越高 |
| B.离子键的本质就是阴、阳离子之间的相互吸引 |
| C.金刚石转化为石墨的过程中不存在化学键被破坏的过程 |
| D.由原子构成的晶体可能是原子晶体,也可能是分子晶体 |
您最近一年使用:0次


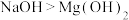

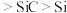
 中的
中的 键成键原理完全相同
键成键原理完全相同
 比
比 熔沸点高
熔沸点高

