下表是元素周期表的一部分。
(1)写出表中 元素的元素符号:
元素的元素符号:
__________ 、
__________ 、
__________ 、
__________ 、
__________ 、
__________ 、
__________ 、
__________ 。
(2) 的简单离子的结构示意图为
的简单离子的结构示意图为________ 。
(3) 元素形成的单质中氧化性最强的是
元素形成的单质中氧化性最强的是_______ ,还原性最强的是_____ 。
(4) 元素最高价氧化物对应的水化物中酸性最强的是
元素最高价氧化物对应的水化物中酸性最强的是_____ ,最稳定的气态氢化物是______ 。
(5)按碱性逐渐减弱、酸性逐渐增强的顺序,将 、
、 、
、 、
、 4种元素的最高价氧化物对应的水化物的化学式进行排序
4种元素的最高价氧化物对应的水化物的化学式进行排序_______ 。
(6) 单质与
单质与 的最高价氧化物对应的水化物反应的离子方程式为
的最高价氧化物对应的水化物反应的离子方程式为________ 。
| 族 周期 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | 0 |
| 1 |  | |||||||
| 2 |  |  |  | |||||
| 3 |  |  |  |  |
(1)写出表中
 元素的元素符号:
元素的元素符号:







(2)
 的简单离子的结构示意图为
的简单离子的结构示意图为(3)
 元素形成的单质中氧化性最强的是
元素形成的单质中氧化性最强的是(4)
 元素最高价氧化物对应的水化物中酸性最强的是
元素最高价氧化物对应的水化物中酸性最强的是(5)按碱性逐渐减弱、酸性逐渐增强的顺序,将
 、
、 、
、 、
、 4种元素的最高价氧化物对应的水化物的化学式进行排序
4种元素的最高价氧化物对应的水化物的化学式进行排序(6)
 单质与
单质与 的最高价氧化物对应的水化物反应的离子方程式为
的最高价氧化物对应的水化物反应的离子方程式为
更新时间:2020-09-06 08:15:44
|
【知识点】 元素周期表提供的元素信息解读
相似题推荐
填空题
|
适中
(0.65)
【推荐1】元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,并回答下列问题:
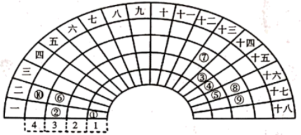
(1)元素②的名称为___________ ;元素⑩在常见周期表中的位置是___________ 。
(2)元素③、④、⑤形成的简单氢化物,稳定性最强的是___________ (填化学式,下同);元素④、⑧、⑨的最高价氧化物对应的水化物,酸性最强的是___________ 。
(3)元素⑥、⑦、⑧对应的简单离子的半径由大到小的顺序为___________ (用离子符号表示)。
(4)元素①、⑤和元素①、⑧均能形成18电子的化合物,这两种化合物发生反应的化学方程式为___________ 。
(5)请设计简单实验,比较元素②、⑦的金属性强弱。

(1)元素②的名称为
(2)元素③、④、⑤形成的简单氢化物,稳定性最强的是
(3)元素⑥、⑦、⑧对应的简单离子的半径由大到小的顺序为
(4)元素①、⑤和元素①、⑧均能形成18电子的化合物,这两种化合物发生反应的化学方程式为
(5)请设计简单实验,比较元素②、⑦的金属性强弱。
| 实验步骤 | 实验现象 | 实验结论 |
| 金属性:②>⑦ |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下表是元素周期表的一部分,针对表中的①~⑧种元素,填写下列空白:
(1)在最高价氧化物的水化物中,酸性最强的化合物的名称 是______ ,碱性最强的化合物的化学式 是_______ 。
(2)⑤⑦形成化合物的电子式___ 。②形成的最高价氧化物的结构式____ 。
(3)最高价氧化物是两性氧化物的元素 其元素符号是____ ;写出它的氢氧化物与 ⑧的最高价氧化物的水化物反应的离子方程式
⑧的最高价氧化物的水化物反应的离子方程式________ 。
(4)⑥的单质与⑤的最高价氧化物的水化物反应的离子方程式是______ 。
(5)②和⑦可形成原子数1∶2的液态化合物甲,并能溶解⑦的单质,用电子式表示甲的形成过程:____________ 。
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
2 | ① | ② | ③ | ④ | |||
3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)在最高价氧化物的水化物中,酸性最强的化合物的
(2)⑤⑦形成化合物的电子式
(3)最高价氧化物是两性氧化物的
 ⑧的最高价氧化物的水化物反应的离子方程式
⑧的最高价氧化物的水化物反应的离子方程式(4)⑥的单质与⑤的最高价氧化物的水化物反应的离子方程式是
(5)②和⑦可形成原子数1∶2的液态化合物甲,并能溶解⑦的单质,用电子式表示甲的形成过程:
您最近一年使用:0次



