实验室制备 1,2-二溴乙烷,可用足量的乙醇先制备乙烯,再用乙烯和少量的溴制备 1,2-二溴乙烷,装置如下图所示:
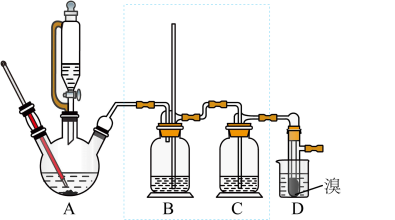
有关数据列表如下:
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到 170℃左右,其最主要目的是_______ ; (填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置 A 中除了浓硫酸和乙醇外,还应加入___ ,装置A 中生成副产物乙醚的化学反应方程式__ 。
(3) 实验室制取乙烯,常因温度过高而使乙醇和浓 H2SO4反应生成少量的二氧化硫,为了验证二氧化硫的存在并除去二氧化硫对后续反应的干扰,某同学在 A 和 D 之间加入了 B、C 两个装置,其中 B 和C 中可分别盛放_____ 。
a.酸性 KMnO4和水 b.品红和NaOH 溶液
c.酸性 KMnO4和 NaOH 溶液 d.品红和酸性 KMnO4
(4) 将 1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在______ 层(填“上”、“下”);若产物中有少量副产物乙醚。可用_______ 的方法除去。

有关数据列表如下:
物质 | 乙醇 | 1,2—二溴乙烷 | 乙醚 |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g‧cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到 170℃左右,其最主要目的是
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置 A 中除了浓硫酸和乙醇外,还应加入
(3) 实验室制取乙烯,常因温度过高而使乙醇和浓 H2SO4反应生成少量的二氧化硫,为了验证二氧化硫的存在并除去二氧化硫对后续反应的干扰,某同学在 A 和 D 之间加入了 B、C 两个装置,其中 B 和C 中可分别盛放
a.酸性 KMnO4和水 b.品红和NaOH 溶液
c.酸性 KMnO4和 NaOH 溶液 d.品红和酸性 KMnO4
(4) 将 1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在
更新时间:2020-09-07 22:48:38
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验室制取乙烯的装置如图Ⅰ所示。根据实验及有关操作回答下列问题。
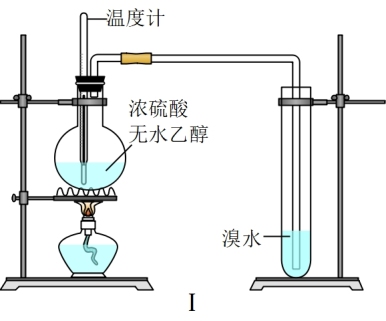
(1)甲同学按照如图Ⅰ所示的实验装置进行了实验。当温度升至170℃左右时,有大量气体产生,产生的气体通入溴水中,溴水的颜色迅速褪去。甲同学认为达到了实验目的,写出烧瓶中发生反应的化学方程式:___ 。
(2)乙同学仔细考察了甲同学的整个实验过程,发现当温度升到100℃左右时,无色液体开始变色,到160℃左右时,混合液全呈黑色,在超过170℃后生成气体速度明显加快,生成的气体有刺激性气味。由此他推出,产生的气体中应有某杂质,可能影响乙烯的检验,必须除去。乙同学设计了如图Ⅱ所示的实验装置进行实验。请回答:
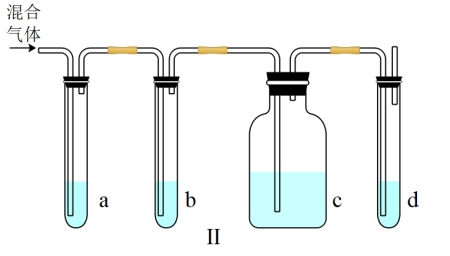
①Ⅱ装置abcd中可盛放的试剂的顺序依次是____ (填序号)。
a.品红溶液 b.NaOH溶液 c.浓硫酸 d.酸性KMnO4溶液
②乙设计的实验中能确定生成了乙烯的现象是____ 。
(3)丙同学根据甲、乙同学的分析,认为还可能有CO、CO2两种气体产生。为证明CO的存在,他设计了如图Ⅲ所示过程(假设该过程可把实验中产生的有机产物除净),发现最后气体经点燃产生蓝色火焰,确认有一氧化碳生成。
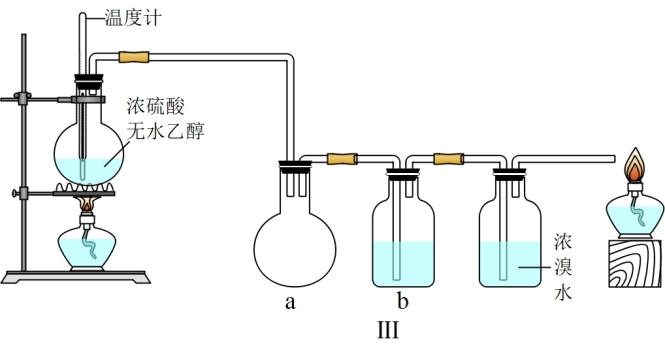
①图Ⅲ中装置a的作用是____ 。
②为除去混合气中的SO2和CO2,装置b中应该盛放的试剂是____ 。
③浓溴水的作用是____ 。
④丙同学认为该装置还需添加一个装置验证杂质气体是否除净,该操作是____ 。

(1)甲同学按照如图Ⅰ所示的实验装置进行了实验。当温度升至170℃左右时,有大量气体产生,产生的气体通入溴水中,溴水的颜色迅速褪去。甲同学认为达到了实验目的,写出烧瓶中发生反应的化学方程式:
(2)乙同学仔细考察了甲同学的整个实验过程,发现当温度升到100℃左右时,无色液体开始变色,到160℃左右时,混合液全呈黑色,在超过170℃后生成气体速度明显加快,生成的气体有刺激性气味。由此他推出,产生的气体中应有某杂质,可能影响乙烯的检验,必须除去。乙同学设计了如图Ⅱ所示的实验装置进行实验。请回答:

①Ⅱ装置abcd中可盛放的试剂的顺序依次是
a.品红溶液 b.NaOH溶液 c.浓硫酸 d.酸性KMnO4溶液
②乙设计的实验中能确定生成了乙烯的现象是
(3)丙同学根据甲、乙同学的分析,认为还可能有CO、CO2两种气体产生。为证明CO的存在,他设计了如图Ⅲ所示过程(假设该过程可把实验中产生的有机产物除净),发现最后气体经点燃产生蓝色火焰,确认有一氧化碳生成。

①图Ⅲ中装置a的作用是
②为除去混合气中的SO2和CO2,装置b中应该盛放的试剂是
③浓溴水的作用是
④丙同学认为该装置还需添加一个装置验证杂质气体是否除净,该操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
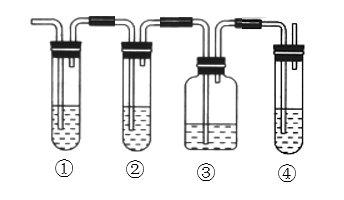
【推荐2】实验室中通常用加热无水乙醇与浓硫酸的混合物的方法制取乙烯,浓硫酸是乙醇反应的催化剂和脱水剂。在具体的化学实验中常因加热的温度过高导致副反应发生而使乙烯气体中混有二氧化硫气体。下图所表示的装置可以用于确认乙烯气体中混有二氧化硫气体。
可选择的化学试剂有:
A.品红溶液 B.烧碱溶液 C.浓硫酸 D.酸性高锰酸钾溶液
回答下列问题:
(1)由乙醇生成乙烯的化学反应方程式是__________________________________ ,
该化学反应所属的类型可以是________ 或________ 。
A.取代反应 B.加成反应 C.脱水反应 D.消去反应
(2)图中①、②、③、④的容器内盛放的化学试剂分别是(填写代号)
①________ 、②________ 、③________ 、④________ 。
(3)能说明二氧化硫气体存在的现象是____________________ 。
(4)使用装置②的目的是________________ ;使用装置③的目的是________________ 。
(5)确认乙烯气体存在的现象是__________________________ 。
(6)实验室中可以采用将乙烯气体通入酸性高锰酸钾溶液的实验方法证明乙烯具有容易被氧化的化学性质。在将乙烯气体通入酸性高锰酸钾溶液之前要进行的一项实验是____________ 。

可选择的化学试剂有:
A.品红溶液 B.烧碱溶液 C.浓硫酸 D.酸性高锰酸钾溶液
回答下列问题:
(1)由乙醇生成乙烯的化学反应方程式是
该化学反应所属的类型可以是
A.取代反应 B.加成反应 C.脱水反应 D.消去反应
(2)图中①、②、③、④的容器内盛放的化学试剂分别是(填写代号)
①
(3)能说明二氧化硫气体存在的现象是
(4)使用装置②的目的是
(5)确认乙烯气体存在的现象是
(6)实验室中可以采用将乙烯气体通入酸性高锰酸钾溶液的实验方法证明乙烯具有容易被氧化的化学性质。在将乙烯气体通入酸性高锰酸钾溶液之前要进行的一项实验是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
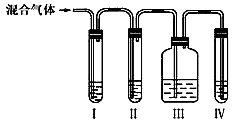
【推荐3】为探究乙烯与溴的加成反应:甲同学设计并进行了如下实验:先用乙醇和浓硫酸为原料制取乙烯,将生成的气体直接通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应。乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量浓硫酸的还原产物气体,由此他提出必须先除去之,再与溴水反应。请你回答下列问题:
(l)乙同学推测此乙烯中必定含有的一种杂质气体,它与溴水反应的化学方程式是_______ ,在验证过程中必须全部除去,为此乙同学设计了如图所示的实验装置。请回答:______ ;Ⅱ______ ;Ⅲ______ ;Ⅳ______ ;(选填序号)。
A.品红溶液 B. NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
② 乙设计的实验中能确定生成了乙烯的现象是_____________ 。
(2)为验证乙烯与溴的反应是加成反应而不是取代反应,丙同学提出可将上述乙除杂后的气体通入溴水中,用pH试纸测反应后溶液的酸碱性,你认为是否合理______ (填合理、不合理),理由是___________________ 。
(3)比赛中,当运动员肌肉挫伤或扭伤时,队医随即对准球员的受伤部位喷射药剂氯乙烷(沸点12.27℃),进行局部冷冻麻醉应急处理。要得到较纯净的氯乙烷应采用的制取方法是[用化学反应方程式(有机物用结构简式表示)]___________ 。该反应的类型是______ 反应。决定氯乙烷能用于冷冻麻醉应急处理的具体性质______________ 。
(l)乙同学推测此乙烯中必定含有的一种杂质气体,它与溴水反应的化学方程式是
A.品红溶液 B. NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
② 乙设计的实验中能确定生成了乙烯的现象是
(2)为验证乙烯与溴的反应是加成反应而不是取代反应,丙同学提出可将上述乙除杂后的气体通入溴水中,用pH试纸测反应后溶液的酸碱性,你认为是否合理
(3)比赛中,当运动员肌肉挫伤或扭伤时,队医随即对准球员的受伤部位喷射药剂氯乙烷(沸点12.27℃),进行局部冷冻麻醉应急处理。要得到较纯净的氯乙烷应采用的制取方法是[用化学反应方程式(有机物用结构简式表示)]
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验室里用乙醇和浓硫酸反应生成乙烯,接着再用溴与之反应生成1,2-二溴乙烷,在制备过程中有部分乙醇被浓硫酸氧化产生CO2、SO2,SO2进一步与Br2反应生成HBr等物质。
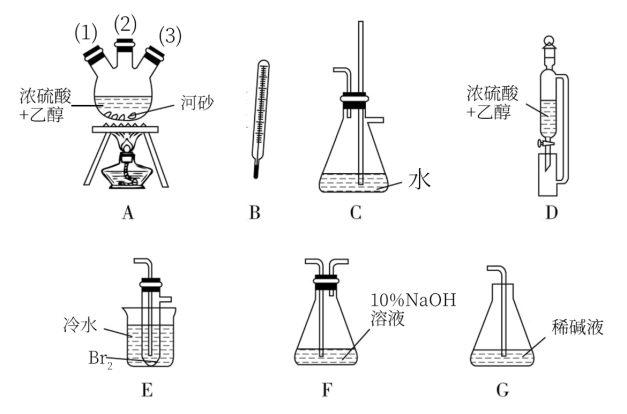
(1)用下列仪器,以上述三种物质为原料制备1,2-二溴乙烷.如果气体流向为从左到右,正确的连接顺序是(短接口或橡皮管均已略去):_____ 经A(1)插入A中,_____ 接A(2);A(3)接_____ 接_____ 接_____ 接_____ (填各装置的代号)
(2)在三颈烧瓶A中的主要反应的化学方程式为_________________________ ;
(3)在反应管E中进行的主要反应的化学方程式为_________________________ ;
(4)温度计水银球的正确位置是_________________________ ;
(5)反应管E中加入少量水及把反应管E置于盛有冷水的小烧杯中是因为________________________ 。

(1)用下列仪器,以上述三种物质为原料制备1,2-二溴乙烷.如果气体流向为从左到右,正确的连接顺序是(短接口或橡皮管均已略去):
(2)在三颈烧瓶A中的主要反应的化学方程式为
(3)在反应管E中进行的主要反应的化学方程式为
(4)温度计水银球的正确位置是
(5)反应管E中加入少量水及把反应管E置于盛有冷水的小烧杯中是因为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】下图是实验室用来验证乙烯与氢气反应产物的装置,请回答下列问题:
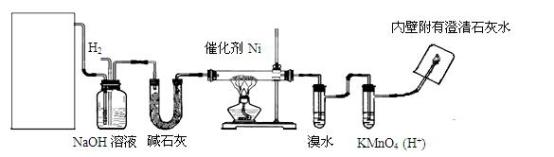
(1)方框内装置用来制取乙烯,其中包括的仪器是:①碎瓷片②石棉网和铁架台③圆底烧瓶④温度计(量程100℃)⑤温度计(量程200℃)⑥酒精灯⑦单孔塞⑧双孔塞⑨导管。不选用的仪器有_______ (填编号)。
(2)写出制乙烯化学方程式:_______ 。
(3)碱石灰的作用是:_______ 。
(4)实验过程中,发现溴水会褪色,可能的原因是:_______ 。
(5)出现什么现象可说明生成了乙烷?_______ 。

(1)方框内装置用来制取乙烯,其中包括的仪器是:①碎瓷片②石棉网和铁架台③圆底烧瓶④温度计(量程100℃)⑤温度计(量程200℃)⑥酒精灯⑦单孔塞⑧双孔塞⑨导管。不选用的仪器有
(2)写出制乙烯化学方程式:
(3)碱石灰的作用是:
(4)实验过程中,发现溴水会褪色,可能的原因是:
(5)出现什么现象可说明生成了乙烷?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】如图所示是实验室利用乙醇消去反应制取乙烯并检验产物的实验装置图。回答以下问题。___________ 。
(2)为避免发生副反应,烧瓶 中的温度需要迅速升至170C∘,副反应的化学方程式为
中的温度需要迅速升至170C∘,副反应的化学方程式为___________ 。
(3)反应中,观察到烧瓶 中混合液变为黑色,有气态副产物生成。
中混合液变为黑色,有气态副产物生成。
①装置 中所用试剂为滴加酚酞的
中所用试剂为滴加酚酞的 溶液,用于除去气体中的杂质,在虚线方框内将装置
溶液,用于除去气体中的杂质,在虚线方框内将装置 补充完整
补充完整___________ 。
②实验过程中,装置 中溶液颜色变浅,用化学方程式说明原因
中溶液颜色变浅,用化学方程式说明原因___________ 。
(4)装置C中所用试剂为溴水,用于检验乙烯的生成,实验中在该装置处观察到的实验现象为___________ ;反应一段时间后,装置C中溶液分层,有机物位于___________ (填“上”或“下”)层。
(5)有同学认为在装置C后应添加一个尾气处理装置,该装置中的试剂应选择___________ (填序号)。
 酸性
酸性 溶液
溶液  碱石灰
碱石灰  浓
浓

(2)为避免发生副反应,烧瓶
 中的温度需要迅速升至170C∘,副反应的化学方程式为
中的温度需要迅速升至170C∘,副反应的化学方程式为(3)反应中,观察到烧瓶
 中混合液变为黑色,有气态副产物生成。
中混合液变为黑色,有气态副产物生成。①装置
 中所用试剂为滴加酚酞的
中所用试剂为滴加酚酞的 溶液,用于除去气体中的杂质,在虚线方框内将装置
溶液,用于除去气体中的杂质,在虚线方框内将装置 补充完整
补充完整②实验过程中,装置
 中溶液颜色变浅,用化学方程式说明原因
中溶液颜色变浅,用化学方程式说明原因(4)装置C中所用试剂为溴水,用于检验乙烯的生成,实验中在该装置处观察到的实验现象为
(5)有同学认为在装置C后应添加一个尾气处理装置,该装置中的试剂应选择
 酸性
酸性 溶液
溶液  碱石灰
碱石灰  浓
浓
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】1-溴丁烷常用作稀有元素萃取剂、烃化剂及合成染料和香料的有机原料。实验室制备1-溴丁烷的反应、主要装置和有关数据如下:NaBr+H2SO4 NaHSO4+HBr↑、CH3CH2CH2CH2OH+HBr
NaHSO4+HBr↑、CH3CH2CH2CH2OH+HBr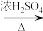 CH3CH2CH2CH2Br+H2O。
CH3CH2CH2CH2Br+H2O。
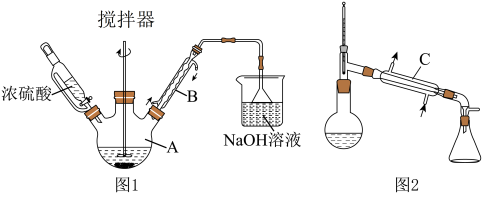
实验步骤:
在仪器A中加入10mL水,边搅拌边缓慢滴加20mL过量的浓硫酸,冷却至室温。再依次加入7.4g正丁醇、16.5g研细的溴化钠和几粒沸石。在不断搅拌下,用图1所示装置小火加热回流90min,得到粗品。
将粗品依次用15mL水、7mL浓硫酸、10mL水、10mL饱和碳酸氢钠溶液、10mL水洗涤并分液,分出的产物用无水氯化钙充分干燥,滤除氯化钙固体,用图2所示装置加热蒸馏,收集99~103℃的馏分,得纯净1-溴丁烷9.3g。
回答下列问题:
(1)仪器B的名称是___________ 。仪器B与仪器C___________ (填“能”或“不能”)交换使用。
(2)NaOH溶液的作用是___________ 。
(3)粗品经第一次水洗后,所得产物略带红棕色,其原因是___________ 。
用浓硫酸洗涤的主要目的是___________ ,在用浓硫酸洗涤、分液的操作中,待液体分层后,产物应从分液漏斗的___________ (填“上口倒出”或“下口放出”)。
(4)产品用浓硫酸洗涤后,不直接用饱和碳酸氢钠溶液洗涤而先用水洗,其原因是___________ 。
(5)本实验最可能产生两种有机副产物,任写其中一种副产物的结构简式___________ 。
(6)本实验中,1-溴丁烷的产率为___________ (保留三位有效数字)。
 NaHSO4+HBr↑、CH3CH2CH2CH2OH+HBr
NaHSO4+HBr↑、CH3CH2CH2CH2OH+HBr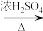 CH3CH2CH2CH2Br+H2O。
CH3CH2CH2CH2Br+H2O。
| 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度(g/cm3) | 溶解性 | |
| 正丁醇 | 74 | -89.8 | 117.7 | 0.81 | 微溶于水,易溶于浓硫酸和有机溶剂 |
| 1-溴丁烷 | 137 | -112.4 | 101.6 | 1.28 | 不溶于水,易溶于醇、醚等有机溶剂 |
| 浓硫酸 | 98 | 10.3 | 338 | 1.84 | 易溶于水 |
在仪器A中加入10mL水,边搅拌边缓慢滴加20mL过量的浓硫酸,冷却至室温。再依次加入7.4g正丁醇、16.5g研细的溴化钠和几粒沸石。在不断搅拌下,用图1所示装置小火加热回流90min,得到粗品。
将粗品依次用15mL水、7mL浓硫酸、10mL水、10mL饱和碳酸氢钠溶液、10mL水洗涤并分液,分出的产物用无水氯化钙充分干燥,滤除氯化钙固体,用图2所示装置加热蒸馏,收集99~103℃的馏分,得纯净1-溴丁烷9.3g。
回答下列问题:
(1)仪器B的名称是
(2)NaOH溶液的作用是
(3)粗品经第一次水洗后,所得产物略带红棕色,其原因是
用浓硫酸洗涤的主要目的是
(4)产品用浓硫酸洗涤后,不直接用饱和碳酸氢钠溶液洗涤而先用水洗,其原因是
(5)本实验最可能产生两种有机副产物,任写其中一种副产物的结构简式
(6)本实验中,1-溴丁烷的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】实验室制备溴乙烷的装置和步骤如图:(加热装置已略去)

实验流程:
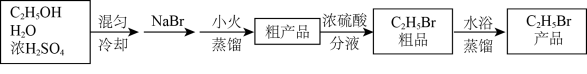
已知:①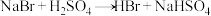
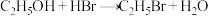
②溴乙烷的沸点为38.4℃,密度约1.45g·mL-1(25℃)
③乙醇、乙醚等有机物在浓硫酸中会因质子化而溶于浓硫酸,浓硫酸密度约1.84g·mL-1
请回答下列问题:
(1)仪器A的名称________ ,冷却水的出水口是________ 。(填a或b)
(2)第一次蒸馏制得的粗产品中含有主要杂质是乙醚,产生这种杂质的化学反应方程式为________________ 。
(3)分液时粗产品位于________ 层(上或下),第二次蒸馏时采用水浴加热,水浴温度应控制在________ 。
(4)某同学在加入浓硫酸后立即加入NaBr粉末,发现制得粗产品略显黄色,其可能的原因是________ 。(用化学方程式表示)
(5)试设计实验证明最终产品是卤代烃________________ 。

实验流程:

已知:①
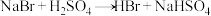
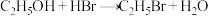
②溴乙烷的沸点为38.4℃,密度约1.45g·mL-1(25℃)
③乙醇、乙醚等有机物在浓硫酸中会因质子化而溶于浓硫酸,浓硫酸密度约1.84g·mL-1
请回答下列问题:
(1)仪器A的名称
(2)第一次蒸馏制得的粗产品中含有主要杂质是乙醚,产生这种杂质的化学反应方程式为
(3)分液时粗产品位于
(4)某同学在加入浓硫酸后立即加入NaBr粉末,发现制得粗产品略显黄色,其可能的原因是
(5)试设计实验证明最终产品是卤代烃
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度为2.18g·cm-3,沸点为131.4℃ ,熔点为9.3℃,微溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验中可以用如图所示装置制备1,2-二溴乙烷 ,其中试管d中装有液溴(表面覆盖少量水)。回答下列问题:
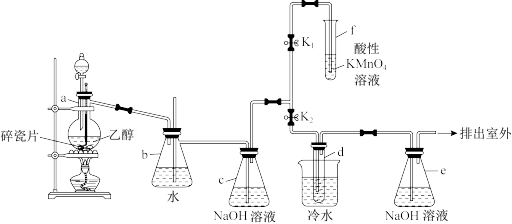
(1)仪器a的名称是______ ,1,2-二溴乙烷在______ (填字母)中得到。
(2)组装好仪器后,实验开始前要进行的操作是______ 。
(3)a中的反应要求温度迅速升高到170℃,不宜太低也不能太高,太低乙醇容易发生副反应,太高会观察到a中溶液变黑,请写出乙醇在170℃发生的主要反应的化学方程式:______ 。
(4)打开K1,关闭K2,f中的现象能说明______ (填物质名称)具有______ ;若无装置c,能否说明f中现象得到的结论,______ (填“能”或“不能”),理由:______ 。
(5)装置e的作用是______ 。

(1)仪器a的名称是
(2)组装好仪器后,实验开始前要进行的操作是
(3)a中的反应要求温度迅速升高到170℃,不宜太低也不能太高,太低乙醇容易发生副反应,太高会观察到a中溶液变黑,请写出乙醇在170℃发生的主要反应的化学方程式:
(4)打开K1,关闭K2,f中的现象能说明
(5)装置e的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验室制备1,2二溴乙烷的反应原理如下:CH3CH2OH CH2=CH2↑+H2O,CH2=CH2+Br2→BrCH2CH2Br。用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如下图所示:
CH2=CH2↑+H2O,CH2=CH2+Br2→BrCH2CH2Br。用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如下图所示:
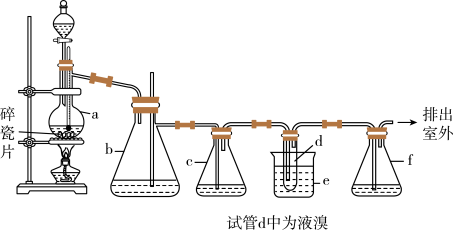
有关数据列表如下:
回答下列问题:
(1)在装置c中应加入________ (选填序号),其目的是吸收反应中可能生成的酸性气体。
①水 ②浓硫酸 ③氢氧化钠溶液 ④饱和碳酸氢钠溶液
(2)判断d管中制备二溴乙烷反应已结束的最简单方法是______________________ 。
(3)将二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在水的________ (填“上”或“下”)层。
(4)若产物中有少量未反应的Br2,最好用________ (填正确选项前的序号)洗涤除去。
①水 ②氢氧化钠溶液 ③碘化钠溶液 ④乙醇
(5)反应过程中需用冷水冷却(装置e),其主要目的是______________________ ; 但不用冰水进行过度冷却,原因_______________________________________________ 。
 CH2=CH2↑+H2O,CH2=CH2+Br2→BrCH2CH2Br。用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如下图所示:
CH2=CH2↑+H2O,CH2=CH2+Br2→BrCH2CH2Br。用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如下图所示:
有关数据列表如下:
| 乙醇 | 1,2二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在装置c中应加入
①水 ②浓硫酸 ③氢氧化钠溶液 ④饱和碳酸氢钠溶液
(2)判断d管中制备二溴乙烷反应已结束的最简单方法是
(3)将二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在水的
(4)若产物中有少量未反应的Br2,最好用
①水 ②氢氧化钠溶液 ③碘化钠溶液 ④乙醇
(5)反应过程中需用冷水冷却(装置e),其主要目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上,三氯乙醛(Cl3CCHO)用于制造敌百虫等杀虫剂、三氯乙醛脲除草剂。医药上用于生产氯霉素等。重庆八中某化学小组希望通过制备三氯乙醛来杀灭宿舍的蚊虫。
[查阅资料]
①反应原理:在80~90 ℃下乙醇与氯气反应生成三氯乙醛,副产物为氯化氢。可能发生的副反应有:C2H5OH+HCl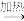 C2H5Cl+H2O,CCl3CHO+HClO
C2H5Cl+H2O,CCl3CHO+HClO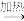 CCl3COOH(三氯乙酸)+HCl
CCl3COOH(三氯乙酸)+HCl
②有关物质的相对分子质量和部分物理性质如表所示:
[设计实验]
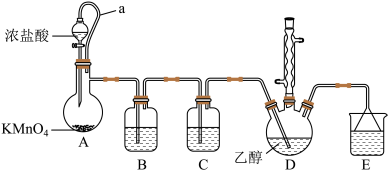
(注:可将D装置放置在磁力搅拌器上使反应物充分混合)
(1)写出A装置中发生反应的离子方程式:___________ 。
(2)实验中D装置的温度需要控制在80~90 ℃,最合适的加热方式是___________ ;写出D装置中制备三氯乙醛的化学方程式:___________ 。
(3)A装置上方橡胶软管a的作用为___________ 。
(4)B装置中的试剂是___________ ,若不使用B装置,D装置中会明显增加的副产物是___________ 。
(5)下列有关说法正确的是___________ 。
a.C装置盛装浓硫酸,用于干燥氯气
b.D装置中球形冷凝管的作用是冷凝回流
c.E装置可盛装FeCl2(aq)、Na2CO3(aq),只吸收尾气中的氯化氢
d.可采用分液操作进一步分离、提纯D装置中的三氯乙醛
(6)测定产品纯度:称取产品0.2950g 配成待测溶液,加入0.1000mol/L碘标准溶液20.00mL,充分反应后,调节溶液的pH,立即用0.02000mol/L Na2S2O3溶液滴定至终点。进行三次平行实验,测得平均消耗Na2S2O3溶液20.00mL。则产品的纯度为___________ 。滴定反应原理:①CCl3CHO+I2+H2O = CCl3COOH+2H++2I-、②I2+2S2O =2I-+S4O
=2I-+S4O
[查阅资料]
①反应原理:在80~90 ℃下乙醇与氯气反应生成三氯乙醛,副产物为氯化氢。可能发生的副反应有:C2H5OH+HCl
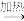 C2H5Cl+H2O,CCl3CHO+HClO
C2H5Cl+H2O,CCl3CHO+HClO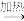 CCl3COOH(三氯乙酸)+HCl
CCl3COOH(三氯乙酸)+HCl②有关物质的相对分子质量和部分物理性质如表所示:
| 物质 | C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl |
| 相对分子质量 | 46 | 147.5 | 163.5 | 64.5 |
| 熔点/℃ | −114.1 | −57.5 | 58 | −140.8 |
| 沸点/℃ | 78.5 | 97.8 | 198 | 12.3 |
| 溶解性 | 与水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇、三氯乙醛 | 微溶于水,可溶于乙醇 |

(注:可将D装置放置在磁力搅拌器上使反应物充分混合)
(1)写出A装置中发生反应的离子方程式:
(2)实验中D装置的温度需要控制在80~90 ℃,最合适的加热方式是
(3)A装置上方橡胶软管a的作用为
(4)B装置中的试剂是
(5)下列有关说法正确的是
a.C装置盛装浓硫酸,用于干燥氯气
b.D装置中球形冷凝管的作用是冷凝回流
c.E装置可盛装FeCl2(aq)、Na2CO3(aq),只吸收尾气中的氯化氢
d.可采用分液操作进一步分离、提纯D装置中的三氯乙醛
(6)测定产品纯度:称取产品0.2950g 配成待测溶液,加入0.1000mol/L碘标准溶液20.00mL,充分反应后,调节溶液的pH,立即用0.02000mol/L Na2S2O3溶液滴定至终点。进行三次平行实验,测得平均消耗Na2S2O3溶液20.00mL。则产品的纯度为
 =2I-+S4O
=2I-+S4O
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】用下图所示的实验装置制取乙酸乙酯。回答以下问题:

(1)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液的方法是先向试管中加入一定量的________ ,然后边振荡边缓缓加入________ ,冷却后再加入一定量的________ ,轻轻振荡使之混合均匀。
(2)浓硫酸的作用是__________________________
(3)饱和碳酸钠溶液的作用是__________________________
(4)生成的乙酸乙酯,其密度比水________ (填“大”或“小”),有________ 味。
(5)与书中采用的实验装置的不同之处是本实验采用了球形干燥管代替了长导管,并将干燥管的末端插入了饱和碳酸钠溶液中。在此处球形干燥管的作用有________ 。

(1)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液的方法是先向试管中加入一定量的
(2)浓硫酸的作用是
(3)饱和碳酸钠溶液的作用是
(4)生成的乙酸乙酯,其密度比水
(5)与书中采用的实验装置的不同之处是本实验采用了球形干燥管代替了长导管,并将干燥管的末端插入了饱和碳酸钠溶液中。在此处球形干燥管的作用有
您最近一年使用:0次



