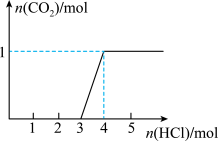
为了测定NaCl、Na2CO3·10H2O和NaHCO3的混合物中各组分的含量,某同学设计如下实验:取一定质量的混合物,通过测量反应前后②和③装置质量的变化,测定该混合物中各组分的质量分数。下列说法错误的是
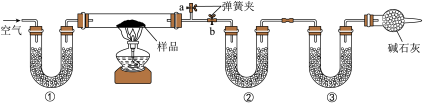

| A.①、②、③中可以依次盛装碱石灰、无水CaCl2、碱石灰 |
| B.若将①装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl含量偏大 |
| C.硬质玻璃管加热前,应关闭b,打开a,缓缓通入空气,直至a处出来的空气不再使澄清石灰水变浑浊为止 |
| D.实验结束时先停止通入空气,再停止加热 |
更新时间:2020-09-13 11:15:54
|
相似题推荐
多选题
|
适中
(0.65)
名校
解题方法
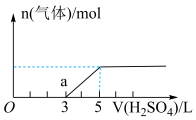
【推荐1】标准状况下,将VL 气体通入2L的NaOH溶液中,在所得溶液中逐滴加入
气体通入2L的NaOH溶液中,在所得溶液中逐滴加入 稀硫酸全过量,产生的气体与消耗的
稀硫酸全过量,产生的气体与消耗的 体积关系如图所示(忽略
体积关系如图所示(忽略 的溶解)。下列说法正确的是
的溶解)。下列说法正确的是
说法正确的是
 气体通入2L的NaOH溶液中,在所得溶液中逐滴加入
气体通入2L的NaOH溶液中,在所得溶液中逐滴加入 稀硫酸全过量,产生的气体与消耗的
稀硫酸全过量,产生的气体与消耗的 体积关系如图所示(忽略
体积关系如图所示(忽略 的溶解)。下列说法正确的是
的溶解)。下列说法正确的是
说法正确的是
A.标准状况下 |
B.O到a点过程中发生反应先后顺序为: 、 、 |
C.a点溶液中所含溶质的化学式为 |
D.NaOH溶液的物质的量浓度为 |
您最近半年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】通过测定混合气中O2含量可计算已变质的Na2O2(含Na2CO3)纯度,实验装置如图(Q为弹性良好的气囊)。下列分析错误的是


| A.量筒Ⅰ用于测二氧化碳的量,干燥管b中装入碱石灰,量筒Ⅱ用于测氧气的量 |
| B.Q气球中产生的气体主要成分为O2、CO2 |
| C.测定气体总体积必须关闭K1、K2,打开K3 |
| D.读完气体总体积后,关闭K3,缓缓打开K1;可观察到Q气球慢慢缩小 |
您最近半年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】下列说法正确的是
| A.小苏打用作食品膨松剂,用激光笔照射硫酸铜溶液,可观察到“丁达尔效应” |
| B.明矾可用于净水,酸雨就是pH<7的雨水 |
| C.工业上可用电解熔融氯化镁制得金属镁 |
| D.煤的气化、液化和石油的裂化、裂解都是化学变化 |
您最近半年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】实验室有一包含有 、
、 和
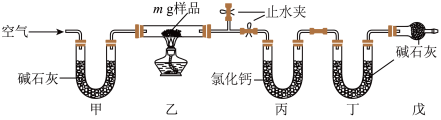
和 的混合物。某同学利用下图所示装置进行实验,通过测量反应前后装置丙和丁的增重,测定该混合物中各组分的质量分数。下列说法错误的是
的混合物。某同学利用下图所示装置进行实验,通过测量反应前后装置丙和丁的增重,测定该混合物中各组分的质量分数。下列说法错误的是
 、
、 和
和 的混合物。某同学利用下图所示装置进行实验,通过测量反应前后装置丙和丁的增重,测定该混合物中各组分的质量分数。下列说法错误的是
的混合物。某同学利用下图所示装置进行实验,通过测量反应前后装置丙和丁的增重,测定该混合物中各组分的质量分数。下列说法错误的是
| A.装置丙中的氯化钙做干燥剂 |
B.撤去装置戊对 质量分数的测得不会造成影响 质量分数的测得不会造成影响 |
C.将装置甲换为盛放浓硫酸的洗气瓶,则测得 的质量分数偏低 的质量分数偏低 |
| D.若能测量样品反应后剩余固体的质量,则撤去装置丁不能达到实验目的 |
您最近半年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】磷化铝与水反应产生高毒的PH3气体(还原性强、易自燃),可用于粮食熏蒸杀虫。食品安全标准规定:粮食中磷化物(以PH3计)的含量低于0.05mg/kg时合格。可用以下方法测定粮食中残留的磷化物含量:
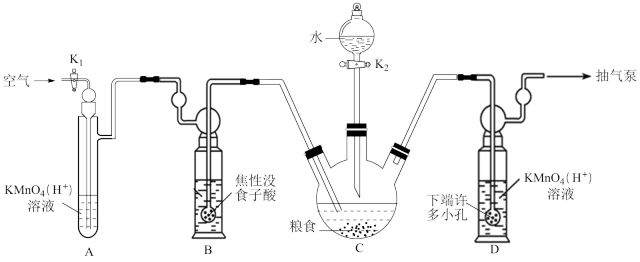
已知:装置C中盛100g粮食。装置D中反应共消耗4.0×10-7mol KMnO4。
下列说法错误的是

已知:装置C中盛100g粮食。装置D中反应共消耗4.0×10-7mol KMnO4。
下列说法错误的是
| A.装置A的作用是除去空气中的还原性气体 |
| B.实验中,应先打开K2,再打开K1,将装置中生成的PH3赶出 |
C.装置D发生反应的离子方程式是:5PH3+8MnO +24H+=5H3PO4+8Mn2++12H2O +24H+=5H3PO4+8Mn2++12H2O |
| D.该原粮样品磷化物的含量合格 |
您最近半年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】将78 g金属钾在空气中燃烧,生成KO2和K2O2的混合物。该混合物与足量的CO2充分反应后生成O2(4KO2+2CO2→2K2CO3+3O2),得到O2的物质的量可能为
| A.0.50 mol | B.0.75 mol | C.1.00 mol | D.1.50 mol |
您最近半年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】实验室有一包含有 、
、 和
和 的混合物。某同学利用下图所示装置进行实验,通过测量反应前后装置丙和丁的增重,测定该混合物中各组分的质量分数。下列说法错误的是
的混合物。某同学利用下图所示装置进行实验,通过测量反应前后装置丙和丁的增重,测定该混合物中各组分的质量分数。下列说法错误的是

 、
、 和
和 的混合物。某同学利用下图所示装置进行实验,通过测量反应前后装置丙和丁的增重,测定该混合物中各组分的质量分数。下列说法错误的是
的混合物。某同学利用下图所示装置进行实验,通过测量反应前后装置丙和丁的增重,测定该混合物中各组分的质量分数。下列说法错误的是
| A.装置丙中的氯化钙做干燥剂 |
B.撤去装置戊对 质量分数的测得不会造成影响 质量分数的测得不会造成影响 |
C.将装置甲换为盛放浓硫酸的洗气瓶,则测得 的质量分数偏低 的质量分数偏低 |
| D.若能测量样品反应后剩余固体的质量,则撤去装置丁不能达到实验目的 |
您最近半年使用:0次
多选题
|
适中
(0.65)
【推荐2】向等量的NaOH溶液中分别通入CO2气体。因CO2的通入量不同,得到组分不同的溶液M。若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)关系如下,(注:①假设CO2全部逸出;②C图中oa=ab)。其中M中只有1种溶质的是
A.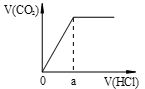 | B.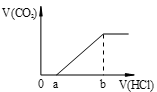 |
C.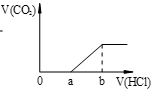 | D.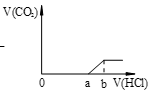 |
您最近半年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐3】FeSO4·7H2O样品5.56 g受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示,下列说法不正确的是
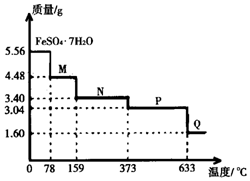

| A.温度为78℃时固体物质M的化学式为FeSO4·3H2O |
| B.取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成,Q的化学式为Fe2O3 |
| C.在隔绝空气条件下,N得到P的化学方程式为FeSO4·H2O=FeSO4+H2O |
| D.温度为159℃时固体N的化学式为FeSO4·2H2O |
您最近半年使用:0次