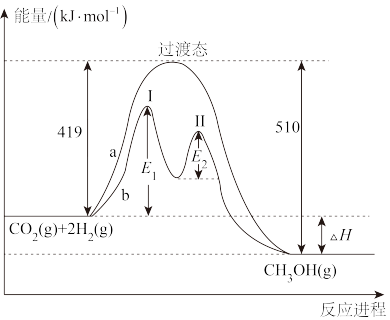
下列说法正确的是( )
| A.化学反应的热效应的大小与参加反应的物质的多少无关 |
| B.由H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,则向含0.1 mol HCl的盐酸中加入4.0 gNaOH固体,放出热量等于5.73 kJ |
| C.同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同 |
| D.反应物的总能量大于生成物的总能量的反应一定是放热反应 |
更新时间:2020-09-14 08:38:40
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】已知断开 1mol Cl2(g)中Cl-Cl键需要吸收243kJ能量,根据能量变化示意图,下列说法或热化学方程式正确的是
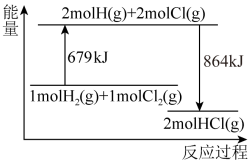

| A.H2(g)+Cl2(g) = 2HCl(g) ΔH= + 185 kJ·mol-1 |
| B.生成1mol H2(g)中的H-H键放出 121.5 kJ 能量 |
| C.断开1mol HCl(g)中的H-C1键要吸收 864 kJ 能量 |
D.HCl(g) = H2(g)+ H2(g)+ Cl2(g) ΔH= + 92.5kJ·mol-1 Cl2(g) ΔH= + 92.5kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】CH4和CO2在一定条件下能发生反应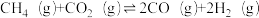 ,该反应过程中能量变化趋势如图,下列说法正确的是
,该反应过程中能量变化趋势如图,下列说法正确的是
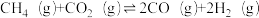 ,该反应过程中能量变化趋势如图,下列说法正确的是
,该反应过程中能量变化趋势如图,下列说法正确的是
A.甲烷的分子结构模型为 |
| B.该反应过程中有非极性键的断裂和生成 |
| C.提高反应时的温度,可以实现CH4的完全转化 |
| D.该反应中反应物断键吸收的总能量大于生成物成键放出的总能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知:分解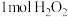 放出热量98kJ。常温下在含有少量
放出热量98kJ。常温下在含有少量 的溶液中,
的溶液中, 的分解机理为:
的分解机理为:
① 慢;②H2O2+IO-→H2O+O2+I- 快
慢;②H2O2+IO-→H2O+O2+I- 快
下列说法正确的是
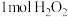 放出热量98kJ。常温下在含有少量
放出热量98kJ。常温下在含有少量 的溶液中,
的溶液中, 的分解机理为:
的分解机理为:①
 慢;②H2O2+IO-→H2O+O2+I- 快
慢;②H2O2+IO-→H2O+O2+I- 快下列说法正确的是
A.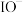 是该反应的催化剂 是该反应的催化剂 | B.反应的活化能不一定等于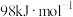 |
C.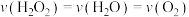 | D.上述过程中 分解的快慢由反应②决定 分解的快慢由反应②决定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】可逆反应A(g)+B(g)  C(g) +D(g)在反应过程中的能量变化如图所示,下列叙述不正确的是
C(g) +D(g)在反应过程中的能量变化如图所示,下列叙述不正确的是
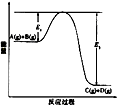
 C(g) +D(g)在反应过程中的能量变化如图所示,下列叙述不正确的是
C(g) +D(g)在反应过程中的能量变化如图所示,下列叙述不正确的是
| A.该反应是放热反应 |
| B.向反应体系中加入催化剂对反应热无影响 |
| C.向反应体系中加入催化剂,E1减小,E2增大 |
| D.该反应ΔH=-(E2-E1)kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】已知反应H2(g)+Br2(g) 2HBr(g)分下列三步进行,有关键能如下表所示:
2HBr(g)分下列三步进行,有关键能如下表所示:
①Br2 2Br(快反应) △H1,K1
2Br(快反应) △H1,K1
②Br+H2 HBr+H(慢反应) △H2,K2
HBr+H(慢反应) △H2,K2
③H+Br HBr(快反应) △H3,K3
HBr(快反应) △H3,K3
则下列说法错误的是
 2HBr(g)分下列三步进行,有关键能如下表所示:
2HBr(g)分下列三步进行,有关键能如下表所示:化学键 | 键能 |
H—H | 436 kJ/mol |
Br—Br | 200 kJ/mol |
H—Br | 369 kJ/mol |
 2Br(快反应) △H1,K1
2Br(快反应) △H1,K1②Br+H2
 HBr+H(慢反应) △H2,K2
HBr+H(慢反应) △H2,K2③H+Br
 HBr(快反应) △H3,K3
HBr(快反应) △H3,K3则下列说法错误的是
| A.△H1>△H2>△H3 |
| B.25℃时:K1>K3 |
C.H2(g)+Br2(g) 2HBr(g)的速率由反应②的速率决定 2HBr(g)的速率由反应②的速率决定 |
D.H2(g)+Br2(g) 2HBr(g) △H<0 2HBr(g) △H<0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
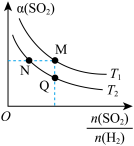
【推荐1】可用水煤气还原法处理 ,其中一个反应为
,其中一个反应为
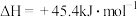 。在一定压强下发生该反应,平衡时
。在一定压强下发生该反应,平衡时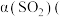 二氧化硫的转化率
二氧化硫的转化率 与原料气投料比
与原料气投料比 和温度
和温度 的关系如图所示。下列说法不正确的是
的关系如图所示。下列说法不正确的是
 ,其中一个反应为
,其中一个反应为
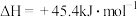 。在一定压强下发生该反应,平衡时
。在一定压强下发生该反应,平衡时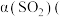 二氧化硫的转化率
二氧化硫的转化率 与原料气投料比
与原料气投料比 和温度
和温度 的关系如图所示。下列说法不正确的是
的关系如图所示。下列说法不正确的是 
A.正反应的活化能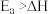 | B. : : |
C.逆反应速率: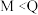 | D.增大压强,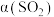 增大 增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在烃分子中去掉2个H原子形成一个双键是吸热反应,大约需117 kJ热量。但1,3-环己二烯失去2 个H原子变成苯是放热反应,反应热是-23.4 kJ·mol-1,以上事实表明
| A.1,3-环己二烯比苯稳定 |
| B.苯比1,3-环己二烯稳定 |
| C.1,3-环己二烯加氢是吸热反应 |
| D.苯加氢生成环己烷是吸热反应 |
您最近一年使用:0次

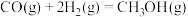 ,其两种反应过程中的能量变化曲线如图
,其两种反应过程中的能量变化曲线如图 所示,下列说法错误的是
所示,下列说法错误的是