U、V、W、X、Y、Z 是原子序数依次增大的六种常见元素,Y 的单质在W2中燃烧的产物可使品红溶液褪色。Z 的单质在W2中燃烧的产物Z3W4具有磁性。U 的单质在W2中燃烧可生成UW 和 UW2两种气体。X 的单质是一种金属,该金属在 UW2中剧烈燃烧生成黑、白两种固体。请回答下列问题:
(1)V 的单质分子的电子式为______ 。
(2)U 元素形成的具有空间网状结构的单质,高温使其熔化断裂的化学键类型是______ 。
(3)U、V、W 形成的 10 电子氢化物中,稳定性最强的是:______ (写化学式)。
(4)金属X在UW2中剧烈燃烧的反应方程式为______ ;Z3W4与稀硫酸反应的离子方程式为 ______ 。
(1)V 的单质分子的电子式为
(2)U 元素形成的具有空间网状结构的单质,高温使其熔化断裂的化学键类型是
(3)U、V、W 形成的 10 电子氢化物中,稳定性最强的是:
(4)金属X在UW2中剧烈燃烧的反应方程式为
更新时间:2020-09-23 17:14:56
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】前四周期元素X、Y、Z、W核电荷数依次增大,核电荷数之和为58;Y原子的M层p轨道有3个未成对电子;Z与Y同周期,且在该周期中电负性最大;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:2。
(1)写出Z元素在元素周期表中的位置:___________ 。
(2) 与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是
与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是___________  写分子式
写分子式 。
。
(3) 的最高价氧化物的水化物的化学式为
的最高价氧化物的水化物的化学式为___________ ;
(4) 单质
单质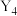 与
与 在一定条件下恰好完全反应生成
在一定条件下恰好完全反应生成 化合物C,一个C分子中所含有的σ键数目为
化合物C,一个C分子中所含有的σ键数目为___________ ;
(5)含W元素的最高化合价的含氧酸根离子是___________ ,该含氧酸根离子在分析化学中有重要作用,在酸性条件下该含氧酸根离子可将 氧化成
氧化成 ,请写出该反应的离子方程式
,请写出该反应的离子方程式___________ 。
(1)写出Z元素在元素周期表中的位置:
(2)
 与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是
与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是 写分子式
写分子式 。
。(3)
 的最高价氧化物的水化物的化学式为
的最高价氧化物的水化物的化学式为(4)
 单质
单质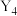 与
与 在一定条件下恰好完全反应生成
在一定条件下恰好完全反应生成 化合物C,一个C分子中所含有的σ键数目为
化合物C,一个C分子中所含有的σ键数目为(5)含W元素的最高化合价的含氧酸根离子是
 氧化成
氧化成 ,请写出该反应的离子方程式
,请写出该反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W、Y的氧化物是导致酸雨的主要物质,X的基态原子核外有7个原子轨道填充了电子,Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物。
(1)W位于元素周期表第________ 周期第________ 族。W的气态氢化物稳定性比H2O(g)________ (填“强”或“弱”)。
(2)Y的基态原子价层电子排布式为________________ ,Y的第一电离能比X的________ (填“大”或“小”)。
(3)Y的最高价氧化物对应水化物的浓溶液与Z的单质反应的化学方程式是
________________________________________________________________________ 。
(1)W位于元素周期表第
(2)Y的基态原子价层电子排布式为
(3)Y的最高价氧化物对应水化物的浓溶液与Z的单质反应的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】X、Y、Z、W四种元素在元素周期表中序数逐渐增大。X为非金属元素,且X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍。试推断:
(1)X、Y、Z的元素符号分别是:______ 、_______ 、________ 。
(2)画出Z的离子结构示意图__________ 。
(3)X、Y、Z的简单离子半径大小顺序为________________________________ 。
(4)用电子式表示W与Z形成化合物W2Z的过程____________________________ 。
(5)由X、Y、Z所形成的离子化合物是__________ ,它与W的最高价氧化物对应水化物的溶液加热时反应的离子方程式是________________________________ 。
(1)X、Y、Z的元素符号分别是:
(2)画出Z的离子结构示意图
(3)X、Y、Z的简单离子半径大小顺序为
(4)用电子式表示W与Z形成化合物W2Z的过程
(5)由X、Y、Z所形成的离子化合物是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】A~D为核电荷数小于18的元素,其性质或结构信息如下表:
请根据表中的信息回答下列问题:
(1)四种元素名称或符号为:A___________ ;B___________ ;C___________ ;D___________ ;
(2)B原子的结构示意图:___________ ;
(3)写出由A、B、D三种元素构成的物质在水中的电离方程式___________ ,D与硫元素形成的化合物的水溶液跟单质C的水溶液混合发生置换反应,其离子方程式为___________ ;
(4)有某AC的浓溶液,密度为1.19g/cm3,质量分数为36.5%,其物质的量浓度为___________ 。
| 元素 | A | B | C | D |
| 性质或结构信息 | 原子核内只有1个质子 | 海水中含量最多,其原子有2个电子层 | 其阴离子是构成食盐的粒子之一 | 其原子的M电子层上只有1个电子 |
(1)四种元素名称或符号为:A
(2)B原子的结构示意图:
(3)写出由A、B、D三种元素构成的物质在水中的电离方程式
(4)有某AC的浓溶液,密度为1.19g/cm3,质量分数为36.5%,其物质的量浓度为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】现有部分前四周期元素的性质或原子结构如下表:
(1)T在周期表中的位置为___________ ,基态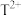 的核外电子排布式为
的核外电子排布式为_____________ ;T的单质在高温下与X的氢化物反应,其化学方程式为____________________________________________ 。
(2)基态Z原子中,核外电子占据的最高能级的符号是______________ ,占据最高能级的电子的电子云形状为______________ 。
(3)W、X、Y三种元素的离子半径由大到小的顺序是______________ (用离子符号表示)。
(4)在W、X的气态氢化物中,较稳定的是__________________________________________ 。
元素编号 | 元素性质或原子结构 |
W | 单质能与水剧烈反应,所得溶液呈弱酸性 |
X | 基态原子的s轨道与p轨道电子数相等 |
Y | 第三周期元素的简单离子中半径最小 |
Z | L层有三个未成对电子 |
T | 该元素的正三价离子的3d能级为半充满 |
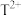 的核外电子排布式为
的核外电子排布式为(2)基态Z原子中,核外电子占据的最高能级的符号是
(3)W、X、Y三种元素的离子半径由大到小的顺序是
(4)在W、X的气态氢化物中,较稳定的是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】科学家合成一种新化合物(如图所示)。其中W、X、Y、Z为短周期元素,且位于同一周期,W是所在周期中第一电离能最小的元素,Y元素基态原子的未成对电子数等于其电子层数,Z元素的原子核外最外层电子数是X元素原子核外电子数的一半。回答下列问题:
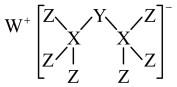
(1)W、X、Y、Z原子半径由大到小的顺序为
(2)Z的核外电子排布式为
(3)基态X原子价电子轨道表示式为
(4)W元素基态原子核外电子有
(5)X的电负性
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】I.实验室需要0.5 mol∙L−1CuSO4溶液450mL和0.5 mol∙L−1硫酸溶液500mL,根据这两种溶液的配制情况回答下列问题:
(1)配制CuSO4溶液时,如果用CuSO4固体,应该称量固体的质量为___________ ;配制硫酸溶液时,需要取质量分数为98%、密度为1.84 g∙cm−3的浓硫酸的体积为___________ 。
(2)下列操作对溶液的浓度有何影响?(填“偏大”、“偏小”、“无影响”)
①配制的过程中有少量的液体迸溅出来___________
②定容时俯视刻度线___________ 。
Ⅱ.A、B、C、D、E是五种短周期的主族元素,它们的原子序数依次增大,C原子最外层电子数是电子层数的3倍,E和C同主族,A、B组成的气态化合物的水溶液呈碱性,D与C能按原子个数比为1:1或2:1形成离子化合物。
(1)A与C形成的化合物中,原子个数比为2:1的化合物的结构式为___________ ,此化合物中含有的化学键为___________ 。
(2)D与C按原子个数比为1:1形成化合物的电子式是___________ 。
(1)配制CuSO4溶液时,如果用CuSO4固体,应该称量固体的质量为
(2)下列操作对溶液的浓度有何影响?(填“偏大”、“偏小”、“无影响”)
①配制的过程中有少量的液体迸溅出来
②定容时俯视刻度线
Ⅱ.A、B、C、D、E是五种短周期的主族元素,它们的原子序数依次增大,C原子最外层电子数是电子层数的3倍,E和C同主族,A、B组成的气态化合物的水溶液呈碱性,D与C能按原子个数比为1:1或2:1形成离子化合物。
(1)A与C形成的化合物中,原子个数比为2:1的化合物的结构式为
(2)D与C按原子个数比为1:1形成化合物的电子式是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】下表是元素周期表中前四周期的部分元素,表中所列字母分别代表一种元素。
回答下列问题:
(1)i在元素周期表中的位置是__________ 。
(2)a、e、g、l形成的简单离子其半径由大到小的顺序为__________ (填写离子符号)。
(3)n与o形成的化合物为__________ (填写化学式),将该化合物进行焰色试验,火焰呈__________ 色。
(4)用电子式表示g和m形成化合物的过程__________ 。
(5)将足量d的氢化物溶于水,再取少量 的水溶液滴入其中,反应的离子方程式为
的水溶液滴入其中,反应的离子方程式为__________ 。
(6)某同学欲探究元素性质递变规律与原子结构的关系,进行如下实验:
实验操作:取已除去氧化膜且表面积相等的镁条和铝条,分别投入 盐酸中。
盐酸中。
实验现象:镁与盐酸反应比铝更剧烈。
①比较金属性:
______  (选填“>”或“<”);
(选填“>”或“<”);
②利用元素周期律对上述实验结论进行解释__________ 。
(7)向 的碱性溶液中通入m单质,可得到
的碱性溶液中通入m单质,可得到 ,反应的离子方程式为:
,反应的离子方程式为:__________ 。
a | b | |||||||
c | d | e | f | |||||
g | h | i | j | k | l | m | ||
o | n | |||||||
(1)i在元素周期表中的位置是
(2)a、e、g、l形成的简单离子其半径由大到小的顺序为
(3)n与o形成的化合物为
(4)用电子式表示g和m形成化合物的过程
(5)将足量d的氢化物溶于水,再取少量
 的水溶液滴入其中,反应的离子方程式为
的水溶液滴入其中,反应的离子方程式为(6)某同学欲探究元素性质递变规律与原子结构的关系,进行如下实验:
实验操作:取已除去氧化膜且表面积相等的镁条和铝条,分别投入
 盐酸中。
盐酸中。实验现象:镁与盐酸反应比铝更剧烈。
①比较金属性:

 (选填“>”或“<”);
(选填“>”或“<”);②利用元素周期律对上述实验结论进行解释
(7)向
 的碱性溶液中通入m单质,可得到
的碱性溶液中通入m单质,可得到 ,反应的离子方程式为:
,反应的离子方程式为:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如表:
(1)X和W的元素符号分别为___ 、___ 。
(2)X与Y形成的原子个数比为2∶1的化合物中,Y原子最外层为8电子结构,请写出该化合物的电子式___ ,工业合成Y的氢化物的化学方程式为___ 。
(3)X和Z组成的化合物中,既含有极性共价键又含有非极性共价键的是___ 。此化合物还可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为___ 。
| 元素 | 相关信息 |
| X | X的单质为密度最小的气体 |
| Y | Y的氢化物的水溶液呈碱性 |
| Z | Z是地壳中含量最高的元素 |
| W | W的一种核素的质量数为35,中子数为18 |
(2)X与Y形成的原子个数比为2∶1的化合物中,Y原子最外层为8电子结构,请写出该化合物的电子式
(3)X和Z组成的化合物中,既含有极性共价键又含有非极性共价键的是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】有A、B、C、D、E五种元素,元素A的一种原子无中子,B位于第二周期第IVA族,C位于第二周期第VIA族,B、C能形成无色无味的气体BC2,元素D有三个电子层,它和元素C属于同一主族,D和C形成有刺激性气味的气体DC2;元素E的阳离子E+的电子层结构与Ar的电子层结构相同,试回答:
(1)它们的元素符号是:A__ ;B___ ;C__ ;D__ ;E__ 。
(2)A与B形成的化合物以___ 键结合,C和E的化合物以__ 键结合。
(3)BC2的结构式为___ ;C和E形成的化合物E2C其电子式为:___ 。
(1)它们的元素符号是:A
(2)A与B形成的化合物以
(3)BC2的结构式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】已知A、B、C、D、E、F为周期表前四周期原子序数依次增大的六种元素。其中A是元素周期表中原子半径最小的元素,B原子最外层电子数是内层电子数的2倍。D、E为同主族元素,且E的原子序数为D的2倍。F元素在地壳中含量位于金属元素的第二位。试回答下列问题:
(1)F元素价层电子排布式为___________________ 。
(2)关于B2A2的下列说法中正确的是________________ 。
A.B2A2中的所有原子都满足8电子结构
B.每个B2A2分子中σ键和π键数目比为1∶1
C.B2A2是由极性键和非极性键形成的非极性分子
D.B2A2分子中的B-A键属于s—spσ键
(3) B和D形成的一种三原子分子与C和D形成的一种化合物互为等电子体,则满足上述条件的B和D形成的化合物的空间构型是________________ 。
(4) C元素原子的第一电离能比B、D两元素原子的第一电离能高的主要原因__________ 。
(5) A与D可以形成原子个数比分别为2∶1,1∶1的两种化合物X和Y,其中 Y含有____________ 键(填“极性键”“非极性键”),A与C组成的两种化合物M和N所含的电子数分别与X、Y相 等,N的 结构式为________ 。
(6) E的氢化物的价层电子对互斥理论模型为________ ,E 原子的杂化方式为________ 杂化。
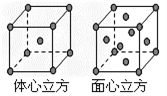
(7) F单质的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示。面心立方晶胞和体心立方晶胞的棱边长分别为acm、bcm,则F单质的面心立方晶胞和体心立方晶胞的密度之比为_________ ,F原子配位数之比为__________________ 。
(1)F元素价层电子排布式为
(2)关于B2A2的下列说法中正确的是
A.B2A2中的所有原子都满足8电子结构
B.每个B2A2分子中σ键和π键数目比为1∶1
C.B2A2是由极性键和非极性键形成的非极性分子
D.B2A2分子中的B-A键属于s—spσ键
(3) B和D形成的一种三原子分子与C和D形成的一种化合物互为等电子体,则满足上述条件的B和D形成的化合物的空间构型是
(4) C元素原子的第一电离能比B、D两元素原子的第一电离能高的主要原因
(5) A与D可以形成原子个数比分别为2∶1,1∶1的两种化合物X和Y,其中 Y含有
(6) E的氢化物的价层电子对互斥理论模型为
(7) F单质的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示。面心立方晶胞和体心立方晶胞的棱边长分别为acm、bcm,则F单质的面心立方晶胞和体心立方晶胞的密度之比为

您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】下表为元素周期表的一部分,针对表中①~⑧元素填空,回答相关问题。
(1)化学性质最稳定的是_______ (填元素符号)。
(2)原子半径最大的是_______ (填元素符号);离子半径最大的是_______ (填离子符号);得电子能力最强的是_______ (填元素符号)。
(3)④⑤形成的化合物中,含有非极性共价键的化合物的电子式为_______ 。
(4)⑧单质与⑤最高价氧化物的水化物反应制得84消毒液的离子方程式为_______ 。
(5)③④两种元素组成的某化合物,常温下是一种红棕色气体,该气体与水发生反应的化学方程式为_______ 。
(6)比较②和⑦两种元素得电子能力强弱,其简单实验方案是_______ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 |
| 一 | ① | ||||||
| 二 | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)原子半径最大的是
(3)④⑤形成的化合物中,含有非极性共价键的化合物的电子式为
(4)⑧单质与⑤最高价氧化物的水化物反应制得84消毒液的离子方程式为
(5)③④两种元素组成的某化合物,常温下是一种红棕色气体,该气体与水发生反应的化学方程式为
(6)比较②和⑦两种元素得电子能力强弱,其简单实验方案是
您最近一年使用:0次



