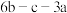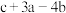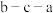2SO2(g)+O2(g) 2SO3(g)反应过程中的能量变化如图所示(图中E1表示无催化剂时正反应的活化能,E2表示无催化剂时逆反应的活化能)。下列有关叙述
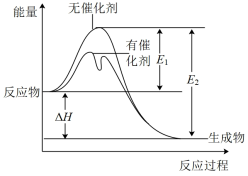
2SO3(g)反应过程中的能量变化如图所示(图中E1表示无催化剂时正反应的活化能,E2表示无催化剂时逆反应的活化能)。下列有关叙述不正确 的是( )
 2SO3(g)反应过程中的能量变化如图所示(图中E1表示无催化剂时正反应的活化能,E2表示无催化剂时逆反应的活化能)。下列有关叙述
2SO3(g)反应过程中的能量变化如图所示(图中E1表示无催化剂时正反应的活化能,E2表示无催化剂时逆反应的活化能)。下列有关叙述
| A.该反应的逆反应为吸热反应,升高温度可提高活化分子的百分数 |
| B.该反应中,反应物的总键能大于生成物的总键能 |
| C.ΔH=E1-E2 |
| D.使用催化剂改变活化能,但不改变反应的焓变 |
20-21高二上·湖北·阶段练习 查看更多[6]
湖北省部分重点中学(郧阳中学、恩施高中、随州二中、沙市中学)2020-2021学年高二上学期联考化学试题湖北省麻城实验高中2020-2021学年高二上学期12月月考化学试题(已下线)练习1 反应热 热化学方程式-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)广东省化州市第一中学2020-2021学年高二上学期10月月考化学试题广西桂林市第十八中学2022-2023学年高二上学期期中考试化学试题广西防城港市实验高级中学2023-2024学年高二上学期期中考试化学试题
更新时间:2020-09-24 11:34:25
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】化学反应的吸热和放热对生产和生活具有重要意义。下列变化中,属于放热反应的是
| A.碳酸氢钠与盐酸反应 | B.生石灰与水混合 |
| C.碳与水蒸气反应制备水煤气 | D.煅烧石灰石 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列说法正确的是
①离子化合物中含离子键,也可能含共价键
②共价化合物中含共价键,也可能含离子键
③含金属元素的化合物不一定是离子化合物
④任何物质中含有化学键
⑤常温下能发生的反应一定是放热反应
①离子化合物中含离子键,也可能含共价键
②共价化合物中含共价键,也可能含离子键
③含金属元素的化合物不一定是离子化合物
④任何物质中含有化学键
⑤常温下能发生的反应一定是放热反应
| A.②③④ | B.②④⑤ | C.①③ | D.①③⑤ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】键能是指断裂1 mol化学键形成气态原子时吸收的能量(kJ),单位为kJ·mol-1。从手册上查得:H—H、Cl—Cl和H—Cl的键能分别为436 kJ·mol-1、243 kJ·mol-1和431 kJ·mol-1,请用此数据估计由Cl2、H2生成1 mol HCl时应该
| A.放热183 kJ | B.放热91.5 kJ | C.吸热183 kJ | D.吸热91.5 kJ |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】已知反应: N2(g) +3H2(g)  2NH3(g),其中1mol H-H键断裂吸收436kJ的能量,1molN-H键断裂吸收391kJ的能量,1mol N≡ N键断裂吸收946kJ的能量,则生成2molNH3需
2NH3(g),其中1mol H-H键断裂吸收436kJ的能量,1molN-H键断裂吸收391kJ的能量,1mol N≡ N键断裂吸收946kJ的能量,则生成2molNH3需
 2NH3(g),其中1mol H-H键断裂吸收436kJ的能量,1molN-H键断裂吸收391kJ的能量,1mol N≡ N键断裂吸收946kJ的能量,则生成2molNH3需
2NH3(g),其中1mol H-H键断裂吸收436kJ的能量,1molN-H键断裂吸收391kJ的能量,1mol N≡ N键断裂吸收946kJ的能量,则生成2molNH3需| A.吸收能量92kJ | B.放出能量92kJ |
| C.放出能量30. 67kJ | D.吸收能量30.67kJ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
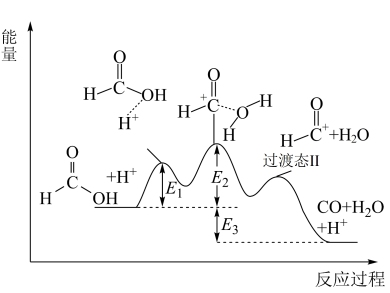
【推荐1】已知甲酸分解反应:HCOOH(aq)  CO(g)+H2O(l) ΔH。根据过渡态理论,在H+催化作用下反应过程中的能量变化如图(其中E1、E2、E3均大于0)。下列说法错误的是
CO(g)+H2O(l) ΔH。根据过渡态理论,在H+催化作用下反应过程中的能量变化如图(其中E1、E2、E3均大于0)。下列说法错误的是
 CO(g)+H2O(l) ΔH。根据过渡态理论,在H+催化作用下反应过程中的能量变化如图(其中E1、E2、E3均大于0)。下列说法错误的是
CO(g)+H2O(l) ΔH。根据过渡态理论,在H+催化作用下反应过程中的能量变化如图(其中E1、E2、E3均大于0)。下列说法错误的是
| A.E2为正反应的最高活化能 |
| B.该反应为放热反应ΔH=E3 |
C.生成过渡态Ⅰ的反应方程式: 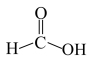 +H+ +H+ 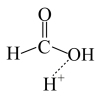 |
| D.使用催化剂后正逆反应速率同等程度改变平衡不移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】反应A(g)+B(g)→C(g)△H,分两步进行:①A(g)+B(g)→X(g)△H1②X(g)→C(g)△H2,反应过程中能量变化如图所示,E1表示A+B→X的活化能,下列说法正确的是
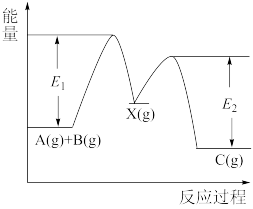

| A.△H1=△H-△H2 >0 | B.X是反应A(g)+B(g)→C(g)的催化剂 |
| C.E2是反应②的活化能 | D.△H = E1-E2 |
您最近一年使用:0次