变量控制方法是研究化学变化规律的重要思想方法。请仔细观察下表中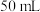 稀盐酸和
稀盐酸和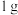 碳酸钙反应的实验数据:
碳酸钙反应的实验数据:
分析上述数据,回答下列问题:
(1)该反应属于____________________ 反应(填“吸热”或“放热”)。
(2)实验6和7表明,____________ 对反应速率有影响,__________________ ,反应速率越大。
(3)根据实验1、3、4、6可以得出外界条件对反应速率的影响规律是___________________________________________ 。
(4)该实验中影响反应速率的因素还有__________________________________________________ ,能表明这一规律的实验序号是1和2与__________________________________________________ 。
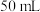 稀盐酸和
稀盐酸和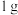 碳酸钙反应的实验数据:
碳酸钙反应的实验数据:| 实验序号 | 碳酸钙状态 | 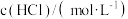 | 溶液温度/℃ | 碳酸钙消失所用的时间/s | |
| 反应前 | 反应后 | ||||
| 1 | 粒状 |  | 20 | 39 | 400 |
| 2 | 粉末 |  | 20 | 40 | 60 |
| 3 | 粒状 | 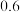 | 20 | 41 | 280 |
| 4 | 粒状 |  | 20 | 40 | 200 |
| 5 | 粉末 |  | 20 | 40 | 30 |
| 6 | 粒状 |  | 20 | 40 | 120 |
| 7 | 粒状 |  | 30 | 50 | 40 |
(1)该反应属于
(2)实验6和7表明,
(3)根据实验1、3、4、6可以得出外界条件对反应速率的影响规律是
(4)该实验中影响反应速率的因素还有
更新时间:2020-09-24 19:37:07
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】“绿水青山就是金山银山”,研究 、CO等大气污染物处理对建设美丽中国具有重要意义。
、CO等大气污染物处理对建设美丽中国具有重要意义。
(1)氨气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和 ,在一定条件下发生反应:
,在一定条件下发生反应: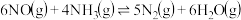 。
。
①能说明该反应已达到平衡状态的标志是_______ 。
A.反应速率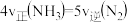
B.容器内压强不再随时间而发生变化
C.容器内气体的密度不再发生变化
D.容器内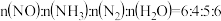
E.容器内气体的平均相对分子质量不再改变
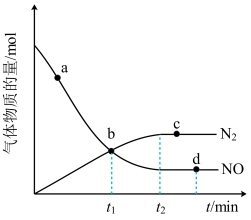
②某次实验中测得容器内NO及 的物质的量随时间变化如图所示,图中b点对应的速率关系是v(正)
的物质的量随时间变化如图所示,图中b点对应的速率关系是v(正)_______ v(逆);d点对应的速率关系是v(正)_______ v(逆)。(填>、<或=)。
(2)一定条件下,在2L密闭容器内,反应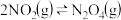 ,
,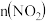 随时间变化如下表:
随时间变化如下表:
①用 表示0~2s内该反应的平均速率为
表示0~2s内该反应的平均速率为_______ 。在第5s时, 的转化率为
的转化率为_______ 。
②根据上表可以看出,随着反应进行,反应速率逐渐减小,其原因是_______ 。
 、CO等大气污染物处理对建设美丽中国具有重要意义。
、CO等大气污染物处理对建设美丽中国具有重要意义。(1)氨气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和
 ,在一定条件下发生反应:
,在一定条件下发生反应: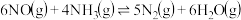 。
。①能说明该反应已达到平衡状态的标志是
A.反应速率
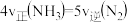
B.容器内压强不再随时间而发生变化
C.容器内气体的密度不再发生变化
D.容器内
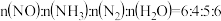
E.容器内气体的平均相对分子质量不再改变
②某次实验中测得容器内NO及
 的物质的量随时间变化如图所示,图中b点对应的速率关系是v(正)
的物质的量随时间变化如图所示,图中b点对应的速率关系是v(正)
(2)一定条件下,在2L密闭容器内,反应
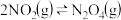 ,
,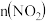 随时间变化如下表:
随时间变化如下表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
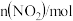 | 0.40 | 0.20 | 0.10 | 0.05 | 0.05 | 0.05 |
 表示0~2s内该反应的平均速率为
表示0~2s内该反应的平均速率为 的转化率为
的转化率为②根据上表可以看出,随着反应进行,反应速率逐渐减小,其原因是
您最近一年使用:0次
填空题
|
适中
(0.64)
名校
【推荐2】某课外兴趣小组对H2O2的分解速率做了如下实验探究。
⑴ 下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:
用10mL H2O2制取150mLO2所需的时间(秒)
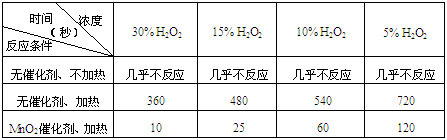
① 该小组在设计方案时,考虑了浓度、a: 、b: 等因素对过氧化氢分解速率的影响。
② 从上述影响H2O2分解速率的因素a和b中任选一个,说明该因素对该反应速率的影响:
。
⑵ 将质量相同但聚集状态不同的MnO2分别加入到5mL 5%的双氧水中,并用带火星的木
条测试。测定结果如下:
① 写出H2O2发生的化学反应方程式 _______________ ______。
② 实验结果说明催化剂作用的大小与________ _________有关。
⑴ 下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:
用10mL H2O2制取150mLO2所需的时间(秒)

① 该小组在设计方案时,考虑了浓度、a: 、b: 等因素对过氧化氢分解速率的影响。
② 从上述影响H2O2分解速率的因素a和b中任选一个,说明该因素对该反应速率的影响:
。
⑵ 将质量相同但聚集状态不同的MnO2分别加入到5mL 5%的双氧水中,并用带火星的木
条测试。测定结果如下:
| 催化剂(MnO2) | 操作情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 混合不振荡 | 剧烈反应,带火星的木条复燃 | 3.5分钟 |
| 块状 | 反应较慢,火星红亮但木条未复燃 | 30分钟 |
① 写出H2O2发生的化学反应方程式 _______________ ______。
② 实验结果说明催化剂作用的大小与________ _________有关。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某小组利用H2C2O4溶液和酸性KMnO4溶液(H2SO4酸化)反应来探究“外界条件对化学反应速率的影响”。该小组欲通过测定单位时间内生成CO2的体积来判断反应的快慢。设计实验方案如下:
(1)已知反应后H2C2O4转化为CO2逸出, 转化为Mn2+,写出该反应的离子方程式
转化为Mn2+,写出该反应的离子方程式______________ ;每消耗1 molH2C2O4,则反应中转移________________ mol电子。
(2)探究浓度对化学反应速率影响的实验编号是_________ ,实验②、③探究_________ 对化学反应速率影响。本实验还可通过测定____________ 来比较化学反应速率。
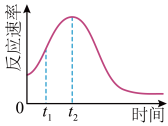
(3)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:a、该反应放热,使体系温度升高;b、____________ 。
(4)若实验①在5 min末收集49.0 mLCO2气体,则在5 min末,c( )=
)=_______ mol•L-1。(已知25℃时,气体摩尔体积Vm=24.5 L• mol-1)
| 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度℃ | ||
| 浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | 体积/mL | ||
| ① | 0.10 | 20 | 0.10 | 30 | 25 |
| ② | 0.20 | 20 | 0.10 | 30 | 25 |
| ③ | 0.20 | 20 | 0.10 | 30 | 50 |
 转化为Mn2+,写出该反应的离子方程式
转化为Mn2+,写出该反应的离子方程式(2)探究浓度对化学反应速率影响的实验编号是
(3)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:a、该反应放热,使体系温度升高;b、

(4)若实验①在5 min末收集49.0 mLCO2气体,则在5 min末,c(
 )=
)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在一定条件下,反应A(g)+B(g)  C(g)(正反应为放热反应)达到平衡后,根据下列图像判断:
C(g)(正反应为放热反应)达到平衡后,根据下列图像判断:
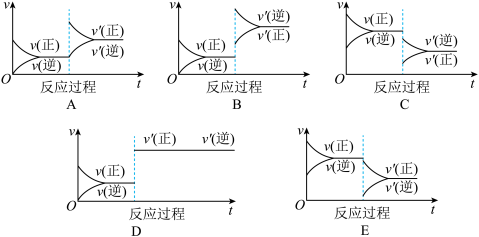
(1)升温,达到新平衡的是________ ,新平衡中C的体积分数________ (填“增大”、“减小”或“不变”,下同)。
(2)降压,达到新平衡的是________ ,A的转化率________ 。
(3)减少C的量,达到新平衡的是_______ 。
(4)增加A的量,达到新平衡的是____ ,此时B的转化率________ ,A的转化率________ 。
(5)使用催化剂,达到平衡的是________ , C的质量分数________ 。
 C(g)(正反应为放热反应)达到平衡后,根据下列图像判断:
C(g)(正反应为放热反应)达到平衡后,根据下列图像判断:
(1)升温,达到新平衡的是
(2)降压,达到新平衡的是
(3)减少C的量,达到新平衡的是
(4)增加A的量,达到新平衡的是
(5)使用催化剂,达到平衡的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】“碘钟”实验中, 的反应速率可以用
的反应速率可以用 与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在
与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在 进行实验,得到的数据如下表:
进行实验,得到的数据如下表:
回答下列问题:
(1)该实验的目的是___________________________________ 。
(2)根据实验数据,推测显色时间
__________ 。
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间 的范围为
的范围为__________ (填字母)。
a. <22.0s b.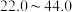 s c. >44.0s d. 数据不足,无法判断
s c. >44.0s d. 数据不足,无法判断
(4)通过分析比较上表数据,得到的结论是___________________________________ 。
 的反应速率可以用
的反应速率可以用 与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在
与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在 进行实验,得到的数据如下表:
进行实验,得到的数据如下表:| 实验编号 | ① | ② | ③ | ④ | ⑤ |
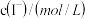 | 0.040 | 0.080 | 0.080 | 0.160 | 0.160 |
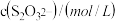 | 0.040 | 0.040 | 0.080 | 0.020 | 0.040 |
| t/s | 88.0 | 44.0 | 22.0 | 44.0 |  |
回答下列问题:
(1)该实验的目的是
(2)根据实验数据,推测显色时间

(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间
 的范围为
的范围为a. <22.0s b.
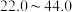 s c. >44.0s d. 数据不足,无法判断
s c. >44.0s d. 数据不足,无法判断(4)通过分析比较上表数据,得到的结论是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】2SO2(g)+O2(g) 2SO3(g) +Q ,是接触法生产硫酸的主要反应之一。
2SO3(g) +Q ,是接触法生产硫酸的主要反应之一。
完成下列填空:
(1)生产过程中温度控制在400℃~500℃,目的是__________________________________ ;该反应无需加压的原因是____________________________________________________ 。
(2)上述反应在密闭容器中达到化学平衡状态的标志为______________________________ 。
(3)上述反应的平衡常数表达式为__________________________________ ,随着温度升高,平衡常数__________________ (选填“增大”、“减小”或“不变”)。
(4)接触法生产硫酸尾气中含有SO2,可以采用氨水吸收,生成(NH4)2SO3与NH4HSO3的混合溶液。反应所得(NH4)2SO3又可以将NO2转化为N2和(NH4)2SO4。
① 写出生成NH4HSO3的化学方程式__________________________________________ 。
② 书写NO2与(NH4)2SO3反应的化学方程式,标出该反应中电子转移的方向和数目__________________________________ 。
 2SO3(g) +Q ,是接触法生产硫酸的主要反应之一。
2SO3(g) +Q ,是接触法生产硫酸的主要反应之一。完成下列填空:
(1)生产过程中温度控制在400℃~500℃,目的是
(2)上述反应在密闭容器中达到化学平衡状态的标志为
(3)上述反应的平衡常数表达式为
(4)接触法生产硫酸尾气中含有SO2,可以采用氨水吸收,生成(NH4)2SO3与NH4HSO3的混合溶液。反应所得(NH4)2SO3又可以将NO2转化为N2和(NH4)2SO4。
① 写出生成NH4HSO3的化学方程式
② 书写NO2与(NH4)2SO3反应的化学方程式,标出该反应中电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,同温度下涉及如下反应:
①2NO(g)+Cl2(g)⇌2ClNO(g) 平衡常数为K1;
②2NO2(g)+NaCl(s)⇌NaNO3(s)+ClNO(g) 平衡常数为K2。
(1)4NO2(g)+2NaCl(s)⇌2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=____ (用K1、K2表示)。
(2)若反应①在温度T下达到平衡时,平衡常数为K1,升高温度后K1增大,则正反应的焓变△H____ 0(填“>”、“<”或“=”)。若平衡后在其他条件不变的情况下,充入少量Cl2,Cl2的转化率___________ (填“变大”、“变小”或“不变”,下同),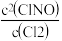 的值
的值___________ 。
Ⅱ.近年,科学家研究了乙醇催化合成乙酸乙酯的新方法:2C2H5OH(g) CH3COOC2H5(g)+2H2(g)在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图3所示。关于该方法,下列推测合理的是
CH3COOC2H5(g)+2H2(g)在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图3所示。关于该方法,下列推测合理的是________ 。
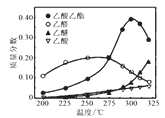
A.反应温度不宜超过300℃
B.增大体系压强,有利于提高乙醇平衡转化率
C.在催化剂作用下,乙醛是反应历程中的中间产物
D.提高催化剂的活性和选择性,减少乙醚、乙烯等副产物是工艺的关键
①2NO(g)+Cl2(g)⇌2ClNO(g) 平衡常数为K1;
②2NO2(g)+NaCl(s)⇌NaNO3(s)+ClNO(g) 平衡常数为K2。
(1)4NO2(g)+2NaCl(s)⇌2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=
(2)若反应①在温度T下达到平衡时,平衡常数为K1,升高温度后K1增大,则正反应的焓变△H
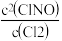 的值
的值Ⅱ.近年,科学家研究了乙醇催化合成乙酸乙酯的新方法:2C2H5OH(g)
 CH3COOC2H5(g)+2H2(g)在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图3所示。关于该方法,下列推测合理的是
CH3COOC2H5(g)+2H2(g)在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图3所示。关于该方法,下列推测合理的是
A.反应温度不宜超过300℃
B.增大体系压强,有利于提高乙醇平衡转化率
C.在催化剂作用下,乙醛是反应历程中的中间产物
D.提高催化剂的活性和选择性,减少乙醚、乙烯等副产物是工艺的关键
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】工业合成氨在一定条件下发生如下反应: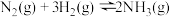 ,当进入合成塔的
,当进入合成塔的 和
和 的体积比为1:3时,经测定,在一定温度、压强和催化剂条件下所得氨的平衡浓度(体积分数)如下表所示:
的体积比为1:3时,经测定,在一定温度、压强和催化剂条件下所得氨的平衡浓度(体积分数)如下表所示:
而实际从合成塔出来的混合气体中含有氨约15%。
完成下列填空:
(1)目前公认的合成氨工业最恰当的催化剂是________ 。
a.酶 b.二氧化锰 c.铁触媒 d.五氧化二钒
(2)298K时合成氨,每生成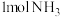 ,同时放出46.2kJ的热量。则该反应的热化学方程式为
,同时放出46.2kJ的热量。则该反应的热化学方程式为__________ ;该温度下,取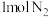 和
和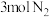 放在一密闭容器中,在催化剂条件下反应,测得反应放出的热量总小于92.4kJ,其原因是
放在一密闭容器中,在催化剂条件下反应,测得反应放出的热量总小于92.4kJ,其原因是________________________________ 。
(3)合成氨的温度和压强通常控制在约500℃以及20-50MPa的原因是_________________________________ 。
(4)实际上从合成塔出来的混合气体中氨的体积分数小于理论值的原因是________ 。
a.表中所测数据有明显误差 b.生成条件控制不当
c.氨的分解速率大于预测值 d.合成塔中的反应未达到平衡
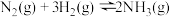 ,当进入合成塔的
,当进入合成塔的 和
和 的体积比为1:3时,经测定,在一定温度、压强和催化剂条件下所得氨的平衡浓度(体积分数)如下表所示:
的体积比为1:3时,经测定,在一定温度、压强和催化剂条件下所得氨的平衡浓度(体积分数)如下表所示:| 20MPa | 50MPa | |
| 500℃ | 19.1 | 42.2 |
而实际从合成塔出来的混合气体中含有氨约15%。
完成下列填空:
(1)目前公认的合成氨工业最恰当的催化剂是
a.酶 b.二氧化锰 c.铁触媒 d.五氧化二钒
(2)298K时合成氨,每生成
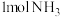 ,同时放出46.2kJ的热量。则该反应的热化学方程式为
,同时放出46.2kJ的热量。则该反应的热化学方程式为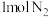 和
和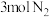 放在一密闭容器中,在催化剂条件下反应,测得反应放出的热量总小于92.4kJ,其原因是
放在一密闭容器中,在催化剂条件下反应,测得反应放出的热量总小于92.4kJ,其原因是(3)合成氨的温度和压强通常控制在约500℃以及20-50MPa的原因是
(4)实际上从合成塔出来的混合气体中氨的体积分数小于理论值的原因是
a.表中所测数据有明显误差 b.生成条件控制不当
c.氨的分解速率大于预测值 d.合成塔中的反应未达到平衡
您最近一年使用:0次

 2Fe2(SO4)3+2H2O。由图1和图2判断使用硫杆菌的最佳条件为
2Fe2(SO4)3+2H2O。由图1和图2判断使用硫杆菌的最佳条件为


