元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M原子的最外层电子数与次外电子数之比为3∶4;N-与Ar原子电子层结构相同;X是短周期主族元素中原子半径最小的;Z是短周期主族元素中原子半径最大的;化合物XN常温下为气体。据此回答:
(1)N的最高价氧化物对应水化物的化学式是_______ 。
(2)Z与M形成的化合物水溶液显碱性,其原因是_______ (用离子方程式表示)。
(3)X与Y、X与M均可形成18电子分子,这两种分子在水溶液中反应可观察到的现象是_______ ,反应的化学方程式是_______ 。
(4)由X、Y、Z、M四种元素组成一种强酸的酸式盐,写出Ba(OH)2溶液中逐滴加入该盐溶液至中性的离子方程式_______ 。
(5)Y、Z、N形成的化合物的水溶液中离子浓度的大小顺序是_______ 。
(6)如图所示:
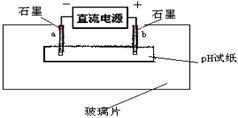
取一张用ZN溶液浸湿的pH试纸平铺在玻璃片上,取两根石墨棒做电极,接通直流电源。一段时间后,a电极处的pH试纸上可观察到的现象是_______ 。
(1)N的最高价氧化物对应水化物的化学式是
(2)Z与M形成的化合物水溶液显碱性,其原因是
(3)X与Y、X与M均可形成18电子分子,这两种分子在水溶液中反应可观察到的现象是
(4)由X、Y、Z、M四种元素组成一种强酸的酸式盐,写出Ba(OH)2溶液中逐滴加入该盐溶液至中性的离子方程式
(5)Y、Z、N形成的化合物的水溶液中离子浓度的大小顺序是
(6)如图所示:

取一张用ZN溶液浸湿的pH试纸平铺在玻璃片上,取两根石墨棒做电极,接通直流电源。一段时间后,a电极处的pH试纸上可观察到的现象是
2012·福建漳州·一模 查看更多[2]
更新时间:2016-12-09 03:14:23
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】A、B、M、D、E为短周期主族元素,且原子序数依次增大,质子数之和为39,B、M同周期,A、D同主族,A为短周期原子半径最小的元素,M原子最外层电子数为次外层的3倍,A、M常温下能形成两种液态化合物A2M和A2M2,E元素的周期数与主族序数相等。请用化学用语回答下列问题:
(1)B元素在周期表中的位置为_________ ;由A、M、D三种元素组成的化合物中含有的化学键为_________ ;A2M分子的空间结构为_________ ;
(2)用电子式表示D2M的形成过程_________
(3)D、E、M形成的简单离子半径从大到小的顺序为_________ (用离子符号表示)
(4)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2M2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出该反应的离子方程式___________ 。
(5)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,DA能与水反应放出氢气,且反应后的溶液呈碱性。若将0.1mol的DA和0.1mol的E单质混合后加入足量的水,充分反应后生成的气体在标准状况下的体积是___________ L。
(1)B元素在周期表中的位置为
(2)用电子式表示D2M的形成过程
(3)D、E、M形成的简单离子半径从大到小的顺序为
(4)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2M2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出该反应的离子方程式
(5)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,DA能与水反应放出氢气,且反应后的溶液呈碱性。若将0.1mol的DA和0.1mol的E单质混合后加入足量的水,充分反应后生成的气体在标准状况下的体积是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】A、B、C、D、E、F、G七种短周期元素的原子序数依次增大,其中仅有一种稀有气体元素.A和E最外层电子数相同,短周期主族元素的原子中,E原子的半径最大; B、C和F在周期表中相邻,B、C同周期,C、F同主族,F原子的质子数是C原子质子数的2倍;A和C可形成两种常见的液态化合物X和Y(相对分子质量X<Y ),D形成的分子为单原子分子.回答问题:
(1)Y的电子式为 ;
(2)液态化合物Y与稀H2SO4酸化的K2Cr2O7溶液作用可产生一种无色助燃性气体及可溶性的Cr2(SO4)3,则该反应的离子方程式为 ;
(3)用某种金属易拉罐与A、C、E组成的化合物的水溶液反应,产生的气体可充填气球,请写出该反应的离子方程式 ;
(4)P和Q两种物质都是由A、C、E、F四种元素组成的盐,其水溶液都显酸性,等物质的量的P和Q恰好完全反应.写出该反应的离子方程式 ,这两种盐均含有的化学键类型为 ;
(5)由A、B两元素形成的化合物W可作为火箭推进器中的强还原剂,已知一个W分子和一个Y分子中都含有18个电子,0.5mol液态W和足量液态Y反应,生成一种无色无味无毒的气体B2和液态X,并放出408.8KJ热量.写出该反应的热化学方程式为 .
(1)Y的电子式为 ;
(2)液态化合物Y与稀H2SO4酸化的K2Cr2O7溶液作用可产生一种无色助燃性气体及可溶性的Cr2(SO4)3,则该反应的离子方程式为 ;
(3)用某种金属易拉罐与A、C、E组成的化合物的水溶液反应,产生的气体可充填气球,请写出该反应的离子方程式 ;
(4)P和Q两种物质都是由A、C、E、F四种元素组成的盐,其水溶液都显酸性,等物质的量的P和Q恰好完全反应.写出该反应的离子方程式 ,这两种盐均含有的化学键类型为 ;
(5)由A、B两元素形成的化合物W可作为火箭推进器中的强还原剂,已知一个W分子和一个Y分子中都含有18个电子,0.5mol液态W和足量液态Y反应,生成一种无色无味无毒的气体B2和液态X,并放出408.8KJ热量.写出该反应的热化学方程式为 .
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
名校
【推荐3】Q、R、T、W四种短周期元素在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:
(1)T的原子结构示意图为_______ 。
(2)元素的非金属性为(原子的得电子能力):Q_______ W(填“强于”或“弱于”)。
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为_______ 。
(4)原子序数比R多1的元素的一种氢化物A能分解为其另一种氢化物B,写出A的电子式_____ 。
(5)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是___ 。
(6)在298K下,Q、T的单质各1mol完全燃烧,分别放出热量aKJ和bKJ。又知一定条件下,T的单质能将Q从它的最高价氧化物中置换出来,若此置换反应生成3molQ的单质,则该反应在298K下的△H =_______ kJ/mol(注:题中所设单质均为最稳定单质)
Q | R | ||
T | W |
(1)T的原子结构示意图为
(2)元素的非金属性为(原子的得电子能力):Q
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为
(4)原子序数比R多1的元素的一种氢化物A能分解为其另一种氢化物B,写出A的电子式
(5)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是
(6)在298K下,Q、T的单质各1mol完全燃烧,分别放出热量aKJ和bKJ。又知一定条件下,T的单质能将Q从它的最高价氧化物中置换出来,若此置换反应生成3molQ的单质,则该反应在298K下的△H =
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 3种原子最外层共有11个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素名称:
A_________ ,B_________ ,C________ ,D_______ ,E__________
(2)A与E两元素可形成化合物,用电子式表示其化合物的形成过程:_______________
(3)写出A的最高价氧化物对应水化物与B对应元素单质反应的化学方程式:__________________
(4)C、D、E的氢化物稳定性由强到弱依次为:(用化学式表示)_____________________
(1)写出下列元素名称:
A
(2)A与E两元素可形成化合物,用电子式表示其化合物的形成过程:
(3)写出A的最高价氧化物对应水化物与B对应元素单质反应的化学方程式:
(4)C、D、E的氢化物稳定性由强到弱依次为:(用化学式表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】如图是元素周期表的一部分。回答下列问题:
(1)世界上绝大部分卤素都存在于海洋中,海洋是卤素的资源宝库。
① 的离子结构示意图
的离子结构示意图___________ 。
②表中几种元素的最高价氧化物对应水化物酸性最强的是___________ (填化学式)。
③用电子式表示短周期元素中,原子半径最大的元素与氯形成的简单化合物的形成过程:___________ 。
④氰[(CN)2]是一种无色、可燃气体,剧毒、有苦杏仁味,与卤素单质的性质相似,试写出氰与NaOH溶液在常温下反应的离子方程式:___________ 。
(2)硒是人体必需的微量元素,起到抗氧化的作用。
①写出Se在周期表中的位置:___________ 。
② 溶于水生成
溶于水生成 ,向所得溶液中通入
,向所得溶液中通入 气体发生反应,生成Se和
气体发生反应,生成Se和 。写出
。写出 与
与 反应的化学方程式:
反应的化学方程式:___________ 。
(3)下列说法正确的是___________ (填字母)。
a.原子半径: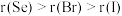
b.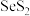 存在的化学键为极性共价键
存在的化学键为极性共价键
c.非金属性: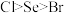
| 16 S 硫 32.06 | 17 Cl 氯 35.45 |
| 34 Se 硒 78.96 | 35 Br 溴 79.90 |
| 53 I 碘 126.9 |
①
 的离子结构示意图
的离子结构示意图②表中几种元素的最高价氧化物对应水化物酸性最强的是
③用电子式表示短周期元素中,原子半径最大的元素与氯形成的简单化合物的形成过程:
④氰[(CN)2]是一种无色、可燃气体,剧毒、有苦杏仁味,与卤素单质的性质相似,试写出氰与NaOH溶液在常温下反应的离子方程式:
(2)硒是人体必需的微量元素,起到抗氧化的作用。
①写出Se在周期表中的位置:
②
 溶于水生成
溶于水生成 ,向所得溶液中通入
,向所得溶液中通入 气体发生反应,生成Se和
气体发生反应,生成Se和 。写出
。写出 与
与 反应的化学方程式:
反应的化学方程式:(3)下列说法正确的是
a.原子半径:
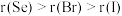
b.
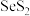 存在的化学键为极性共价键
存在的化学键为极性共价键c.非金属性:
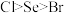
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下表是元素周期表的一部分,按要求回答下列问题:
(1)③的元素符号为__________ ,⑦的原子结构示意图为___________ ,⑨的单质的电子式为___________ 。
(2)①~⑨对应元素中,非金属性最强的是___________ (填元素符号,下同),金属性最强的是__________ ,单质的化学性质最不活泼的是__________ 。
(3)②③④三种元素对应的简单氢化物中最稳定的是__________ (填化学式,下同),⑥⑦两种元素的最高价氧化物对应水化物中,碱性最强的是__________ 。
(4)⑧的最高价氧化物对应水化物的化学式为____________ ,写出实验室制备②的简单氢化物的化学方程式____________ 。
| 族 周期 | ⅠA | ⅡA | Ⅲ | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ |
(1)③的元素符号为
(2)①~⑨对应元素中,非金属性最强的是
(3)②③④三种元素对应的简单氢化物中最稳定的是
(4)⑧的最高价氧化物对应水化物的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】右表为元素周期表的一部分。回答下列问题:
(1)Z的元素符号为_________________ 。
(2)X位于元素周期表第_______ 周期_______ 族。
(3)W与Y形成的化合物WY中,W的化合价是________ 。
(4)硫的最简单氢化物与硫的低价氧化物通入水中时,发生反应的化学方程式为_________________________ 。
| W | 氮 | Y | |
| X | 硫 | Z |
(1)Z的元素符号为
(2)X位于元素周期表第
(3)W与Y形成的化合物WY中,W的化合价是
(4)硫的最简单氢化物与硫的低价氧化物通入水中时,发生反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】X、Y、Z、W、Q 五种元素原子序数依次增大,X原子核外的L层电子数是K层的两倍,Z原子价电子排布式为nsnnp2n,W原子核外的M层中只有两对成对电子,Q的核电荷数是Z与W的核电荷数之和.请回答下列问题:
(1)Y、Q的元素符号依次为__ 、__ ;
(2)Y与Z的第一电离能大小关系是(用元素符号回答)__ ;
(3)X、Y、Z两两组合可形成很多等电子体,请任意写出两组等电子体__ 、__ ;
(4)Q在元素周期表 区,其价电子排布图为__ .
(5)X与W的电负性大小关系是(用元素符号回答)__ ,这两种元素组成的一种化合物是一种常见的溶剂,其电子式为__ .
(1)Y、Q的元素符号依次为
(2)Y与Z的第一电离能大小关系是(用元素符号回答)
(3)X、Y、Z两两组合可形成很多等电子体,请任意写出两组等电子体
(4)Q在元素周期表 区,其价电子排布图为
(5)X与W的电负性大小关系是(用元素符号回答)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】镁铝碱式碳酸盐MgaAlb(OH)c(CO3)d·xH2O是一种不溶于水的新型无机阻燃剂,其受热分解产物中的MgO、Al2O3熔点较高且都不燃烧,有阻燃作用。完成下列填空:
(1)组成镁铝碱式碳酸盐的三种非金属元素的原子半径从小到大的顺序是______________ 。碳原子最外层电子排布式是________________ ,铝原子核外有_________ 种能量不同的电子。
(2)将MgaAlb(OH)c (CO3)d·x H2O表示成氧化物的形式:2aMgO·bAl2O3·2dCO2·( ) H2O;
(3)焦炭与石英高温下在氮气流中发生如下反应,工业上可由此制得一种新型陶瓷材料氮化硅(Si3N4):3SiO2(s)+6C(s)+2N2(g) Si3N4(s)+6CO(g) + Q (Q>0)。
Si3N4(s)+6CO(g) + Q (Q>0)。
①该反应中,氧化产物是________________________ 。若测得反应生成4.48 L CO气体(标准状况下),则转移的电子的物质的量为_____________ 。
②该反应的平衡常数表达式K=_____________________________ ;若升高温度,K值____________ (填“增大”、“减小”或“不变”)。
③该反应的速率与反应时间的关系如右图所示,t4时刻引起正逆反应速率变化的原因是___________________________ (写出一种即可)。

(1)组成镁铝碱式碳酸盐的三种非金属元素的原子半径从小到大的顺序是
(2)将MgaAlb(OH)c (CO3)d·x H2O表示成氧化物的形式:2aMgO·bAl2O3·2dCO2·
(3)焦炭与石英高温下在氮气流中发生如下反应,工业上可由此制得一种新型陶瓷材料氮化硅(Si3N4):3SiO2(s)+6C(s)+2N2(g)
 Si3N4(s)+6CO(g) + Q (Q>0)。
Si3N4(s)+6CO(g) + Q (Q>0)。①该反应中,氧化产物是
②该反应的平衡常数表达式K=
③该反应的速率与反应时间的关系如右图所示,t4时刻引起正逆反应速率变化的原因是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据下列几种粒子的结构示意图,回答问题:
A.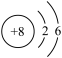 B.
B.  C.
C.  D.
D. 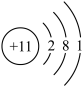
(1)其中属于阴离子的是________ ;(填字母序号,下同)
(2)具有相似化学性质的是________ 。
(3)C离子的结构示意图________ ;
(4)写出C与D形成化合物的化学式________ 。
A.
 B.
B.  C.
C.  D.
D. 
(1)其中属于阴离子的是
(2)具有相似化学性质的是
(3)C离子的结构示意图
(4)写出C与D形成化合物的化学式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】A、B、C、D四种元素的核电荷数依次增大且质子数均小于18。已知A的原子核外最外层电子数是次外层电子数的2倍,B的最外层电子数是内层电子总数的1/2,C原子的核外次外层电子数为8,最外层电子数为6。D是四种元素中质子数最大的,则:
(1)A、B、C、D的元素符号分别是__________ 、_________ 、________ 、__________ 。
(2)B原子结构示意图是_________________ ,C离子结构示意图是_________________ 。
(1)A、B、C、D的元素符号分别是
(2)B原子结构示意图是
您最近一年使用:0次



