X、Y、Z、W、Q 五种元素原子序数依次增大,X原子核外的L层电子数是K层的两倍,Z原子价电子排布式为nsnnp2n,W原子核外的M层中只有两对成对电子,Q的核电荷数是Z与W的核电荷数之和.请回答下列问题:
(1)Y、Q的元素符号依次为__ 、__ ;
(2)Y与Z的第一电离能大小关系是(用元素符号回答)__ ;
(3)X、Y、Z两两组合可形成很多等电子体,请任意写出两组等电子体__ 、__ ;
(4)Q在元素周期表 区,其价电子排布图为__ .
(5)X与W的电负性大小关系是(用元素符号回答)__ ,这两种元素组成的一种化合物是一种常见的溶剂,其电子式为__ .
(1)Y、Q的元素符号依次为
(2)Y与Z的第一电离能大小关系是(用元素符号回答)
(3)X、Y、Z两两组合可形成很多等电子体,请任意写出两组等电子体
(4)Q在元素周期表 区,其价电子排布图为
(5)X与W的电负性大小关系是(用元素符号回答)
更新时间:2018-12-24 21:28:05
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】元素周期表反映元素之间的内在联系,是研究物质性质的重要工具。如表是元素周期表的一部分,请回答下列问题:
(1)元素②、③、⑥的简单离子半径由大到小的排序为___________ (填离子符号)。
(2)②和④组成的物质中含有___________ 键,可以证明该化合物含有此类型化学键的实验事实为___________ 。
(3)⑤的氧化物和⑥的最高价氧化物对应的水化物反应的离子方程式为___________ 。
(4)已知④的单质与①的最高价氧化物A在点燃条件下能反应生成黑色单质,推测③的单质___________ (填“能”或“不能”)与A反应,说明推测的理由___________ 。
| 周期 | IA | 0 | |||||||
| 1 | IIA | … | IIIA | IVA | VA | VIA | VIIA | ||
| 2 | ① | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | |||||
(2)②和④组成的物质中含有
(3)⑤的氧化物和⑥的最高价氧化物对应的水化物反应的离子方程式为
(4)已知④的单质与①的最高价氧化物A在点燃条件下能反应生成黑色单质,推测③的单质
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有部分短周期元素的性质或原子结构如下表:
(1)写出元素X的离子结构示意图____________ 。
(2)写出Y元素最高价氧化物的水化物与NaOH溶液反应的离子方程式______________
(3)写出Y的价电子排布式_________________________ 。
(4)元素T与氯元素相比,非金属性较强的是_______ (用元素符号表示),下列表述中能用于证明这一事实的是_______ (填字母代号)。
A.气态氢化物的挥发性 B.两元素的电负性
C.含氧酸的酸性 D.氢化物中X—H键的键长(X代表T和Cl两种元素)
(5)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是___ (填元素符号)
| 元素编号 | 元素性质或原子结构 |
| T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| X | L层p电子数比s电子数多2个 |
| Y | 第三周期元素的简单离子中半径最小 |
| Z | L层有三个未成对电子 |
(1)写出元素X的离子结构示意图
(2)写出Y元素最高价氧化物的水化物与NaOH溶液反应的离子方程式
(3)写出Y的价电子排布式
(4)元素T与氯元素相比,非金属性较强的是
A.气态氢化物的挥发性 B.两元素的电负性
C.含氧酸的酸性 D.氢化物中X—H键的键长(X代表T和Cl两种元素)
(5)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】如表是元素周期表的一部分,回答下列有关问题。
(1)写出下列元素符号:①___________
(2)画出原子的结构示意图:④___________
(3)在①—⑫元素中,金属性最强的元素是___________ ,非金属性最强的元素是___________ ,最不活泼的元素是___________ 。(均填元素符号)
(4)第三周期中原子半径最大的元素是___________ (填序号),跟它同周期原子半径最小的元素是___________ (填序号),它们可以形成___________ (填“离子”或“共价”)化合物,用电子式表示其形成过程如下:___________ 。
(5)在①~⑩元素的最高价氧化物对应的水化物中,呈两性的是___________ 。写出其与另两种水溶液之间相互反应的离子方程式___________ ,___________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)画出原子的结构示意图:④
(3)在①—⑫元素中,金属性最强的元素是
(4)第三周期中原子半径最大的元素是
(5)在①~⑩元素的最高价氧化物对应的水化物中,呈两性的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据下表回答问题:
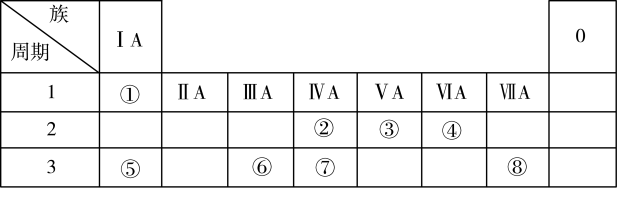
(1)元素⑦在周期表中的位置是___ 。
(2)元素①和⑤的原子序数相差___ 。
(3)写出元素⑤的最高价氧化物对应的水化物与元素⑧形成的单质反应的化学方程式___ 。
(4)写出元素③形成的不同化合价的化合物的化学式(写出四个)___ ,其中能与元素⑥形成的单质反应的化学方程式为___ 。

(1)元素⑦在周期表中的位置是
(2)元素①和⑤的原子序数相差
(3)写出元素⑤的最高价氧化物对应的水化物与元素⑧形成的单质反应的化学方程式
(4)写出元素③形成的不同化合价的化合物的化学式(写出四个)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】无机非金属材料、金属材料和有机高分子材料并称为三大材料,是发展高新技术的基石,在科技发展中发挥着重要的作用。完成下列填空:
I.新型材料α-Fe粉具有超强的磁性能,用作高密度磁记录的介质以及高效催化剂等。
(1)自然界一共存在四种稳定的铁原子,计算铁元素的近似相对原子质量的计算式为:54×a1%+56×a2%+57×a3%+58×a4%,其中a1%是指_______ ,58是指_______ 。
(2)已知铁位于周期表第四周期,与铁同周期的主族元素中,最高价氧化物对应水化物中,碱性最强的化合物与酸性最强的化合物的化学反应方程式为_______ 。
II.硅元素是无机非金属材料的主角。
(3)硅在周期表中的位置是_______ ,SiH4的空间构型为_______ 。
III.Nierite是一种高熔点高硬度的陶瓷材料,摩尔质量为140 g/mol,硅元素的质量分数为60%。已知1 mol NH3与足量的化合物T充分反应后可得到35 g Nierite与3 mol HCl气体。
(4)Nierite的化学式为_______ ,T的电子式为_______ 。
(5)碳化硅(SiC)单晶是目前技术最成熟的第三代半导体材料, 下列能说明碳的非金属性强于硅的反应(或反应组)是_______ (选填编号)
a.SiO + 2CO2 + 2H2O = H2SiO3 + 2HCO
+ 2CO2 + 2H2O = H2SiO3 + 2HCO
b.
c.SiH4 Si+2H2↑;CH4
Si+2H2↑;CH4 C+2H2↑
C+2H2↑
d.Si+O2 SiO2;C+O2
SiO2;C+O2 CO2
CO2
I.新型材料α-Fe粉具有超强的磁性能,用作高密度磁记录的介质以及高效催化剂等。
(1)自然界一共存在四种稳定的铁原子,计算铁元素的近似相对原子质量的计算式为:54×a1%+56×a2%+57×a3%+58×a4%,其中a1%是指
(2)已知铁位于周期表第四周期,与铁同周期的主族元素中,最高价氧化物对应水化物中,碱性最强的化合物与酸性最强的化合物的化学反应方程式为
II.硅元素是无机非金属材料的主角。
(3)硅在周期表中的位置是
III.Nierite是一种高熔点高硬度的陶瓷材料,摩尔质量为140 g/mol,硅元素的质量分数为60%。已知1 mol NH3与足量的化合物T充分反应后可得到35 g Nierite与3 mol HCl气体。
(4)Nierite的化学式为
(5)碳化硅(SiC)单晶是目前技术最成熟的第三代半导体材料, 下列能说明碳的非金属性强于硅的反应(或反应组)是
a.SiO
 + 2CO2 + 2H2O = H2SiO3 + 2HCO
+ 2CO2 + 2H2O = H2SiO3 + 2HCO
b.

c.SiH4
 Si+2H2↑;CH4
Si+2H2↑;CH4 C+2H2↑
C+2H2↑d.Si+O2
 SiO2;C+O2
SiO2;C+O2 CO2
CO2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下列为元素周期表中的一部分,用化学式或元素符号回答下列问题。
(1)11种元素中,化学性质最不活泼的是___________ ,原子半径最小的是___________ 。
(2)①②⑤中最高价氧化物的水化物,碱性最强的是___________ 。
(3)②③④中形成的简单离子半径由大到小的顺序是___________ 。
(4)元素⑦的氢化物电子式为___________ ,该氢化物常温下和元素②的单质反应的离子方程式是___________ 。
(5)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为___________ 。
(6)⑧⑨⑪三种元素形成的气态氢化物最稳定的是___________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑦ | ⑪ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)①②⑤中最高价氧化物的水化物,碱性最强的是
(3)②③④中形成的简单离子半径由大到小的顺序是
(4)元素⑦的氢化物电子式为
(5)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为
(6)⑧⑨⑪三种元素形成的气态氢化物最稳定的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
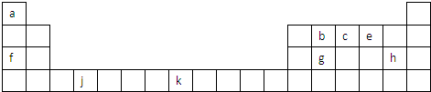
【推荐1】如图是元素周期表的一部分,表中所列字母分别代表一种元素.
试回答下列问题:
(1)以上元素中,属于d区元素的是________ (填元素符号),h在周期表的位置是_________ 。
(2)由e、f以原子个数1∶1形成的晶体中,化学键类型为______________ 。
(3)元素k的基态原子电子排布式为__________ ;画出c的核外电子排布图:_____________ 。
(4)元素c的电负性______ 元素g的电负性(填“>”、“=”、“<”),元素b、c、e的第一电离能由大到小的顺序是___________________ (用元素符号表示)。
(5)工业上冶炼g元素的单质的化学方程式_______________________________ ,f、 h两种元素最高价氧化物对应的水化物反应的化学方程式是___________________ 。
试回答下列问题:
(1)以上元素中,属于d区元素的是
(2)由e、f以原子个数1∶1形成的晶体中,化学键类型为
(3)元素k的基态原子电子排布式为
(4)元素c的电负性
(5)工业上冶炼g元素的单质的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】砷化镍可用于制作发光器件、半导体激光器、太阳能电池和高速集成电路。
(1)基态Ni原子的价电子排布式为_______ 。
(2)第一电离能As_______ Se(填“>”或“<”)。
(3) 是两性氧化物,
是两性氧化物, 溶于盐酸生成
溶于盐酸生成 ,
, 用
用 还原生成
还原生成 。
。
① 的中心原子的杂化方式为
的中心原子的杂化方式为_______ 。
② 分子中H-As-H键角
分子中H-As-H键角_______ 109.5°(填“>”、“=”或“<”)。
(4)有机砷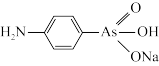 是治疗昏睡病的药物,它存在的化学键种类为
是治疗昏睡病的药物,它存在的化学键种类为_______ (填字母编号)。
a.离子键 b.σ键 c.π键 d.碳碳双键
(1)基态Ni原子的价电子排布式为
(2)第一电离能As
(3)
 是两性氧化物,
是两性氧化物, 溶于盐酸生成
溶于盐酸生成 ,
, 用
用 还原生成
还原生成 。
。①
 的中心原子的杂化方式为
的中心原子的杂化方式为②
 分子中H-As-H键角
分子中H-As-H键角(4)有机砷
 是治疗昏睡病的药物,它存在的化学键种类为
是治疗昏睡病的药物,它存在的化学键种类为a.离子键 b.σ键 c.π键 d.碳碳双键
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.完成下列问题
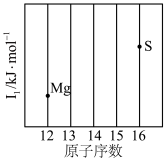
(1)依据第3周期元素第一电离能的变化规律,参照如图Mg、S元素的位置,用小黑点标出Al、Si、P三种元素的相对位置________ 。
Ⅱ.元素的电负性是元素的一种基本性质,下面给出10种元素的电负性。
(2)通过分析电负性的变化规律,确定Mg元素电负性的最小范围___________ 。
(3)下列物质属于离子化合物的是___________
(1)依据第3周期元素第一电离能的变化规律,参照如图Mg、S元素的位置,用小黑点标出Al、Si、P三种元素的相对位置

Ⅱ.元素的电负性是元素的一种基本性质,下面给出10种元素的电负性。
| 元素 | Al | Be | Mg | C | Cl | Na | Li | N | Si | O | H |
| O电负性 | 1.5 | 1.5 | 2.5 | 3.0 | 0.9 | 1.0 | 3.0 | 1.8 | 3.5 | 2.1 |
(2)通过分析电负性的变化规律,确定Mg元素电负性的最小范围
(3)下列物质属于离子化合物的是___________
| A.BeCl2 | B.Li3N | C.HCl | D.CCl4 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)仅由第二周期元素组成的共价分子中,互为等电子体的是:_______ 和_____ ;_____ 和______ 。
(2)HF的沸点比HCl的高,原因是____ ;SiH4的沸点比CH4的高,原因是________ 。
(3)在下列物质①P4 ②NH3 ③HCN ④BF3 ⑤H2O ⑥SO3 ⑦CH3Cl中,属于含有极性键的极性分子的是(填序号)_______ 。
(4)根据价层电子对互斥理论判断下列问题:
CO2分子中,中心原子的杂化方式为__ 杂化,分子的立体构型为________ 。
SO32-中,中心原子的杂化方式为__ 杂化,离子的立体构型为_________ 。
HCHO分子中,中心原子的杂化方式为__ 杂化,分子的立体构型为_________ 。
(5)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):
HClO4_____ HClO2 H2CO3______ H2SiO3 H2SO3_______ H2SO4
(2)HF的沸点比HCl的高,原因是
(3)在下列物质①P4 ②NH3 ③HCN ④BF3 ⑤H2O ⑥SO3 ⑦CH3Cl中,属于含有极性键的极性分子的是(填序号)
(4)根据价层电子对互斥理论判断下列问题:
CO2分子中,中心原子的杂化方式为
SO32-中,中心原子的杂化方式为
HCHO分子中,中心原子的杂化方式为
(5)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):
HClO4
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】请回答下列问题:
(1)工业冶炼镁时采用电解冶炼氯化镁而不是氧化镁的主要原因是___________ 。
(2)已知:①具有相同核外电子数和原子核数的微粒结构相似;②HN3是一元弱酸,HN3 H++N
H++N ;试写出HN3的可能结构式:
;试写出HN3的可能结构式:___________ 。
(1)工业冶炼镁时采用电解冶炼氯化镁而不是氧化镁的主要原因是
(2)已知:①具有相同核外电子数和原子核数的微粒结构相似;②HN3是一元弱酸,HN3
 H++N
H++N ;试写出HN3的可能结构式:
;试写出HN3的可能结构式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】有X、Y、Z、Q、G原子序数依次递增的七种元素,除G元素外其余均为短周期主族元素。X的原子中没有成对电子,Y元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子数相同,Z元素原子的外围电子层排布式为nsnpn+1,Q的基态原子核外成对电子数是成单电子数的3倍,G原子最外电子层只有未成对电子,其内层所有轨道全部充满,但并不是第ⅠA族元素。
(1)基态G原子的价电子排布式为____________ 。
(2)Z、Q、Y三种元素的第一电离能从大到小的顺序为____________ (用元素符号表示)。
(3)用电子式表示X2Q的形成过程________________________________________________ 。
(4)根据等电子体原理,写出YQ的结构式__________________________ 。
(1)基态G原子的价电子排布式为
(2)Z、Q、Y三种元素的第一电离能从大到小的顺序为
(3)用电子式表示X2Q的形成过程
(4)根据等电子体原理,写出YQ的结构式
您最近一年使用:0次



