砷化镍可用于制作发光器件、半导体激光器、太阳能电池和高速集成电路。
(1)基态Ni原子的价电子排布式为_______ 。
(2)第一电离能As_______ Se(填“>”或“<”)。
(3) 是两性氧化物,
是两性氧化物, 溶于盐酸生成
溶于盐酸生成 ,
, 用
用 还原生成
还原生成 。
。
① 的中心原子的杂化方式为
的中心原子的杂化方式为_______ 。
② 分子中H-As-H键角
分子中H-As-H键角_______ 109.5°(填“>”、“=”或“<”)。
(4)有机砷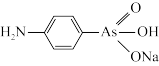 是治疗昏睡病的药物,它存在的化学键种类为
是治疗昏睡病的药物,它存在的化学键种类为_______ (填字母编号)。
a.离子键 b.σ键 c.π键 d.碳碳双键
(1)基态Ni原子的价电子排布式为
(2)第一电离能As
(3)
 是两性氧化物,
是两性氧化物, 溶于盐酸生成
溶于盐酸生成 ,
, 用
用 还原生成
还原生成 。
。①
 的中心原子的杂化方式为
的中心原子的杂化方式为②
 分子中H-As-H键角
分子中H-As-H键角(4)有机砷
 是治疗昏睡病的药物,它存在的化学键种类为
是治疗昏睡病的药物,它存在的化学键种类为a.离子键 b.σ键 c.π键 d.碳碳双键
更新时间:2022-07-14 19:06:53
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】元素周期表中第四周期的某些过渡元素(如Ti、Co等)在生产、生活中有着广泛的应用。Co2+能与水杨醛缩对氯苯胺形成具有发光性的配合物,水杨醛缩对氯苯胺制备反应方程式如下:
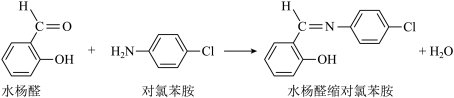
(1)基态Co2+核外电子排布式_______ ;C原子的轨道表示式为_______ ;C、N、O元素的电负性由大到小的顺序为_______ 。
(2)水杨醛所含的官能团为_______ 。
(3)1mol水杨醛最多与_______ H2发生加成反应。
(4)一定条件下,水杨醛缩对氯苯胺与足量NaOH溶液反应的化学方程式_______ 。

(1)基态Co2+核外电子排布式
(2)水杨醛所含的官能团为
(3)1mol水杨醛最多与
(4)一定条件下,水杨醛缩对氯苯胺与足量NaOH溶液反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氮族元素包括氮、磷、砷、锑、铋等元素,其单质及其化合物在研究和生产中有着广泛的应用。试回答下列问题:
(1)NaNO2是一种重要的化工原料,有毒,NaNO2也是一种食品添加剂,使用时须严格控制用量。已知:HNO2有强氧化性,酸性H2SO3>HNO2>CH3COOH。
①氮原子核外共有____ 种能量不同的电子。
②亚硝酰氯(NOCl)是一种红褐色液体,每个原子最外层都达到8e-结构,则其电子式为____ ,其水解会生成两种酸,写出水解的化学方程式____ 。
③往冷的NaNO2溶液中加入下列某种物质可得HNO2稀溶液,该物质是____ (填序号)。
a.稀硫酸 b.二氧化碳 c.二氧化硫 d.醋酸
(2)砷化镓(GaAs)是当前最重要,技术成熟度最高的半导体材料之一,我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。基态As原子外围电子排布式为____ ,最高能级的电子云形状为____ ,As元素在元素周期表中的位置为____ 。
(3)GaN是一种直接能隙(directbandgap)的半导体,自1990年起常用在发光二极管中。工业上以镓粉为原料,用镍催化法生产GaN,在氨气流中于1050~1100℃下加热30min可制得疏松的灰色粉末状GaN,同时得到一种单质,请写出对应的化学方程式____ 。
(1)NaNO2是一种重要的化工原料,有毒,NaNO2也是一种食品添加剂,使用时须严格控制用量。已知:HNO2有强氧化性,酸性H2SO3>HNO2>CH3COOH。
①氮原子核外共有
②亚硝酰氯(NOCl)是一种红褐色液体,每个原子最外层都达到8e-结构,则其电子式为
③往冷的NaNO2溶液中加入下列某种物质可得HNO2稀溶液,该物质是
a.稀硫酸 b.二氧化碳 c.二氧化硫 d.醋酸
(2)砷化镓(GaAs)是当前最重要,技术成熟度最高的半导体材料之一,我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。基态As原子外围电子排布式为
(3)GaN是一种直接能隙(directbandgap)的半导体,自1990年起常用在发光二极管中。工业上以镓粉为原料,用镍催化法生产GaN,在氨气流中于1050~1100℃下加热30min可制得疏松的灰色粉末状GaN,同时得到一种单质,请写出对应的化学方程式
您最近一年使用:0次
【推荐3】根据已学知识,请回答下列问题:
(1)基态N原子中,核外电子占据的最高能层的符号是_______ ,占据该能层电子的原子轨道形状为_______ 。
(2)写出3p轨道上有2个未成对电子的元素的符号:_______ 。
(3)已知铁是26号元素,写出Fe的价层电子排布式:_______ ;
(4)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为_______ ,电负性由大到小的顺序是_______ 。
(5)Zn2+的核外电子排布式为_______ 。
(1)基态N原子中,核外电子占据的最高能层的符号是
(2)写出3p轨道上有2个未成对电子的元素的符号:
(3)已知铁是26号元素,写出Fe的价层电子排布式:
(4)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为
(5)Zn2+的核外电子排布式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】C和Si元素在化学中占有极其重要的地位。
(1)写出Si的基态原子核外电子排布式___________ 。C、Si和O元素的电负性由大至小的顺序为___________ 。
(2)SiC的晶体结构与晶体硅相似,其中C原子的杂化方式为___________ ,微粒间存在的作用力是___________ ;lmol硅晶体中有___________ molSi-Si键。
(3)氧化物MO的电子总数与SiC的相等,则M为___________ (填元素符号)。MO是优良的耐高温材料,其晶体结构与NaCl晶体相似。MO的熔点比CaO的高,其原因是___________ 。
(4)C、Si为同一主族的元素,CO2和SiO2化学式相似,但结构和性质有很大不同。CO2中C与O原子间形成σ键和π键,SiO2中Si与О原子间不形成上述π键。从原子半径大小的角度分析,为何C、O原子间能形成,而Si、O原子间不能形成上述π键?___________ 。
(1)写出Si的基态原子核外电子排布式
(2)SiC的晶体结构与晶体硅相似,其中C原子的杂化方式为
(3)氧化物MO的电子总数与SiC的相等,则M为
(4)C、Si为同一主族的元素,CO2和SiO2化学式相似,但结构和性质有很大不同。CO2中C与O原子间形成σ键和π键,SiO2中Si与О原子间不形成上述π键。从原子半径大小的角度分析,为何C、O原子间能形成,而Si、O原子间不能形成上述π键?
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
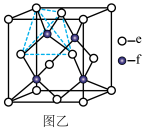
【推荐2】a、b、c、d、e、f分别是H、C、N、Na、Si、Cu六种元素中的其中一种,已知:下图甲表示的是这六种元素单质的熔点高低顺序,其中c、d均是热和电的良导体,f形成的某种单质硬度最大。

回答下列问题:
(1)a、b、f三种元素的电负性从小到大的顺序为___________ (用元素符号表示);
(2)元素b的单质的一个分子中含有___________ 个σ键和___________ 个π键;
(3)c单质分别与氟气和氯气形成化合物甲和乙,则甲的熔点___________ 乙的熔点(填>或<);
(4)元素d的基态原子的价电子排布式为___________ ;
(5)元素c和f可形成化合物丙(丙的晶胞结构如图乙所示),则丙的化学式为___________ ,丙的晶体类型为___________ ,在丙中,每个e原子周围最近的e原子数目为___________ 。

回答下列问题:
(1)a、b、f三种元素的电负性从小到大的顺序为
(2)元素b的单质的一个分子中含有
(3)c单质分别与氟气和氯气形成化合物甲和乙,则甲的熔点
(4)元素d的基态原子的价电子排布式为
(5)元素c和f可形成化合物丙(丙的晶胞结构如图乙所示),则丙的化学式为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】决定物质性质的重要因素是物质结构。请回答下列问题:
(1)已知元素M是组成物质Ca5(PO4)3F的一种元素。元素M的气态原子逐个失去第1个至第5个电子所需能量(即电离能,用符号I1至I5表示)如表所示:
元素M化合态常见化合价是___________ 价,其基态原子电子排布式为____________ 。
(2)往硫酸铜溶液中加入过量氨水,可形成[Cu(NH3)4]S04溶液,该溶液可用于溶解纤维素。
①[Cu (NH3) 4 ] S04中阴离子的立体构型是______________ 。
②除硫元素外,[Cu( NH3) 4 ] S04中所含元素的电负性由小到大的顺序为________________ 。
③NF3与NH3的空间构型相同,中心原子的轨道杂化类型均为___________ 。NF3不易与Cu2 +形成化学键,其原因是________________________ 。
(1)已知元素M是组成物质Ca5(PO4)3F的一种元素。元素M的气态原子逐个失去第1个至第5个电子所需能量(即电离能,用符号I1至I5表示)如表所示:
| I1 | I2 | I3 | I4 | I5 | |
| 电离能(kJ/mol) | 589.8 | 1145.4 | 4912.4 | 6491 | 8153 |
元素M化合态常见化合价是
(2)往硫酸铜溶液中加入过量氨水,可形成[Cu(NH3)4]S04溶液,该溶液可用于溶解纤维素。
①[Cu (NH3) 4 ] S04中阴离子的立体构型是
②除硫元素外,[Cu( NH3) 4 ] S04中所含元素的电负性由小到大的顺序为
③NF3与NH3的空间构型相同,中心原子的轨道杂化类型均为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】碳族元素的物质是化学世界中最庞大的家族,“天问一号”轨道飞行器近距离拍摄了火星北极,看到大量白色冰冻区域, 主要是二氧化碳低温凝结形成的干冰,虽然看起来和地球两极很像,但实际温度却比地球两极冷多了!
(1)已知 25℃时,H2CO3的Ka1=4.2×10-7、Ka2=4.8×10- 11,HCN的Ka=4.0×10-10,若向NaCN 溶液中通入少量 CO2,发生反应的离子方程式为___________ 。
(2)下列关于二氧化碳的说法正确的是___________。
(3)干冰和冰的晶体模型如下图存在差别的本质原因___________ 。___________ 。
(5)金刚石晶体中,每个C被___________ 个六元环共用。
(6)晶体硅和碳化硅熔点较高的是___________ (填化学式)。
(7)已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为___________ 。
(1)已知 25℃时,H2CO3的Ka1=4.2×10-7、Ka2=4.8×10- 11,HCN的Ka=4.0×10-10,若向NaCN 溶液中通入少量 CO2,发生反应的离子方程式为
(2)下列关于二氧化碳的说法正确的是___________。
A.电子式为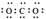 | B.空间填充模型为  |
| C.CO2 是极性分子, 能溶于水 | D.CO2 的水溶液能够导电,但 CO2是非电解质 |
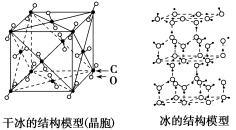
(5)金刚石晶体中,每个C被
(6)晶体硅和碳化硅熔点较高的是
(7)已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)下列变化:①I2升华;②烧碱熔化;③NaCl溶于水;④HCl溶于水;⑤O2溶于水;⑥NH4HCO3受热分解。其中仅发生共价键破坏的是___________ ;(填序号,下同)仅发生离子键破坏的是___________ ;
(2)在下列物质中:①HCl、②N2、③NH3、④Na2O2、⑤H2O2、⑥NH4Cl、⑦NaOH、⑧Ar、⑨CO2、⑩C2H4(用物质前序号填空)。其中只存在非极性键的分子是___________ ;既存在离子键又存在极性键的是___________ 。
(3)写出下列物质的电子式。
①Na2O2___________ ; ②HClO ___________ ;③NH4Cl___________ 。
(4)用电子式表示下列物质的形成过程。
Na2S___________ ;H2O___________ 。
(1)下列变化:①I2升华;②烧碱熔化;③NaCl溶于水;④HCl溶于水;⑤O2溶于水;⑥NH4HCO3受热分解。其中仅发生共价键破坏的是
(2)在下列物质中:①HCl、②N2、③NH3、④Na2O2、⑤H2O2、⑥NH4Cl、⑦NaOH、⑧Ar、⑨CO2、⑩C2H4(用物质前序号填空)。其中只存在非极性键的分子是
(3)写出下列物质的电子式。
①Na2O2
(4)用电子式表示下列物质的形成过程。
Na2S
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)若BCl3与XYn通过B原子与X原子间的配位键结合形成配合物,则该配合物提供孤电子对的原子是________ 。
(2)NH3与BF3可以通过配位键形成NH3·BF3,____ 原子提供孤电子对,________ 原子提供空轨道。写出NH3·BF3的结构式,并用“→”表示出配位键________ 。
(3)肼(N2H4)分子可视为NH3分子中的一个氢原子被—NH2(氨基)取代形成的另一种氮的氢化物。肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内存在________ (填字母)。
a.离子键 b.配位键 c.共价键 d.σ键
(4)向氯化铜溶液中加入过量浓氨水,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]Cl2晶体,上述深蓝色晶体中含有的化学键除普通共价键外,还有________ 和________ 。
(1)若BCl3与XYn通过B原子与X原子间的配位键结合形成配合物,则该配合物提供孤电子对的原子是
(2)NH3与BF3可以通过配位键形成NH3·BF3,
(3)肼(N2H4)分子可视为NH3分子中的一个氢原子被—NH2(氨基)取代形成的另一种氮的氢化物。肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内存在
a.离子键 b.配位键 c.共价键 d.σ键
(4)向氯化铜溶液中加入过量浓氨水,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]Cl2晶体,上述深蓝色晶体中含有的化学键除普通共价键外,还有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】我国是世界稀土资源大国,稀土元素是镧系、钪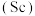 、钇
、钇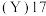 种元素的总称,它们位于元素周期表中同一副族。
种元素的总称,它们位于元素周期表中同一副族。
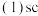 原子的价层电子排布式为
原子的价层电子排布式为______ ,第一电离能Sc______ Y 填“大于”或“小于”
填“大于”或“小于” 。
。
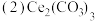 是生产铈的中间化合物,它可由氟碳酸铈
是生产铈的中间化合物,它可由氟碳酸铈
 精矿制得:
精矿制得:
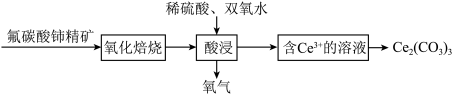
 中,Ce的化合价为
中,Ce的化合价为______ 。
 氧化焙烧生成二氧化铈
氧化焙烧生成二氧化铈 ,其在酸浸时发生反应的离子方程式为
,其在酸浸时发生反应的离子方程式为______ 。
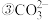 离子的立体构型的名称为
离子的立体构型的名称为______ ,中心原子的杂化方式为______ ,分子或离子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数
键的电子数 如苯分子中的大
如苯分子中的大 键可表示为
键可表示为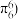 ,则
,则 中的大
中的大 键应表示为
键应表示为______ 。
 常温、常压下
常温、常压下 是铈最稳定的化合物,广泛用于玻璃、原子能、电子管等工业。
是铈最稳定的化合物,广泛用于玻璃、原子能、电子管等工业。 晶胞是立方萤石型,则铈离子的配位数为
晶胞是立方萤石型,则铈离子的配位数为______ ,如图中离子坐标参数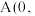 0,
0, ;
;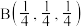 :
: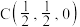 ,若将B选为晶胞顶点坐标参数
,若将B选为晶胞顶点坐标参数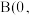 0,
0, ,则D离子处于
,则D离子处于______ 位置,坐标参数为______ 。已知该晶胞的棱长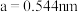 ,其密度为
,其密度为______ 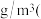 列出计算式即可
列出计算式即可 。
。

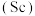 、钇
、钇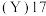 种元素的总称,它们位于元素周期表中同一副族。
种元素的总称,它们位于元素周期表中同一副族。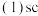 原子的价层电子排布式为
原子的价层电子排布式为 填“大于”或“小于”
填“大于”或“小于” 。
。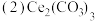 是生产铈的中间化合物,它可由氟碳酸铈
是生产铈的中间化合物,它可由氟碳酸铈
 精矿制得:
精矿制得:
 中,Ce的化合价为
中,Ce的化合价为 氧化焙烧生成二氧化铈
氧化焙烧生成二氧化铈 ,其在酸浸时发生反应的离子方程式为
,其在酸浸时发生反应的离子方程式为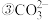 离子的立体构型的名称为
离子的立体构型的名称为 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数
键的电子数 如苯分子中的大
如苯分子中的大 键可表示为
键可表示为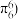 ,则
,则 中的大
中的大 键应表示为
键应表示为 常温、常压下
常温、常压下 是铈最稳定的化合物,广泛用于玻璃、原子能、电子管等工业。
是铈最稳定的化合物,广泛用于玻璃、原子能、电子管等工业。 晶胞是立方萤石型,则铈离子的配位数为
晶胞是立方萤石型,则铈离子的配位数为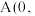 0,
0, ;
;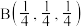 :
: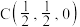 ,若将B选为晶胞顶点坐标参数
,若将B选为晶胞顶点坐标参数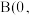 0,
0, ,则D离子处于
,则D离子处于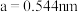 ,其密度为
,其密度为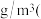 列出计算式即可
列出计算式即可 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】[化学-选修3:物质结构与性质] 2015年8月12号接近午夜时分,天津滨海新区一处集装箱码头发生爆炸。发生爆炸的是集装箱内的易燃易爆物品,爆炸火光震天,并产生巨大蘑菇云。
回答下列问题:
(1)在组成NH4NO3、NaCN两种物质的元素中第一电离能最大的是___________ (填元素符号),解释原因_____________________________________________ 。
(2)二甲基二硫和甲酸中,在水中溶解度较大的是__________ (填名称),原因是_____________ ;烧碱所属的晶体类型为________ ;硫化碱(Na2S)的S2-的基态电子排布式是________________ 。
(3)硝酸铵中,NO3-的立体构型为____ ,中心原子的杂化轨道类型为___________ 。
(4)1mol化合物NaCN中CN-所含的π键数为______ ,与-CN互为等电子体的分子有__ 。(CN)2又称为拟卤素,实验室可以用氰化钠、二氧化锰和浓硫酸在加热条件下制得,写成该制备的化学方程式________________ 。

(5)钠钾合金属于金属晶体,其某种合金的晶胞结构如图所示。合金的化学式为____________ ;晶胞中K 原子的配位数为___ ;已知金属原子半径r(Na)=186pm、r(K)=227pm,计算晶体的空间利用率 __________ (列出计算式,不需要计算出结果)。
回答下列问题:
(1)在组成NH4NO3、NaCN两种物质的元素中第一电离能最大的是
(2)二甲基二硫和甲酸中,在水中溶解度较大的是
(3)硝酸铵中,NO3-的立体构型为
(4)1mol化合物NaCN中CN-所含的π键数为

(5)钠钾合金属于金属晶体,其某种合金的晶胞结构如图所示。合金的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】科学家们锲而不舍地努力,揭示了原子结构的奥秘,知道了原子核外电子的排布决定元素在周期表中的位置。
Ⅰ.请回答下列问题
(1)下列分子中,所有原子都满足最外层为8电子结构的是_________
(2)下列对分子性质的解释中,正确的是_________
(3)关于氢键,下列说法正确的是_________
Ⅱ.氮及其化合物在自然界中存在循环,请回答下列问题:
(4)基态氮原子核外电子共占据___________ 个轨道,最外层有___________ 种不同能量的电子。
(5)NH3中心原子为___________ 杂化,N2的电子式为___________ 。
(6)在催化剂和加热条件下,NO2与NH3可反应生成无害物质,请写出反应的化学方程式:___________ 。
(7)实验室可用烧碱溶液吸收NO2和NO,(已知2NO2+2NaOH=NaNO2+NaNO3+H2O,NO2+NO+2NaOH=2NaNO2+H2O),当消耗100mL 0.5mol·L-1的烧碱溶液时,共吸收混合气体___________ L(标准状况下)。
(8)NH4Fe(SO4)2用作工业废水的凝结剂,为检验其中的铁元素可选用的方法是___________ 。相同条件下,0.1mol/L NH4Fe(SO4)2中[Fe3+]___________ 0.1mol/L FeCl3中[Fe3+](填“=”、“<”或“>”)。
Ⅰ.请回答下列问题
(1)下列分子中,所有原子都满足最外层为8电子结构的是_________
| A.CH4 | B.XeF2 | C.BF3 | D.NF3 |
A.乳酸(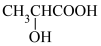 )具有光学活性,因为其分子中含有一个手性碳原子 )具有光学活性,因为其分子中含有一个手性碳原子 |
| B.NH3极易溶于水而CH4难溶于水只是因为NH3是极性分子,CH4是非极性分子 |
| C.水很稳定(1000°C以上才会部分分解)是因为水分子间存在大量的氢键 |
| D.已知酸性:H3PO4>HClO,因为H3PO4的氧原子数大于HClO的氧原子数 |
A.因为氢键的缘故,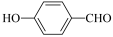 比 比 熔沸点高 熔沸点高 |
| B.分子中有N、O、F原子,分子间就存在氢键 |
| C.NH3的稳定性很强,是因为其分子间能形成氢键 |
| D.“可燃冰”—甲烷水合物(CH4·8H2O)中CH4与H2O之间不存在氢键 |
Ⅱ.氮及其化合物在自然界中存在循环,请回答下列问题:
(4)基态氮原子核外电子共占据
(5)NH3中心原子为
(6)在催化剂和加热条件下,NO2与NH3可反应生成无害物质,请写出反应的化学方程式:
(7)实验室可用烧碱溶液吸收NO2和NO,(已知2NO2+2NaOH=NaNO2+NaNO3+H2O,NO2+NO+2NaOH=2NaNO2+H2O),当消耗100mL 0.5mol·L-1的烧碱溶液时,共吸收混合气体
(8)NH4Fe(SO4)2用作工业废水的凝结剂,为检验其中的铁元素可选用的方法是
您最近一年使用:0次



