氮族元素包括氮、磷、砷、锑、铋等元素,其单质及其化合物在研究和生产中有着广泛的应用。试回答下列问题:
(1)NaNO2是一种重要的化工原料,有毒,NaNO2也是一种食品添加剂,使用时须严格控制用量。已知:HNO2有强氧化性,酸性H2SO3>HNO2>CH3COOH。
①氮原子核外共有____ 种能量不同的电子。
②亚硝酰氯(NOCl)是一种红褐色液体,每个原子最外层都达到8e-结构,则其电子式为____ ,其水解会生成两种酸,写出水解的化学方程式____ 。
③往冷的NaNO2溶液中加入下列某种物质可得HNO2稀溶液,该物质是____ (填序号)。
a.稀硫酸 b.二氧化碳 c.二氧化硫 d.醋酸
(2)砷化镓(GaAs)是当前最重要,技术成熟度最高的半导体材料之一,我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。基态As原子外围电子排布式为____ ,最高能级的电子云形状为____ ,As元素在元素周期表中的位置为____ 。
(3)GaN是一种直接能隙(directbandgap)的半导体,自1990年起常用在发光二极管中。工业上以镓粉为原料,用镍催化法生产GaN,在氨气流中于1050~1100℃下加热30min可制得疏松的灰色粉末状GaN,同时得到一种单质,请写出对应的化学方程式____ 。
(1)NaNO2是一种重要的化工原料,有毒,NaNO2也是一种食品添加剂,使用时须严格控制用量。已知:HNO2有强氧化性,酸性H2SO3>HNO2>CH3COOH。
①氮原子核外共有
②亚硝酰氯(NOCl)是一种红褐色液体,每个原子最外层都达到8e-结构,则其电子式为
③往冷的NaNO2溶液中加入下列某种物质可得HNO2稀溶液,该物质是
a.稀硫酸 b.二氧化碳 c.二氧化硫 d.醋酸
(2)砷化镓(GaAs)是当前最重要,技术成熟度最高的半导体材料之一,我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。基态As原子外围电子排布式为
(3)GaN是一种直接能隙(directbandgap)的半导体,自1990年起常用在发光二极管中。工业上以镓粉为原料,用镍催化法生产GaN,在氨气流中于1050~1100℃下加热30min可制得疏松的灰色粉末状GaN,同时得到一种单质,请写出对应的化学方程式
更新时间:2022-11-08 20:36:18
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可如图表示。
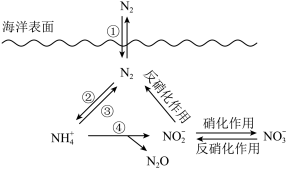
(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是__________ (填图中数字序号)。
(2)下列关于海洋氮循环的说法正确的是_______ (填字母序号)。
a.海洋中存在游离态的氮 b.海洋中的氮循环起始于氮的氧化c.海洋中的反硝化作用一定有氧气的参与d.向海洋排放含 的废水会影响海洋中
的废水会影响海洋中 的含量
的含量
(3)有氧时,在硝化细菌作用下, 可实现过程④的转化,将过程④的离子方程式补充完整:
可实现过程④的转化,将过程④的离子方程式补充完整: ___  + 5O2 == 2
+ 5O2 == 2 +
+ ____ H+ +____ +_____

(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是
(2)下列关于海洋氮循环的说法正确的是
a.海洋中存在游离态的氮 b.海洋中的氮循环起始于氮的氧化c.海洋中的反硝化作用一定有氧气的参与d.向海洋排放含
 的废水会影响海洋中
的废水会影响海洋中 的含量
的含量(3)有氧时,在硝化细菌作用下,
 可实现过程④的转化,将过程④的离子方程式补充完整:
可实现过程④的转化,将过程④的离子方程式补充完整:  + 5O2 == 2
+ 5O2 == 2 +
+
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Li3Fe2(PO4)3作为锂离子电池的负极材料时有良好的放电平台,通过提高材料的电导率可以有效的改善材料的性能。配平下列反应的化学方程式。___ Li3Fe2(PO4)3+1Fe2O3+CO→CO2+LiFePO4
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)化学与生产生活密切相关,请写出下列反应
①实验室制氯气_________________ (离子方程式)
②“腐蚀法”制作印刷电路板____________ (化学方程式)并用双线桥表示该反应的电子转移数目和方向
(2)K2FeO4可用作水处理剂,它可由以下反应制得:
____ Cl2 + ____ Fe(OH)3 + _____ OH- === ______ FeO4 2-+ _____ Cl- +____ H2O
配平此反应方程式。当1mol K2FeO4生成时,转移的电子数目为_____
①实验室制氯气
②“腐蚀法”制作印刷电路板
(2)K2FeO4可用作水处理剂,它可由以下反应制得:
配平此反应方程式。当1mol K2FeO4生成时,转移的电子数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】硫及其化合物在生产、生活中具有广泛的应用,根据所学知识,回答下列问题:
(1)Al2(SO4)3溶液显___________ (填“酸”、“碱”或“中”)性,判断的理由是___________ (用离子方程式表示),若将该溶液蒸干,最终所得固体为___________ (填化学式)。
(2)(NH4)2SO4溶液中,各离子浓度由大到小的关系为___________ 。
(3)室温下,在某NaHSO3、Na2SO3混合溶液中, 、
、 物质的量分数随
物质的量分数随 的变化曲线如图所示,根据图示,
的变化曲线如图所示,根据图示, 的水解平衡常数Kh=
的水解平衡常数Kh=___________ 。

(4)室温下,某浓度的(NH4)2SO3溶液中:
①(NH4)2SO3为___________ (填“强”或“弱”)电解质。
②
___________ (填“>”、“<”或“=”)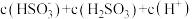 。
。
③往(NH4)2SO3溶液中滴加少量的HClO溶液,发生反应的离子方程式为___________ ,此时所得溶液的pH___________ (填“变大”、“变小”或“不变”)。
(1)Al2(SO4)3溶液显
(2)(NH4)2SO4溶液中,各离子浓度由大到小的关系为
(3)室温下,在某NaHSO3、Na2SO3混合溶液中,
 、
、 物质的量分数随
物质的量分数随 的变化曲线如图所示,根据图示,
的变化曲线如图所示,根据图示, 的水解平衡常数Kh=
的水解平衡常数Kh=
(4)室温下,某浓度的(NH4)2SO3溶液中:
①(NH4)2SO3为
②

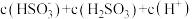 。
。③往(NH4)2SO3溶液中滴加少量的HClO溶液,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】盐类水解离子方程式的书写
(1)盐类水解的离子方程式一般应用“___________ ”连接:
CH3COONa___________ ;NH4Cl___________ 。
(2)多元弱酸根离子水解方程式应___________ 书写,水解是以第一步为主,如 水解方程式为
水解方程式为___________ 。
(3)多元弱碱阳离子水解要求一步写道底:Fe3++3H2O___________ 。
(4)由于水解程度较小,水解生成的弱电解质的浓度很小,即一般不生成沉淀或气体,一般不标“↓”或“↑”符号。
【总结】
(5)盐类水解可视为___________ 的逆反应,因此应为___________ 反应。盐类水解是可逆反应,而且程度很___________ 。盐类的水解在水溶液中可以建立一种平衡状态,称为___________ 。
(1)盐类水解的离子方程式一般应用“
CH3COONa
(2)多元弱酸根离子水解方程式应
 水解方程式为
水解方程式为(3)多元弱碱阳离子水解要求一步写道底:Fe3++3H2O
(4)由于水解程度较小,水解生成的弱电解质的浓度很小,即一般不生成沉淀或气体,一般不标“↓”或“↑”符号。
【总结】
(5)盐类水解可视为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)铁在元素周期表中的位置为_____ ,基态铁原子有个未成对电子_____ ,三价铁离子的电子排布式为_____ 。
(2)基态Si原子中,电子占据的最高能层符号_____ ,该能层具有的原子轨道数为_____ ;铝元素的原子核外共有_____ 种不同运动状态的电子、_____ 种不同能级的电子。
(3)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用_____ 形象化描述。在基态14C原子中,核外存在_____ 对自旋相反的电子。
(2)基态Si原子中,电子占据的最高能层符号
(3)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵【(NH4)3Fe(C6H5O7)2】。
(1)Fe2+基态核外电子排布式为___ ;NO 的空间构型为
的空间构型为___ (用文字描述)。
(2)NH3分子中氮原子的轨道杂化类型是___ ;C、N、O元素的第一电离能由大到小的顺序为___ 。
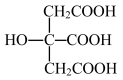
(3)柠檬酸的结构简式见图。1mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为=__ mol。
(4)利用键能数据计算反应的ΔH(请写出解题过程):N2(g)+3H2(g)=2NH3(g)。___
(1)Fe2+基态核外电子排布式为
 的空间构型为
的空间构型为(2)NH3分子中氮原子的轨道杂化类型是
(3)柠檬酸的结构简式见图。1mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为=

(4)利用键能数据计算反应的ΔH(请写出解题过程):N2(g)+3H2(g)=2NH3(g)。
| 化学键 | H—H | N—H | N≡N |
| 键能/(kJ·mol-1) | 436 | 393 | 946 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】根据所学知识,回答下列问题:
(1)Cu的简化电子排布式为___________ 。Fe2+的价电子轨道表示式为___________ 。
(2)乙炔分子中σ键与π键个数之比为___________ 。
(3)吡啶( )是一种常用的有机溶剂。已知吡啶中所有原子共面,且分子中含有与苯类似的
)是一种常用的有机溶剂。已知吡啶中所有原子共面,且分子中含有与苯类似的 大π键,由此可知,吡啶中N原子的价层孤电子对占据
大π键,由此可知,吡啶中N原子的价层孤电子对占据___________ 轨道。
(4)NH3、PH3、AsH3按照沸点由高到低排序,依次为___________ 。
(5)BF3、SiF4、NF3按照键角由大到小排序,依次为___________ 。
(6)科学家合成了一种新型离子化合物NH5,其所有原子最外层都符合相应稀有气体原子电子层结构,该物质遇水会发生水解,生成一种一元弱碱和一种单质气体。该反应的化学方程式为___________ 。
(1)Cu的简化电子排布式为
(2)乙炔分子中σ键与π键个数之比为
(3)吡啶(
 )是一种常用的有机溶剂。已知吡啶中所有原子共面,且分子中含有与苯类似的
)是一种常用的有机溶剂。已知吡啶中所有原子共面,且分子中含有与苯类似的 大π键,由此可知,吡啶中N原子的价层孤电子对占据
大π键,由此可知,吡啶中N原子的价层孤电子对占据(4)NH3、PH3、AsH3按照沸点由高到低排序,依次为
(5)BF3、SiF4、NF3按照键角由大到小排序,依次为
(6)科学家合成了一种新型离子化合物NH5,其所有原子最外层都符合相应稀有气体原子电子层结构,该物质遇水会发生水解,生成一种一元弱碱和一种单质气体。该反应的化学方程式为
您最近一年使用:0次



