现有部分短周期元素的性质或原子结构如下表:
(1)写出元素X的离子结构示意图____________ 。
(2)写出Y元素最高价氧化物的水化物与NaOH溶液反应的离子方程式______________
(3)写出Y的价电子排布式_________________________ 。
(4)元素T与氯元素相比,非金属性较强的是_______ (用元素符号表示),下列表述中能用于证明这一事实的是_______ (填字母代号)。
A.气态氢化物的挥发性 B.两元素的电负性
C.含氧酸的酸性 D.氢化物中X—H键的键长(X代表T和Cl两种元素)
(5)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是___ (填元素符号)
| 元素编号 | 元素性质或原子结构 |
| T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| X | L层p电子数比s电子数多2个 |
| Y | 第三周期元素的简单离子中半径最小 |
| Z | L层有三个未成对电子 |
(1)写出元素X的离子结构示意图
(2)写出Y元素最高价氧化物的水化物与NaOH溶液反应的离子方程式
(3)写出Y的价电子排布式
(4)元素T与氯元素相比,非金属性较强的是
A.气态氢化物的挥发性 B.两元素的电负性
C.含氧酸的酸性 D.氢化物中X—H键的键长(X代表T和Cl两种元素)
(5)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是
更新时间:2018-07-16 16:44:12
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】请写出下列反应的离子方程式:
①氯气与氯化亚铁溶液的反应_________________________________________________
②二氧化锰与浓盐酸反应_______________________________________________________
③氢氧化铝与足量氢氧化钠反应__________________________________________________
④ 偏铝酸钠与过量二氧化碳的反应________________________________________________
①氯气与氯化亚铁溶液的反应
②二氧化锰与浓盐酸反应
③氢氧化铝与足量氢氧化钠反应
④ 偏铝酸钠与过量二氧化碳的反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】简要回答下列问题
(1)氢氧化铝是典型且常用的抗酸药,具有抗酸、吸着、局部止血和保护溃疡面等作用。请用化学方程式表示其治疗胃酸过多的原理:___________ 。
(2)写出Cu在Cl2中燃烧的化学方程式:___________ 。
(3)如何用化学方法辨别溶液中是否含氯离子:___________ 。
(4)实验室浓硝酸应保存在棕色试剂瓶中并放置在阴凉处,其原因是______ (用化学方程式表示)。

(1)氢氧化铝是典型且常用的抗酸药,具有抗酸、吸着、局部止血和保护溃疡面等作用。请用化学方程式表示其治疗胃酸过多的原理:
(2)写出Cu在Cl2中燃烧的化学方程式:
(3)如何用化学方法辨别溶液中是否含氯离子:
(4)实验室浓硝酸应保存在棕色试剂瓶中并放置在阴凉处,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】铝、铁是常见的金属,其化合物也有广泛的用途。回答下列问题:
(1)氢氧化铝是一种两性氢氧化物,写出它的电离方程式___ ,将少量的稀盐酸逐渐滴入NaAlO2溶液,产生的现象为___ ,用平衡移动原理来解释这一现象:___ 。
(2)明矾可以用于净水,用离子反应方程式来解释原理:___ ,将Ba(OH)2溶液滴入明矾溶液中,当SO42-完全沉淀,则铝元素在溶液中存在的形式为___ (用化学式表示)。
(3)高铁酸钠(Na2FeO4)可用作高效水处理剂,既可以杀菌消毒,又可以除去水中的悬浮颗粒物,请用你所学过的化学原理加以解释。___ 。
(1)氢氧化铝是一种两性氢氧化物,写出它的电离方程式
(2)明矾可以用于净水,用离子反应方程式来解释原理:
(3)高铁酸钠(Na2FeO4)可用作高效水处理剂,既可以杀菌消毒,又可以除去水中的悬浮颗粒物,请用你所学过的化学原理加以解释。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】W、X、Y、Z是原子半径依次增大的四种短周期主族元素,已知25℃时,W、Z形成的0.01mol.L-1化合物的水溶液pH=2,X3-电子层结构与氖元素相同,Y的最外层电子数是电子层数的2倍。
(1)Z在元素周期表中位置是_____________ 。
(2)(YX)2结构与卤素单质相似,组成原子均满足8电子稳定结构,(YX)2的结构式为
________ (元素符号表示)。
(3)W、X、Z组成的一种常见化合物可用作焊接金属的除锈剂,该化合物的水溶液与Mg反应有两种气体产生,其中一种气体有刺激性气味,该反应的离子方程式为____________ 。该化合物的稀溶液与稀NaOH溶液混合(不考虑含X微粒的分解和挥发等),所得溶液呈中性,则含X的分子的浓度_________ c(Na+)(填“大于”、“小于”或“等于”)。
(4)XZ3在湿气中易水解生成一种常见的漂白剂,且反应为非氧化还原反应,该反应的化学方程式为__________________________ 。
(1)Z在元素周期表中位置是
(2)(YX)2结构与卤素单质相似,组成原子均满足8电子稳定结构,(YX)2的结构式为
(3)W、X、Z组成的一种常见化合物可用作焊接金属的除锈剂,该化合物的水溶液与Mg反应有两种气体产生,其中一种气体有刺激性气味,该反应的离子方程式为
(4)XZ3在湿气中易水解生成一种常见的漂白剂,且反应为非氧化还原反应,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】用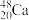 轰击
轰击 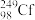 ,生成
,生成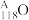 g并放出3个中子(
g并放出3个中子( )。
)。
(1)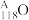 g的原子核内中子数是
g的原子核内中子数是_______ 。
(2)推测Og在元素周期表的位置_______ 。
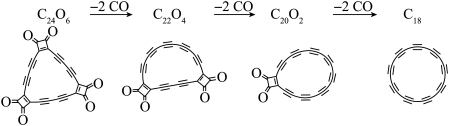
(3)2019年科学家首次合成全碳的环形分子,下列说法正确的是_______
(4)写出实验室制取氯气的化学方程式_______ ;
(5)在383K时,将二氧化锰溶解于浓硫酸中,可得硫酸锰[ Mn2 ( SO4)3]并放出氧气。试写出该反应的化学方程式_______ ;
(6)已知铋酸钠( NaBiO3 )是一种浅黄色的粉末,不溶于冷水,它可以在高酸度的溶液中将Mn2+氧化成 ,自身被还原成Bi3+。试写出该反应的离子方程式
,自身被还原成Bi3+。试写出该反应的离子方程式_______ 。
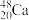 轰击
轰击 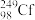 ,生成
,生成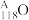 g并放出3个中子(
g并放出3个中子( )。
)。(1)
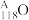 g的原子核内中子数是
g的原子核内中子数是(2)推测Og在元素周期表的位置
(3)2019年科学家首次合成全碳的环形分子,下列说法正确的是_______

| A.C18和金刚石、石墨互为同素异形体 |
| B.C18是一种性质很稳定的化合物 |
| C.C20O2、C22O4、C24O6随着碳原子数的增大,氧元素的质量百分含量依次增大 |
| D.C22O4、CO、CO2都是碳元素的氧化物 |
(5)在383K时,将二氧化锰溶解于浓硫酸中,可得硫酸锰[ Mn2 ( SO4)3]并放出氧气。试写出该反应的化学方程式
(6)已知铋酸钠( NaBiO3 )是一种浅黄色的粉末,不溶于冷水,它可以在高酸度的溶液中将Mn2+氧化成
 ,自身被还原成Bi3+。试写出该反应的离子方程式
,自身被还原成Bi3+。试写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】X、Y、Z、W、Q为元素周期表中前四周期的元素,其元素性质和原子结构如表所述。
回答下列问题:
(1)Y位于元素周期表的___________ 区,基态Z原子的价层电子排布图为___________ 。
(2)与W同周期且第一电离能比其大的元素为___________ (填元素符号),W与X形成的简单化合物分子中,中心原子的VSEPR模型为___________ 。
(3)基态Q原子有___________ 种空间运动状态,Q与X形成的简单化合物和W与X形成的简单化合物在水中溶解度较大的为___________ (写分子式),原因为___________ 。
(4)W和Q形成的某种分子的空间构型为三角锥形,其中心原子的杂化轨道类型为___________ ,该分子为___________ (填“极性”或“非极性”)分子。
| 元素 | 元素性质或原子结构 |
| X | 基态原子只有一种形状的轨道填有电子,且易形成共价键 |
| Y | 基态原子核外的M层中只有两对成对电子 |
| Z | 前四周期元素中基态原子的未成对电子数最多 |
| W | 与Y同周期,且在该周期元素中第一电离能由大到小排第三位 |
| Q | 元素周期表中电负性最大的元素 |
回答下列问题:
(1)Y位于元素周期表的
(2)与W同周期且第一电离能比其大的元素为
(3)基态Q原子有
(4)W和Q形成的某种分子的空间构型为三角锥形,其中心原子的杂化轨道类型为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下面是元素周期表的前三周期。请用相应的化学用语回答下列问题:
(1)写出由e形成的两种阴离子的符号,它们带有相同的电荷数:______ 、_____ ;
(2)h的单质能与g元素的最高价氧化物对应水化物的溶液反应,请写出该反应的化学方程式________

(注:序列与b、c、d、e、f 并不一一对应)
(3)上左图表示的是b、c、d、e、f的氢化物的沸点(℃)。序列 “5”的氢化物是由______ 键构成的______ 分子(均填写“极性”或“非极性”)。由c和 e 组成的可灭火的物质的电子式是_______ 。
(4)上图是表示第三周期8种元素单质的熔点(℃)柱形图,已知柱形“1”代表Ar,则柱形“8”熔点最高的原因是__________ 。
| a | |||||||
| b | c | d | e | f | |||
| g | h |
(1)写出由e形成的两种阴离子的符号,它们带有相同的电荷数:
(2)h的单质能与g元素的最高价氧化物对应水化物的溶液反应,请写出该反应的化学方程式

(注:序列与b、c、d、e、f 并不一一对应)
(3)上左图表示的是b、c、d、e、f的氢化物的沸点(℃)。序列 “5”的氢化物是由
(4)上图是表示第三周期8种元素单质的熔点(℃)柱形图,已知柱形“1”代表Ar,则柱形“8”熔点最高的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】W、X、Y、Z是原子序数依次增大的同一短同期的四种元素。W、X是金属元素,Y、Z是非金属元素。Y的氧化物是现代光学及光纤制品的基本原料。请回答:
(1)Y元素原子结构示意图________________________ 。
(2)将Z单质通入水中,可得到具有漂白作用的溶液,请写出反应的化学方程式:
___________________________________________________________________ 。
(3)0.5 mol X单质与足量W的最高价氧化物对应水化物的溶液发生反应,生成
气体的体积(标准状况)为_________________ 。
(4)WZ是生活中常见的盐,实验室检验该盐中阴离子的操作方法和现象为:取
少量WZ固体溶于水,滴加稀硝酸和硝酸银溶液,若产生白色沉淀,则证明WZ中
有该阴离子。请写出反应的离子方程式:__________________________________
(1)Y元素原子结构示意图
(2)将Z单质通入水中,可得到具有漂白作用的溶液,请写出反应的化学方程式:
(3)0.5 mol X单质与足量W的最高价氧化物对应水化物的溶液发生反应,生成
气体的体积(标准状况)为
(4)WZ是生活中常见的盐,实验室检验该盐中阴离子的操作方法和现象为:取
少量WZ固体溶于水,滴加稀硝酸和硝酸银溶液,若产生白色沉淀,则证明WZ中
有该阴离子。请写出反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】有X、Y、Z三种元素,它们的单质在常温、常压下皆为气体。W单质为固体。
①X单质可在Z单质中燃烧生成XZ,其火焰为苍白色;W单质在Y单质中剧烈燃烧产生黄色火焰,生成淡黄色固体A。
②每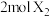 可与
可与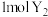 化合生成
化合生成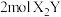 ,
, 在常温下为液体。
在常温下为液体。
③化合物XZ的水溶液可使蓝色石蕊试纸变红;W与水反应后的溶液可使无色酚酞试液变红。
④Z单质溶于化合物 ,所得溶液具有漂白作用;请回答:
,所得溶液具有漂白作用;请回答:
(1)画出W原子的原子结构示意图________________ 。
(2)写出固体A的化学式________________ 。
(3)Z单质与 化学反应方程式:
化学反应方程式:________________ 。
(4)W单质与 化学反应方程式:
化学反应方程式:________________ 。
①X单质可在Z单质中燃烧生成XZ,其火焰为苍白色;W单质在Y单质中剧烈燃烧产生黄色火焰,生成淡黄色固体A。
②每
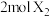 可与
可与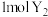 化合生成
化合生成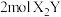 ,
, 在常温下为液体。
在常温下为液体。③化合物XZ的水溶液可使蓝色石蕊试纸变红;W与水反应后的溶液可使无色酚酞试液变红。
④Z单质溶于化合物
 ,所得溶液具有漂白作用;请回答:
,所得溶液具有漂白作用;请回答:(1)画出W原子的原子结构示意图
(2)写出固体A的化学式
(3)Z单质与
 化学反应方程式:
化学反应方程式:(4)W单质与
 化学反应方程式:
化学反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、M、W是原子序数依次增大的前四周期元素,X元素原子核外有三个能级,各能级电子数相等,Y的单质在空气中燃烧生成一种淡黄色的固体;Z元素原子的最外层电子数比次外层电子数少2,M原子外围电子排布式为3dn4sn;W的内层电子已全充满,最外层只有2个电子。
请回答下列问题:
(1)X元素在周期表中的位置是____ ;W2+离子的外围电子排布式为___ 。
(2)X 能与氢、氮、氧三种元素构成化合物 XO(NH2)2,其中X原子和N原子的杂化方式为分别为___ 、___ ,该化合物分子中的π键与σ键的个数之比是____ ;该物质易溶于水的主要原因是___ 。
(3)已知Be和Al元素处于周期表中对角线位置,化学性质相似,请写出Y元素与Be元素两者相应的最高价氧化物对应水化物相互反应的化学方程式:____ 。
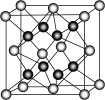
(4)M晶体的原子堆积方式为六方堆积(如图所示),则晶体中M原子的配位数是___ 。某M配合物的化学式是[M(H2O)5Cl]Cl2·H2O,1 mol该配合物中含配位键的数目是____ 。
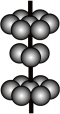
(5)Y离子和Z离子比较,半径较大的是___ (填离子符号),元素Y与元素Z形成的晶体的晶胞结构是如图所示的正方体,每个Y离子周围与它最近的Y离子有___ 个。
请回答下列问题:
(1)X元素在周期表中的位置是
(2)X 能与氢、氮、氧三种元素构成化合物 XO(NH2)2,其中X原子和N原子的杂化方式为分别为
(3)已知Be和Al元素处于周期表中对角线位置,化学性质相似,请写出Y元素与Be元素两者相应的最高价氧化物对应水化物相互反应的化学方程式:
(4)M晶体的原子堆积方式为六方堆积(如图所示),则晶体中M原子的配位数是

(5)Y离子和Z离子比较,半径较大的是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)按要求填空:
①CO2的电子式为:____________________
②基态N原子的轨道表示为________________________________________ ;
③基态Ga原子价电子层的电子排布式为_____________________________ ;
(2)对于A.MgO B.He C.NH3 D.CaO E.干冰 F.Ar五种物质:
①熔沸点最低的是________ ;液态时能导电的是________ (填字母编号)。
②上述物质所含的元素中,基态原子含单电子最多的元素是______ (填元素符号)。
③上述物质的晶体中,属于离子晶体且熔点最高的是____________ (填字母编号)。
④上述物质的晶体熔化时,所克服的微粒间的作用力与冰熔化时所克服的作用力类型完全相同的是______ (填字母编号)。
(3)已知熔融的BeCl2不导电,则BeCl2属于_______ 晶体,中心原子的杂化类型为______ 。
(1)按要求填空:
①CO2的电子式为:
②基态N原子的轨道表示为
③基态Ga原子价电子层的电子排布式为
(2)对于A.MgO B.He C.NH3 D.CaO E.干冰 F.Ar五种物质:
①熔沸点最低的是
②上述物质所含的元素中,基态原子含单电子最多的元素是
③上述物质的晶体中,属于离子晶体且熔点最高的是
④上述物质的晶体熔化时,所克服的微粒间的作用力与冰熔化时所克服的作用力类型完全相同的是
(3)已知熔融的BeCl2不导电,则BeCl2属于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氮及其化合物在自然界中存在循环,请回答下列问题:
(1)氮元素在周期表中的位置是_______ ,氮原子核外电子共占据_______ 个轨道,最外层有_______ 种不同能量的电子。
(2)氨气分子的空间构型为_______ ,氮的最高价氧化物对应水化物的酸性比磷酸的酸性_______ (填“强”或者“弱”)。
(3)工业合成氨反应的化学平衡常数表达式为_______ 。一定条件下,在容积为2L的密闭容器中模拟该反应,测得10min时氮气为0.195mol,请计算0 ~ 10min的氨气的化学反应速率为_______ 。据图判断,反应进行至20 min时,曲线发生变化的原因是_______ (用文字表达)。

(4)工业上用氨水吸收SO2尾气,若最终得到(NH4)2SO4,则该溶液中c(NH )与c(SO
)与c(SO )之比
)之比_______ 2:1(选填“>”、“<”、“=”),请结合离子方程式解释其原因_______ 。
(1)氮元素在周期表中的位置是
(2)氨气分子的空间构型为
(3)工业合成氨反应的化学平衡常数表达式为

(4)工业上用氨水吸收SO2尾气,若最终得到(NH4)2SO4,则该溶液中c(NH
 )与c(SO
)与c(SO )之比
)之比
您最近一年使用:0次



