请写出下列反应的离子方程式:
①氯气与氯化亚铁溶液的反应_________________________________________________
②二氧化锰与浓盐酸反应_______________________________________________________
③氢氧化铝与足量氢氧化钠反应__________________________________________________
④ 偏铝酸钠与过量二氧化碳的反应________________________________________________
①氯气与氯化亚铁溶液的反应
②二氧化锰与浓盐酸反应
③氢氧化铝与足量氢氧化钠反应
④ 偏铝酸钠与过量二氧化碳的反应
12-13高一上·浙江杭州·期末 查看更多[1]
(已下线)2011-2012学年浙江省杭州十四中高一上学期期末化学试卷
更新时间:2012-02-08 23:11:44
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】(I)工业上常用电解饱和食盐水的方法制备氯气,其装置如下图所示:

(1)写出电解饱和食盐水的化学方程式并在化学方程式上标出电子转移的方向和数目:_____ 。
(2)电解时,将Y极(阳极)生成的物质通入盛有NaI溶液的试管中,再加入四氯化碳充分振荡,最后观察到的现象是____________ 。
A.溶液分层,上层无色,下层橙红色
B.溶液分层,上层橙红色,下层无层
C.溶液分层,上层无色,下层紫红色
D.溶液分层,上层紫红色,下层无层
(3)用氯气制备漂白粉,请写出漂白粉长期露置在空气中失效的反应的化学方程式_______ ;____________________________ 。
(II)某同学对实验室制取氯气的装置进行改进,设计了制取无水氯化铁的实验装置图(如下),将浓盐酸滴加到盛有二氧化锰粉末的圆底烧瓶中。请回答下列问题:
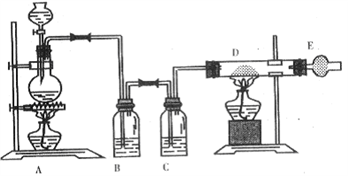
(4)烧瓶中发生反应的化学方程式____________________ ;
(5)产生的气体通过B、C装置,可以得到干燥纯净的氯气,B瓶中的试剂是_____________ ;
(6)如果将过量二氧化锰与20 mL 12 mol·L-1的盐酸混合加热,充分反应后生成的氯气明显少于0.06 mol。其主要原因为______________________________________ 。
(7)玻璃管D中反应现象是_________________ ;写出反应方程式______________________ 。
(8)干燥管E中盛有碱石灰(CaO+NaOH),其作用是__________________ 。

(1)写出电解饱和食盐水的化学方程式并在化学方程式上标出电子转移的方向和数目:
(2)电解时,将Y极(阳极)生成的物质通入盛有NaI溶液的试管中,再加入四氯化碳充分振荡,最后观察到的现象是
A.溶液分层,上层无色,下层橙红色
B.溶液分层,上层橙红色,下层无层
C.溶液分层,上层无色,下层紫红色
D.溶液分层,上层紫红色,下层无层
(3)用氯气制备漂白粉,请写出漂白粉长期露置在空气中失效的反应的化学方程式
(II)某同学对实验室制取氯气的装置进行改进,设计了制取无水氯化铁的实验装置图(如下),将浓盐酸滴加到盛有二氧化锰粉末的圆底烧瓶中。请回答下列问题:

(4)烧瓶中发生反应的化学方程式
(5)产生的气体通过B、C装置,可以得到干燥纯净的氯气,B瓶中的试剂是
(6)如果将过量二氧化锰与20 mL 12 mol·L-1的盐酸混合加热,充分反应后生成的氯气明显少于0.06 mol。其主要原因为
(7)玻璃管D中反应现象是
(8)干燥管E中盛有碱石灰(CaO+NaOH),其作用是
您最近一年使用:0次
【推荐2】请按要求回答下列问题:
(1)实验室二氧化锰和浓盐酸在加热条件下制取Cl2,其中 MnO2 是__________ 剂;反应中氯化氢体现了_____________ 性和 _______________ 性。
(2)室温下KClO3 与浓盐酸反应制取氯气的化学方程式:KClO3+6HCl(浓)=KCl+3Cl2+3H2O请在上式中用单线桥法表示出得失电子的情况。___
(3)用CuCl2作催化剂,在450℃时用空气中的O2 跟 HCl 反应也能制得氯气,其化学方程式:4HCl+O2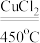 2H2O+2Cl2,从以上3种制备的方法中,可以认为氧化剂的氧化能力从强到弱的顺序为
2H2O+2Cl2,从以上3种制备的方法中,可以认为氧化剂的氧化能力从强到弱的顺序为________ 。
(4)把 Cl2 通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2请在上式用双线桥表示反应的电子转移方向和数目___ ;反应中氧化剂与还原剂分子数之比为 ___ 。若反应中有 6.8 g NH3 发生氧化反应,则反应中生成的 N2 质量为 __________ g。
(1)实验室二氧化锰和浓盐酸在加热条件下制取Cl2,其中 MnO2 是
(2)室温下KClO3 与浓盐酸反应制取氯气的化学方程式:KClO3+6HCl(浓)=KCl+3Cl2+3H2O请在上式中用单线桥法表示出得失电子的情况。
(3)用CuCl2作催化剂,在450℃时用空气中的O2 跟 HCl 反应也能制得氯气,其化学方程式:4HCl+O2
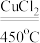 2H2O+2Cl2,从以上3种制备的方法中,可以认为氧化剂的氧化能力从强到弱的顺序为
2H2O+2Cl2,从以上3种制备的方法中,可以认为氧化剂的氧化能力从强到弱的顺序为(4)把 Cl2 通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2请在上式用双线桥表示反应的电子转移方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.(1)如图是温度计、量筒的一部分,其中____ (填“①”或“②”)是量筒,读数为______ mL。
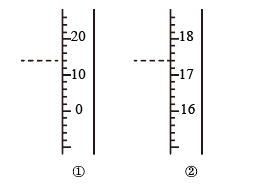
II.如图是实验室制取氯气的装置图。请回答下列问题:

(2)若要除去Cl2中可能混有的少量HCl气体,乙中应盛有___________
(3)KMnO4和浓盐酸在常温下反应也能产生与甲中产物相同的气体,发生反应的离子方程式为_________ 。
(4)小李同学在一次实验中发现:把新制氯水逐滴加到含有酚酞的氢氧化钠溶液中,当加到最后一滴时溶液的红色突然消失。
①推测:对此现象,你的推测是:
i.是氯水中的次氯酸氧化了酚酞,使酚酞由红色变为无色。ii.__________ 。
②查阅资料:你认为小李在实验过程中需要已知或查阅的资料内容包括(填字母代号)____ 。
a.氯水的成分及性质 b.酚酞的化学式 c.使酚酞变红色时溶液的pH值
③设计实验:向已褪色的溶液中继续滴加 NaOH 溶液,若实验中_____________ ,则证明推测 i 是正确的;若实验中__________ ,则证明推测ii是正确的。

II.如图是实验室制取氯气的装置图。请回答下列问题:

(2)若要除去Cl2中可能混有的少量HCl气体,乙中应盛有
(3)KMnO4和浓盐酸在常温下反应也能产生与甲中产物相同的气体,发生反应的离子方程式为
(4)小李同学在一次实验中发现:把新制氯水逐滴加到含有酚酞的氢氧化钠溶液中,当加到最后一滴时溶液的红色突然消失。
①推测:对此现象,你的推测是:
i.是氯水中的次氯酸氧化了酚酞,使酚酞由红色变为无色。ii.
②查阅资料:你认为小李在实验过程中需要已知或查阅的资料内容包括(填字母代号)
a.氯水的成分及性质 b.酚酞的化学式 c.使酚酞变红色时溶液的pH值
③设计实验:向已褪色的溶液中继续滴加 NaOH 溶液,若实验中
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】现有部分元素的性质与原子(或分子)结构如下表所示:
(1)画出元素T的原子结构示意图:_________________ 。
(2)元素Y与Z相比金属性较强的是Y,下列不能证明这一事实的是____ (填字母)。
a.Y的最外层电子数比Z少
b.Y单质与水反应比Z单质与水反应剧烈
c.Y最高价氧化物对应的水化物的碱性比Z的强
(3)写出X形成单质的电子式_________________ 。(用元素符号表示)
(4)T可以形成稳定的阴离子Tm-,Y可以形成稳定的阳离子Yn+,其半径关系为r(Tm-)______ r(Yn+)(填“>”,“<”或“=”)
(5)X、Y、Z的最高价氧化物对应的水化物可以相互发生反应,写出Y、Z的最高价氧化物对应的水化物之间反应的离子方程式___________________________ 。
| 元素编号 | 元素性质与原子(或分子)结构 |
| T | 最外层电子数是次外层电子数的3倍 |
| X | 最高正价与最低负价的代数和为2,常温下单质为气体 |
| Y | M层比K层少1个电子 |
| Z | 第三周期元素的金属离子中半径最小 |
(1)画出元素T的原子结构示意图:
(2)元素Y与Z相比金属性较强的是Y,下列不能证明这一事实的是
a.Y的最外层电子数比Z少
b.Y单质与水反应比Z单质与水反应剧烈
c.Y最高价氧化物对应的水化物的碱性比Z的强
(3)写出X形成单质的电子式
(4)T可以形成稳定的阴离子Tm-,Y可以形成稳定的阳离子Yn+,其半径关系为r(Tm-)
(5)X、Y、Z的最高价氧化物对应的水化物可以相互发生反应,写出Y、Z的最高价氧化物对应的水化物之间反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水中后有1.16g白色沉淀,在所得的悬浊液中逐滴加入1mol·L-1HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示。试回答:
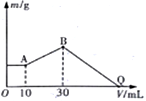
(1)A点沉淀物的化学式为_____________ ,A点溶液中的溶质是___________________ ;B点沉淀物的化学式为____________________ 。
(2)原混合物中MgCl2的物质的量为________________ ,AlCl3的物质的量为__________ ,NaOH的物质的量为________________ 。
(3)HCl溶液在Q点的加入量是____________________ 。

(1)A点沉淀物的化学式为
(2)原混合物中MgCl2的物质的量为
(3)HCl溶液在Q点的加入量是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某溶液中可能含有 、
、 、
、 、
、 、
、 、
、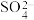 等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的质量随加入的NaOH的物质的量的变化如图所示:
等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的质量随加入的NaOH的物质的量的变化如图所示:

(1)由此可知,该溶液中肯定含有的离子是______________________________________ ,且各离子的物质的量之比为___________________________________________
(2)该溶液中肯定不含的阳离子是________________ 。
(3)写出NaOH的物质的量从8mol到9mol发生的离子反应方程式:____________________________
 、
、 、
、 、
、 、
、 、
、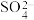 等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的质量随加入的NaOH的物质的量的变化如图所示:
等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的质量随加入的NaOH的物质的量的变化如图所示: 
(1)由此可知,该溶液中肯定含有的离子是
(2)该溶液中肯定不含的阳离子是
(3)写出NaOH的物质的量从8mol到9mol发生的离子反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求写出反应的化学方程式或离子方程式,属于离子反应的必须写离子方程式:
(1)除去Na2CO3固体中的NaHCO3_______ ;
(2)向NaAlO2溶液中通入过量的CO2_______ ;
(3)向NaOH溶液中滴加少量的AlCl3_______ ;
(4)铝与NaOH溶液反应_______ ;
(5)AlCl3溶液与NaAlO2溶液混合_______ ;
(6)Al2(SO4)3溶液中滴加过量氨水_______ 。
(1)除去Na2CO3固体中的NaHCO3
(2)向NaAlO2溶液中通入过量的CO2
(3)向NaOH溶液中滴加少量的AlCl3
(4)铝与NaOH溶液反应
(5)AlCl3溶液与NaAlO2溶液混合
(6)Al2(SO4)3溶液中滴加过量氨水
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求填空:
(1)常用作制冷剂的物质的电子式_______ ;
(2)氮气常用作保护气,但是氮气不能用作金属镁的保护气,其原因用化学方程式表示是_______ ;
(3)浓氨水可以检验输送氯气的管道是否泄露,若泄露则会产生白烟,其原理用化学方程式表示为_______ ;
(4)铵盐与NaOH等强碱的溶液在加热条件下反应的离子方程式是_______ ;
(5)汽车尾气(含有烃类、CO、SO2、NO等物质)是城市空气的污染源之一,治理的方法之一是在汽车的排气管上装一个“催化转换器”,使CO和NO转化为无毒气体,其反应方程式为_______ ;
(6)铝土矿(主要成分为Al2O3,含有少量杂质)是提取铝的原料。提取铝的工艺流程如下:

请用离子方程式表示以上工艺流程中第①步反应:_______ ;写出以上工艺流程中第③步反应的化学方程式:_______ ;若第①步加入的是盐酸,则发生反应的离子方程式为_______ 。
(1)常用作制冷剂的物质的电子式
(2)氮气常用作保护气,但是氮气不能用作金属镁的保护气,其原因用化学方程式表示是
(3)浓氨水可以检验输送氯气的管道是否泄露,若泄露则会产生白烟,其原理用化学方程式表示为
(4)铵盐与NaOH等强碱的溶液在加热条件下反应的离子方程式是
(5)汽车尾气(含有烃类、CO、SO2、NO等物质)是城市空气的污染源之一,治理的方法之一是在汽车的排气管上装一个“催化转换器”,使CO和NO转化为无毒气体,其反应方程式为
(6)铝土矿(主要成分为Al2O3,含有少量杂质)是提取铝的原料。提取铝的工艺流程如下:

请用离子方程式表示以上工艺流程中第①步反应:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I.除去括号中的杂质(填试剂)
(1)CuCl2溶液(FeCl3)_________________________ ;
(2)Fe2(SO4) 3溶液( FeSO4)_______________________ ;
(3)NaHCO3溶液(Na2CO3)___________________ ;
(4)CO2(HCl)_________________________ ;
Ⅱ写出下列反应的离子方程式
(5)二氧化硫使溴水褪色的原理_________________________________ ;
(6)将NaHCO3溶液与澄清石灰水等物质的量混合_________________________________ ;
(7)向NaAlO2溶液中通入过量CO2气体__________________________________________ ;
(8)FeBr2溶液和等物质的量的Cl2反应_________________________________________ 。
(1)CuCl2溶液(FeCl3)
(2)Fe2(SO4) 3溶液( FeSO4)
(3)NaHCO3溶液(Na2CO3)
(4)CO2(HCl)
Ⅱ写出下列反应的离子方程式
(5)二氧化硫使溴水褪色的原理
(6)将NaHCO3溶液与澄清石灰水等物质的量混合
(7)向NaAlO2溶液中通入过量CO2气体
(8)FeBr2溶液和等物质的量的Cl2反应
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】现有五种溶液,分别含下列离子:①Ag+、②Mg2+、③Fe2+、④Al3+、⑤Fe3+。
(1)写出符合下列条件的离子符号:既能被氧化又能被还原的离子是______ ,遇KSCN溶液显血红色的是______ ,加铁粉后溶液增重的是______ ;
(2)向③的溶液中滴加NaOH溶液,现象是______________________ ,写出此步操作属于氧化还原反应的化学方程式_____________________ 。
(1)写出符合下列条件的离子符号:既能被氧化又能被还原的离子是
(2)向③的溶液中滴加NaOH溶液,现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱溶液反应制得Fe(OH)2白色沉淀。若用下图所示实验装置,则可制得纯净的Fe(OH)2白色沉淀。已知两极材料分别为石墨和铁:
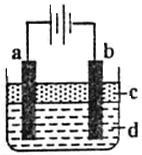
(1)a极材料为______ ,a电极反应式为______ 。
(2)电解液d可以是______ ,则白色沉淀在电极上生成;电解液d也可以是______ ,则白色沉淀在两极间的溶液中生成。
A.纯水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
(3)液体c为苯,其作用是______ ,在加苯之前对d溶液进行加热煮沸处理,目的是______ 。
(4)为了在短时间内看到白色沉淀,可以采取的措施是______ 。
A.改用H2SO4作电解液 B.适当增大电源电压
C.适当缩小两极间距离 D.适当地降低电解液的温度
(5)若d改为Na2SO4溶液,当电解一段时间,看到白色沉淀后,再反接电源继续电解,除了电极上看到的气泡外,另一明显的现象为______ 。

(1)a极材料为
(2)电解液d可以是
A.纯水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
(3)液体c为苯,其作用是
(4)为了在短时间内看到白色沉淀,可以采取的措施是
A.改用H2SO4作电解液 B.适当增大电源电压
C.适当缩小两极间距离 D.适当地降低电解液的温度
(5)若d改为Na2SO4溶液,当电解一段时间,看到白色沉淀后,再反接电源继续电解,除了电极上看到的气泡外,另一明显的现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】铁是人类较早使用的金属之一,运用所学知识,回答下列问题。
I.某学习小组研究 腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
(1)从 腐蚀铜后的废液中回收铜,并获得
腐蚀铜后的废液中回收铜,并获得 溶液,设计如下方案:
溶液,设计如下方案:
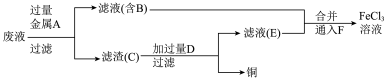
滤渣C中所含物质的化学式为___________ ;通入F发生反应的离子方程式为___________ 。
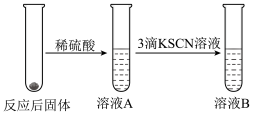
II.学习小组同学继续研究铁与水蒸气的反应,分别进行了如图实验。
请回答:
(2)实验I中反应的化学方程式是___________ 。
(3)甲同学观察到实验I中持续产生肥皂泡,但实验II中溶液B未呈现红色,则溶液B未呈现红色的原因是___________ 。(写出反应的离子方程式)
(4)实验室在制备 时必须隔绝空气,否则发生的现象是
时必须隔绝空气,否则发生的现象是___________ ;反应化学方程式为___________ 。
I.某学习小组研究
 腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
腐蚀铜后所得的废液成分并回收铜,进行了如下实验:(1)从
 腐蚀铜后的废液中回收铜,并获得
腐蚀铜后的废液中回收铜,并获得 溶液,设计如下方案:
溶液,设计如下方案:
滤渣C中所含物质的化学式为
II.学习小组同学继续研究铁与水蒸气的反应,分别进行了如图实验。
| 实验I | 实验II |
 |  |
(2)实验I中反应的化学方程式是
(3)甲同学观察到实验I中持续产生肥皂泡,但实验II中溶液B未呈现红色,则溶液B未呈现红色的原因是
(4)实验室在制备
 时必须隔绝空气,否则发生的现象是
时必须隔绝空气,否则发生的现象是
您最近一年使用:0次



