铁是人类较早使用的金属之一,运用所学知识,回答下列问题。
I.某学习小组研究 腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
(1)从 腐蚀铜后的废液中回收铜,并获得
腐蚀铜后的废液中回收铜,并获得 溶液,设计如下方案:
溶液,设计如下方案:
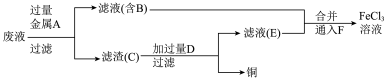
滤渣C中所含物质的化学式为___________ ;通入F发生反应的离子方程式为___________ 。
II.学习小组同学继续研究铁与水蒸气的反应,分别进行了如图实验。
请回答:
(2)实验I中反应的化学方程式是___________ 。
(3)甲同学观察到实验I中持续产生肥皂泡,但实验II中溶液B未呈现红色,则溶液B未呈现红色的原因是___________ 。(写出反应的离子方程式)
(4)实验室在制备 时必须隔绝空气,否则发生的现象是
时必须隔绝空气,否则发生的现象是___________ ;反应化学方程式为___________ 。
I.某学习小组研究
 腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
腐蚀铜后所得的废液成分并回收铜,进行了如下实验:(1)从
 腐蚀铜后的废液中回收铜,并获得
腐蚀铜后的废液中回收铜,并获得 溶液,设计如下方案:
溶液,设计如下方案:
滤渣C中所含物质的化学式为
II.学习小组同学继续研究铁与水蒸气的反应,分别进行了如图实验。
| 实验I | 实验II |
 | 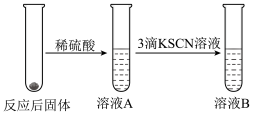 |
(2)实验I中反应的化学方程式是
(3)甲同学观察到实验I中持续产生肥皂泡,但实验II中溶液B未呈现红色,则溶液B未呈现红色的原因是
(4)实验室在制备
 时必须隔绝空气,否则发生的现象是
时必须隔绝空气,否则发生的现象是
更新时间:2023-04-26 10:47:57
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】元素的价类二维图是我们学习元素及其化合物相关知识的重要模型和工具。如图是钠的价类二维图:
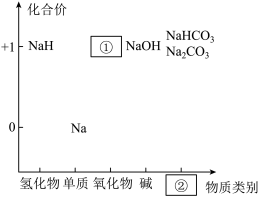
(1)②处应填的物质类别是___________ ;
(2)将钠放入水中发生反应的离子方程式是___________ ;
(3)Na可用石蜡封存,实验室少量Na保存于___________ 中;
(4)将Na2O2投入盛有CuSO4溶液的烧杯中,观察到的现象是___________(填标号);
(5)向酸性KMnO4溶液中加入Na2O2粉末,观察到溶液褪色,发生如下反应:
____ +____Na2O2+______→ ______Mn2++______Na++_____+_____H2O(未配平)
+____Na2O2+______→ ______Mn2++______Na++_____+_____H2O(未配平)
首先请补全方程式并配平__________ ,然后回答反应中被还原的元素是___________ ;反应中每消耗1molNa2O2的同时有___________ mol电子转移。

(1)②处应填的物质类别是
(2)将钠放入水中发生反应的离子方程式是
(3)Na可用石蜡封存,实验室少量Na保存于
(4)将Na2O2投入盛有CuSO4溶液的烧杯中,观察到的现象是___________(填标号);
| A.有气体生成 | B.无气体生成 | C.有蓝色沉淀生成 | D.大量红色固体铜生成 |
(5)向酸性KMnO4溶液中加入Na2O2粉末,观察到溶液褪色,发生如下反应:
____
 +____Na2O2+______→ ______Mn2++______Na++_____+_____H2O(未配平)
+____Na2O2+______→ ______Mn2++______Na++_____+_____H2O(未配平)首先请补全方程式并配平
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】常温下,几种弱酸的电离平衡常数如下,根据表中数据回答下列问题:
(1)25℃时,某浓度的NaCN水溶液的 ,原因是
,原因是___________ (用离子方程式表示),该溶液中由水电离产生的 的浓度为
的浓度为___________ 。
(2)25℃时,向NaCN溶液中通入少量 ,反应的离子方程式为
,反应的离子方程式为___________ 。
(3) 溶液中各离子浓度由大到小的顺序是
溶液中各离子浓度由大到小的顺序是___________ 。
(4)25℃时,体积相同、 相同的三种酸溶液:a.HCOOH;b.HCN;c.HCl分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的顺序是
相同的三种酸溶液:a.HCOOH;b.HCN;c.HCl分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的顺序是___________ (填字母)。
| 化学式 |  | HCN | HCOOH |
| 电离平衡常数 |   | 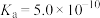 |  |
 ,原因是
,原因是 的浓度为
的浓度为(2)25℃时,向NaCN溶液中通入少量
 ,反应的离子方程式为
,反应的离子方程式为(3)
 溶液中各离子浓度由大到小的顺序是
溶液中各离子浓度由大到小的顺序是(4)25℃时,体积相同、
 相同的三种酸溶液:a.HCOOH;b.HCN;c.HCl分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的顺序是
相同的三种酸溶液:a.HCOOH;b.HCN;c.HCl分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】请按照要求完成下列方程式。
(1)写出泡沫灭火器反应原理的离子方程式:______________________ 。
(2)铁与水蒸气高温下反应的化学反应方程式:_____________________________ 。
(3)NaCN属于剧毒物质,有一种处理方法其原理为CN-与 反应生成两种离子,一种与Fe3+可生成红色溶液,另一种与H+作用产生能使品红溶液褪色的刺激性气体,写出CN-与
反应生成两种离子,一种与Fe3+可生成红色溶液,另一种与H+作用产生能使品红溶液褪色的刺激性气体,写出CN-与 反应离子反应方程式:
反应离子反应方程式:________________________ 。
(4)亚硝酸盐毒性较强的物质,其具有较强的还原性,将亚硝酸钠溶液滴加到K2Cr2O7酸性溶液(橙色)中,溶液由橙色交为绿色(Cr3+),试写出反应的离子方程式_______ 。
(5)将NaHSO4溶液滴入氢氧化钡溶液中至中性的离子反应方程式:________ 。
(1)写出泡沫灭火器反应原理的离子方程式:
(2)铁与水蒸气高温下反应的化学反应方程式:
(3)NaCN属于剧毒物质,有一种处理方法其原理为CN-与
 反应生成两种离子,一种与Fe3+可生成红色溶液,另一种与H+作用产生能使品红溶液褪色的刺激性气体,写出CN-与
反应生成两种离子,一种与Fe3+可生成红色溶液,另一种与H+作用产生能使品红溶液褪色的刺激性气体,写出CN-与 反应离子反应方程式:
反应离子反应方程式:(4)亚硝酸盐毒性较强的物质,其具有较强的还原性,将亚硝酸钠溶液滴加到K2Cr2O7酸性溶液(橙色)中,溶液由橙色交为绿色(Cr3+),试写出反应的离子方程式
(5)将NaHSO4溶液滴入氢氧化钡溶液中至中性的离子反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】请回答下列问题:
(1)2 mol的CO2与3 mol的SO3的分子数比是_______ ;原子数比是_______ 。
(2)9.5 g某二价金属氯化物(ACl2)中含有0.2 molCl-,则A的摩尔质量是___________ 。
(3)铁与蒸汽反应的化学方程式_____________________________________ ;
(4)实验室以二氧化锰为原料制氯气的离子方程式____________________________________ 。
(5)中国的瓷器驰名世界,制备陶瓷是以粘土[主要成分Al2Si2O5(OH)4]为原料,经高温烧结而成.若以氧化物形式表示粘土的组成,应写为_________________________ 。
(1)2 mol的CO2与3 mol的SO3的分子数比是
(2)9.5 g某二价金属氯化物(ACl2)中含有0.2 molCl-,则A的摩尔质量是
(3)铁与蒸汽反应的化学方程式
(4)实验室以二氧化锰为原料制氯气的离子方程式
(5)中国的瓷器驰名世界,制备陶瓷是以粘土[主要成分Al2Si2O5(OH)4]为原料,经高温烧结而成.若以氧化物形式表示粘土的组成,应写为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】“生活无处不化学”,请你回答下列问题。
(1)厨房中的调味品,①盐(主要成分氯化钠)、②碱面(主要成分碳酸钠)、③白醋(主要成分乙酸)。主要成分中具有碱性的是_____ (填序号,下同);属于盐类的是______ ;相互间能发生反应的是________ 。
(2)食盐不慎洒落在天然气的火焰上,观察的现象是_______________ ,该变化称为______ 反应。
(3)沾有水的铁制器皿在高温火焰上会发黑,该反应的化学方程式是__________________ 。
(4)家庭中常用“84”消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。
“消毒液”与“洁厕灵”同时使用会产生有毒的氯气,写出该反应的离子方程式:____________________________________________ 。
(5)纯碱(Na2CO3)、小苏打(NaHCO3)广泛应用在食品加工。苏打饼干原料中含有小苏打,在烘焙受热过程中,小苏打发生分解反应,该反应的化学方程式是_____________________________________ ;苏打饼干可以适当缓解人体胃酸(主要成分盐酸)过多症状,该反应的离子方程式是__________________________________________ 。
(6)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:______________ 。
(1)厨房中的调味品,①盐(主要成分氯化钠)、②碱面(主要成分碳酸钠)、③白醋(主要成分乙酸)。主要成分中具有碱性的是
(2)食盐不慎洒落在天然气的火焰上,观察的现象是
(3)沾有水的铁制器皿在高温火焰上会发黑,该反应的化学方程式是
(4)家庭中常用“84”消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。
“消毒液”与“洁厕灵”同时使用会产生有毒的氯气,写出该反应的离子方程式:
(5)纯碱(Na2CO3)、小苏打(NaHCO3)广泛应用在食品加工。苏打饼干原料中含有小苏打,在烘焙受热过程中,小苏打发生分解反应,该反应的化学方程式是
(6)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】铁及其化合物在生产和生活中有着广泛的应用。
(1)铁元素在元素周期表中的位置为_____ 。
(2)等物质的量的铁分别与足量的盐酸、水蒸气在一定条件下反应,产生相同条件下的气体体积比为_____ ,铁在高温条件下与水蒸气反应的化学方程式为______________ 。
(3)高铁酸钾(K2FeO4)也是常用的水处理剂。它的制备方法有多种:其中熔融法又称为过氧化钠氧化法。先在高温熔融的条件下制备高铁酸钠:Fe+3Na2O2 Na2FeO4+2Na2O,再将高铁酸钠加入到氢氧化钾溶液里,发生反应:2KOH+Na2FeO4=K2FeO4+2NaOH,请根据复分解反应原理分析该反应发生的原因:
Na2FeO4+2Na2O,再将高铁酸钠加入到氢氧化钾溶液里,发生反应:2KOH+Na2FeO4=K2FeO4+2NaOH,请根据复分解反应原理分析该反应发生的原因:_______________________________________ 。
(1)铁元素在元素周期表中的位置为
(2)等物质的量的铁分别与足量的盐酸、水蒸气在一定条件下反应,产生相同条件下的气体体积比为
(3)高铁酸钾(K2FeO4)也是常用的水处理剂。它的制备方法有多种:其中熔融法又称为过氧化钠氧化法。先在高温熔融的条件下制备高铁酸钠:Fe+3Na2O2
 Na2FeO4+2Na2O,再将高铁酸钠加入到氢氧化钾溶液里,发生反应:2KOH+Na2FeO4=K2FeO4+2NaOH,请根据复分解反应原理分析该反应发生的原因:
Na2FeO4+2Na2O,再将高铁酸钠加入到氢氧化钾溶液里,发生反应:2KOH+Na2FeO4=K2FeO4+2NaOH,请根据复分解反应原理分析该反应发生的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如图所示装置可用来制取和观察氢氧化亚铁在空气中被氧化时颜色的变化。实验时必须使用铁屑和6mol/L的硫酸,其他试剂任选。
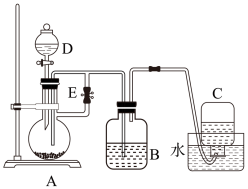
(1)实验开始时就先将止水夹E_______ 。(填“打开”或“关闭”)
(2)待装置B中出现较多白色沉淀时,拔去装置B中的橡皮塞,使空气进入,写出白色沉淀变为红褐色沉淀的化学方程式:_______ 。

(1)实验开始时就先将止水夹E
(2)待装置B中出现较多白色沉淀时,拔去装置B中的橡皮塞,使空气进入,写出白色沉淀变为红褐色沉淀的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】请回答下列问题:
(1)钠在空气中燃烧生成淡黄色的____ (填“Na2O”或“Na2O2”);
(2)A12O3能溶于酸或强碱溶液生成盐和水,则Al2O3是一种____ (填“酸性”、“碱性”或“两性”)氧化物:
(3)除去SiO2中的CaCO3杂质所选用的试剂是____ 。
(4)用亚铁盐制备氢氧化亚铁时,因氢氧化亚铁易发生氧化反应而难以观察到“真实面目”,写出其在空气中发生氧化反应的化学方程式____ 。
(1)钠在空气中燃烧生成淡黄色的
(2)A12O3能溶于酸或强碱溶液生成盐和水,则Al2O3是一种
(3)除去SiO2中的CaCO3杂质所选用的试剂是
(4)用亚铁盐制备氢氧化亚铁时,因氢氧化亚铁易发生氧化反应而难以观察到“真实面目”,写出其在空气中发生氧化反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】油画的白色燃料中曾含二价铅盐,二价铅盐经过长时间空气(含有微量 )的侵蚀,生成
)的侵蚀,生成 而变黑。可用一定量的
而变黑。可用一定量的 溶液擦洗修复,完成下列填空:
溶液擦洗修复,完成下列填空:
(1) 与
与 反应生成
反应生成 的和
的和 ,写出该反应的化学方程式
,写出该反应的化学方程式_______ 。
(2)在 的悬浊液中滴加一定量的
的悬浊液中滴加一定量的 溶液,发生复分解反应,溶液变为澄清,有弱电解质生成,写出该反应的离子反应方程式
溶液,发生复分解反应,溶液变为澄清,有弱电解质生成,写出该反应的离子反应方程式_______ 。上述反应之所以发生,其本质原因是_______ 。
(3) 为二元弱酸,向
为二元弱酸,向 溶液中通入过量
溶液中通入过量 气体,离子反应方程式为
气体,离子反应方程式为_______ 。 溶液又称臭碱,其中加入
溶液又称臭碱,其中加入 溶液,生成黑色
溶液,生成黑色 沉淀,还可能生成白色沉淀,其化学式为
沉淀,还可能生成白色沉淀,其化学式为_______ ,该物质在空气中很快变为红褐色。
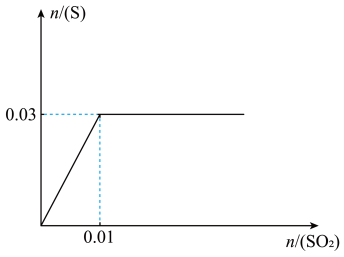
(4)向 溶液中缓慢通入
溶液中缓慢通入 ,发生反应
,发生反应 ,生成
,生成 的物质的量与通入
的物质的量与通入 的物质的量的关系如图(溶液体积变化忽略不计),由此可知原溶液中
的物质的量的关系如图(溶液体积变化忽略不计),由此可知原溶液中 的物质的量浓度为
的物质的量浓度为_______ 。从开始通 至饱和,再继续通一段时间,整个过程中
至饱和,再继续通一段时间,整个过程中 的变化情况为
的变化情况为_______ 。
 )的侵蚀,生成
)的侵蚀,生成 而变黑。可用一定量的
而变黑。可用一定量的 溶液擦洗修复,完成下列填空:
溶液擦洗修复,完成下列填空:(1)
 与
与 反应生成
反应生成 的和
的和 ,写出该反应的化学方程式
,写出该反应的化学方程式(2)在
 的悬浊液中滴加一定量的
的悬浊液中滴加一定量的 溶液,发生复分解反应,溶液变为澄清,有弱电解质生成,写出该反应的离子反应方程式
溶液,发生复分解反应,溶液变为澄清,有弱电解质生成,写出该反应的离子反应方程式(3)
 为二元弱酸,向
为二元弱酸,向 溶液中通入过量
溶液中通入过量 气体,离子反应方程式为
气体,离子反应方程式为 溶液又称臭碱,其中加入
溶液又称臭碱,其中加入 溶液,生成黑色
溶液,生成黑色 沉淀,还可能生成白色沉淀,其化学式为
沉淀,还可能生成白色沉淀,其化学式为(4)向
 溶液中缓慢通入
溶液中缓慢通入 ,发生反应
,发生反应 ,生成
,生成 的物质的量与通入
的物质的量与通入 的物质的量的关系如图(溶液体积变化忽略不计),由此可知原溶液中
的物质的量的关系如图(溶液体积变化忽略不计),由此可知原溶液中 的物质的量浓度为
的物质的量浓度为 至饱和,再继续通一段时间,整个过程中
至饱和,再继续通一段时间,整个过程中 的变化情况为
的变化情况为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】阅读下面两条科普信息,回答问题:
①一个体重50kg的健康人含铁2g,这2g铁在人体中不是以单质金属的形式存在,而是以Fe2+和Fe3+的形式存在.亚铁离子易被吸收,给贫血者补充铁时,应给予含亚离子的亚铁盐,如硫酸亚铁.服用维生素C,可使食物中的铁离子还原成亚铁离子,有于人体吸收。
②在新生代的海水里有一种铁细菌,它们提取海水中的亚铁离子,利用酶为催化剂把它转变成它们的皮鞘(可以用Fe2O3来表示其中的铁),后来便沉积下来形成铁矿;该反应的另一种反应物是CO2,反应后CO2转变成有机物甲醛:(用CH2O表示)。
问题:
这两则科普信息分别介绍了人体内和海水中的亚铁离子与铁离子(或者铁的高价化合物)相互转化的事实、方法和途径
(1)能在人体进行Fe2+和Fe3+的转化,这说明亚铁离子具有_________ 性,铁离子具有_________ 性;
(2)服用维生素C,可以使食物中的Fe3+还原成Fe2+,这句话指出维生素C是_______ 剂,具有_______ 性;
(3)市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化成亚铁盐。此反应的化学方程式为_________ ;离子方程式为:__________ 。
(4)第②条信息中的CO2做__________ 剂,写出②中的离子方程式_________ 。
①一个体重50kg的健康人含铁2g,这2g铁在人体中不是以单质金属的形式存在,而是以Fe2+和Fe3+的形式存在.亚铁离子易被吸收,给贫血者补充铁时,应给予含亚离子的亚铁盐,如硫酸亚铁.服用维生素C,可使食物中的铁离子还原成亚铁离子,有于人体吸收。
②在新生代的海水里有一种铁细菌,它们提取海水中的亚铁离子,利用酶为催化剂把它转变成它们的皮鞘(可以用Fe2O3来表示其中的铁),后来便沉积下来形成铁矿;该反应的另一种反应物是CO2,反应后CO2转变成有机物甲醛:(用CH2O表示)。
问题:
这两则科普信息分别介绍了人体内和海水中的亚铁离子与铁离子(或者铁的高价化合物)相互转化的事实、方法和途径
(1)能在人体进行Fe2+和Fe3+的转化,这说明亚铁离子具有
(2)服用维生素C,可以使食物中的Fe3+还原成Fe2+,这句话指出维生素C是
(3)市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化成亚铁盐。此反应的化学方程式为
(4)第②条信息中的CO2做
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某同学用如下实验探究Fe2+、Fe3+的性质。请回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol·L-1的溶液,在FeCl3溶液中需加入少量铁屑,发生反应的化学方程式为_______ 。
(2)甲同学取2 mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化,FeCl2溶液与氯水反应的化学方程式为_______ 。
(3)乙同学认为甲同学的实验不够严谨,该同学在2 mL FeCl2溶液中先加入0.5 mL煤油,再于液面下依次加入1滴KSCN溶液和几滴氯水,溶液变红,煤油的作用是_______ 。
(4)丁同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为_______ 。
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol·L-1的溶液,在FeCl3溶液中需加入少量铁屑,发生反应的化学方程式为
(2)甲同学取2 mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化,FeCl2溶液与氯水反应的化学方程式为
(3)乙同学认为甲同学的实验不够严谨,该同学在2 mL FeCl2溶液中先加入0.5 mL煤油,再于液面下依次加入1滴KSCN溶液和几滴氯水,溶液变红,煤油的作用是
(4)丁同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知某水泥样品的主要成分为成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物。现一实验小组利用实验室中的几种药品对该水泥样品进行检测,以确定其中各金属元素的含量
(1)取水泥样品10.0g,加入足量稀盐酸、氯化铵,使之完全溶解。待充分反应后发现仍有不溶物。将沉淀过滤后加热、干燥,所得固体为________ (填化学式)
(2)在分析水泥样品溶解过滤后的滤液成分时,实验小组的同学认为其中含有Ca2+、Al3+、Mg2+、Fe2+、Fe3+等阳离子,现欲准确测量各成分含量,需先加入试剂X将Fe2+转化为Fe3+,待滤液中的Fe2+全部转化为Fe3+后,再向其中加入足量的溶液Y并加热,可使滤液中的Al3+、Mg2+、Fe3+全部形成沉淀,则溶液Y名称是________ ,而试剂X可选用下列物质中的__________ (填选项)
a. HNO3 b. H2O2 c. KMnO4 d. Zn
(3)若将溶液Y改为氢氧化钠溶液,发现所得沉淀共1.008g,比原来减少了0.39g,而这些沉淀能恰好完全溶解于1mol/L,32mL的稀盐酸中,则上述说法中所涉及的水泥样品中金属元素种类及其分别占水泥样品的质量分数为____________ 、_____________ 、______________
(4)若最初的水泥样品改为用氢氧化钠溶液溶解,则可能发生的离子反应方程式是:________
(1)取水泥样品10.0g,加入足量稀盐酸、氯化铵,使之完全溶解。待充分反应后发现仍有不溶物。将沉淀过滤后加热、干燥,所得固体为
(2)在分析水泥样品溶解过滤后的滤液成分时,实验小组的同学认为其中含有Ca2+、Al3+、Mg2+、Fe2+、Fe3+等阳离子,现欲准确测量各成分含量,需先加入试剂X将Fe2+转化为Fe3+,待滤液中的Fe2+全部转化为Fe3+后,再向其中加入足量的溶液Y并加热,可使滤液中的Al3+、Mg2+、Fe3+全部形成沉淀,则溶液Y名称是
a. HNO3 b. H2O2 c. KMnO4 d. Zn
(3)若将溶液Y改为氢氧化钠溶液,发现所得沉淀共1.008g,比原来减少了0.39g,而这些沉淀能恰好完全溶解于1mol/L,32mL的稀盐酸中,则上述说法中所涉及的水泥样品中金属元素种类及其分别占水泥样品的质量分数为
(4)若最初的水泥样品改为用氢氧化钠溶液溶解,则可能发生的离子反应方程式是:
您最近一年使用:0次



