用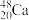 轰击
轰击 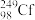 ,生成
,生成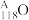 g并放出3个中子(
g并放出3个中子( )。
)。
(1)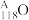 g的原子核内中子数是
g的原子核内中子数是_______ 。
(2)推测Og在元素周期表的位置_______ 。
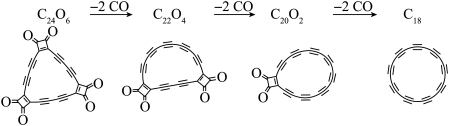
(3)2019年科学家首次合成全碳的环形分子,下列说法正确的是_______
(4)写出实验室制取氯气的化学方程式_______ ;
(5)在383K时,将二氧化锰溶解于浓硫酸中,可得硫酸锰[ Mn2 ( SO4)3]并放出氧气。试写出该反应的化学方程式_______ ;
(6)已知铋酸钠( NaBiO3 )是一种浅黄色的粉末,不溶于冷水,它可以在高酸度的溶液中将Mn2+氧化成 ,自身被还原成Bi3+。试写出该反应的离子方程式
,自身被还原成Bi3+。试写出该反应的离子方程式_______ 。
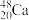 轰击
轰击 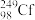 ,生成
,生成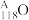 g并放出3个中子(
g并放出3个中子( )。
)。(1)
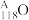 g的原子核内中子数是
g的原子核内中子数是(2)推测Og在元素周期表的位置
(3)2019年科学家首次合成全碳的环形分子,下列说法正确的是_______

| A.C18和金刚石、石墨互为同素异形体 |
| B.C18是一种性质很稳定的化合物 |
| C.C20O2、C22O4、C24O6随着碳原子数的增大,氧元素的质量百分含量依次增大 |
| D.C22O4、CO、CO2都是碳元素的氧化物 |
(5)在383K时,将二氧化锰溶解于浓硫酸中,可得硫酸锰[ Mn2 ( SO4)3]并放出氧气。试写出该反应的化学方程式
(6)已知铋酸钠( NaBiO3 )是一种浅黄色的粉末,不溶于冷水,它可以在高酸度的溶液中将Mn2+氧化成
 ,自身被还原成Bi3+。试写出该反应的离子方程式
,自身被还原成Bi3+。试写出该反应的离子方程式
更新时间:2023-03-07 21:42:09
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】金属钠及其化合物在人类生产、生活中起着重要作用。
(1)Na的轨道表示式为_______ 。
(2)NaCl的熔点为800.8℃。工业上,采用电解熔融的NaCl和 混合盐,制备金属Na,电解的化学方程式为:
混合盐,制备金属Na,电解的化学方程式为: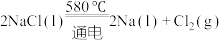 ,加入
,加入 的目的是
的目的是_______ 。
(3)采用空气和Na为原料可直接制备 。空气与熔融的金属Na反应前需依次通过的试剂为
。空气与熔融的金属Na反应前需依次通过的试剂为_______ 、_______ (填序号)。
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d. 溶液
溶液
(4) 的电子式为
的电子式为_______ 。
在25℃和101kPa时,Na与 反应生成
反应生成 放出510.9kJ的热量,写出该反应的热化学方程式:
放出510.9kJ的热量,写出该反应的热化学方程式:_______ 。
(5)向酸性 溶液中加入
溶液中加入 粉末,观察到溶液褪色,发生如下反应。
粉末,观察到溶液褪色,发生如下反应。

配平上述离子方程式_______ 。
该反应说明 具有
具有_______ (选填“氧化性”“还原性”或“漂白性”)。
(6)在密闭容器中,将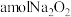 和bmol
和bmol 固体混合物加热至250℃,充分反应后,若剩余固体为
固体混合物加热至250℃,充分反应后,若剩余固体为 和NaOH、排出气体为
和NaOH、排出气体为 和
和 时,
时,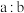 的取值范围为
的取值范围为_______ 。
(1)Na的轨道表示式为
(2)NaCl的熔点为800.8℃。工业上,采用电解熔融的NaCl和
 混合盐,制备金属Na,电解的化学方程式为:
混合盐,制备金属Na,电解的化学方程式为: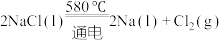 ,加入
,加入 的目的是
的目的是(3)采用空气和Na为原料可直接制备
 。空气与熔融的金属Na反应前需依次通过的试剂为
。空气与熔融的金属Na反应前需依次通过的试剂为a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.
 溶液
溶液(4)
 的电子式为
的电子式为在25℃和101kPa时,Na与
 反应生成
反应生成 放出510.9kJ的热量,写出该反应的热化学方程式:
放出510.9kJ的热量,写出该反应的热化学方程式:(5)向酸性
 溶液中加入
溶液中加入 粉末,观察到溶液褪色,发生如下反应。
粉末,观察到溶液褪色,发生如下反应。
配平上述离子方程式
该反应说明
 具有
具有(6)在密闭容器中,将
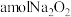 和bmol
和bmol 固体混合物加热至250℃,充分反应后,若剩余固体为
固体混合物加热至250℃,充分反应后,若剩余固体为 和NaOH、排出气体为
和NaOH、排出气体为 和
和 时,
时,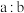 的取值范围为
的取值范围为
您最近一年使用:0次
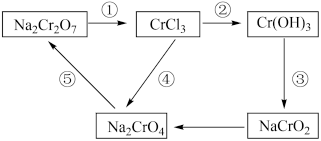
【推荐2】(1)化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该有害物质。例如:在如图有编号的步骤中,发生氧化反应的是_____________ (填编号,下同),发生还原反应的是_____________ 。(提示:铬元素化合价有+6、+3价)。
(2)饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将
的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将 还原N2,其化学方程式为:Al+NaNO3 +NaOH=NaAlO2+N2↑+H2O(未配平)
还原N2,其化学方程式为:Al+NaNO3 +NaOH=NaAlO2+N2↑+H2O(未配平)
请回答下列问题:
①氧化剂是_______________ ;氧化产物是________________ 。
②配平反应的方程式,并用单线桥表示反应中电子转移的方向和数目:
Al+ NaNO3 + NaOH= NaAlO2+ N2↑+ H2O
___
(3)一个完整的氧化还原反应方程式可以拆开写成两个“半反应式”,一个是“氧化反应”式,一个是“还原反应”式。如2Fe3++Cu=2Fe2+ +Cu2+的拆写结果是:
氧化反应:Cu-2e- =Cu2+ 还原反应: 2Fe3++2e- =2Fe2+。
请据此将反应: Fe+2H+ =Fe2+ +H2↑拆写成两个“半反应式”;
氧化反应为______________________________________________________ ;
还原反应为_____________________________________________________ 。

(2)饮用水中的
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将
的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将 还原N2,其化学方程式为:Al+NaNO3 +NaOH=NaAlO2+N2↑+H2O(未配平)
还原N2,其化学方程式为:Al+NaNO3 +NaOH=NaAlO2+N2↑+H2O(未配平)请回答下列问题:
①氧化剂是
②配平反应的方程式,并用单线桥表示反应中电子转移的方向和数目:
Al+ NaNO3 + NaOH= NaAlO2+ N2↑+ H2O
(3)一个完整的氧化还原反应方程式可以拆开写成两个“半反应式”,一个是“氧化反应”式,一个是“还原反应”式。如2Fe3++Cu=2Fe2+ +Cu2+的拆写结果是:
氧化反应:Cu-2e- =Cu2+ 还原反应: 2Fe3++2e- =2Fe2+。
请据此将反应: Fe+2H+ =Fe2+ +H2↑拆写成两个“半反应式”;
氧化反应为
还原反应为
您最近一年使用:0次
【推荐3】ClO2是一种黄绿色或橙黄色的气体,极易溶于水,可用于水的消毒杀菌、水体中Mn2+等重金属离子的除去及烟气的脱硫脱硝。回答下列问题:
(1)将过硫酸钠(Na2S2O8,结构、性质与过氧化钠相似)溶液加入亚氯酸钠(NaClO2)中可制备ClO2,NaClO2中Cl元素的化合价是___ 价,该反应中氧化剂和还原剂的数目之比为___ 。
(2)为研究ClO2脱硝(将氮氧化物转化成NO )的适宜条件,在1L含200mgClO2的溶液中加NaOH溶液调节pH,通入NO气体并测定NO的去除率,其关系如图所示:
)的适宜条件,在1L含200mgClO2的溶液中加NaOH溶液调节pH,通入NO气体并测定NO的去除率,其关系如图所示:
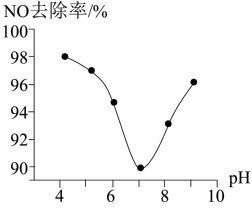
已知:NO的去除率=(1- )×100%
)×100%
①要使NO的去除率更高,应控制的条件是___ 。
②当溶液pH>7时,NO的去除率增大的原因是ClO2与NaOH溶液反应生成更强的吸收剂NaClO2,写出碱性条件下NaClO2脱除NO反应的离子方程式___ 。
(1)将过硫酸钠(Na2S2O8,结构、性质与过氧化钠相似)溶液加入亚氯酸钠(NaClO2)中可制备ClO2,NaClO2中Cl元素的化合价是
(2)为研究ClO2脱硝(将氮氧化物转化成NO
 )的适宜条件,在1L含200mgClO2的溶液中加NaOH溶液调节pH,通入NO气体并测定NO的去除率,其关系如图所示:
)的适宜条件,在1L含200mgClO2的溶液中加NaOH溶液调节pH,通入NO气体并测定NO的去除率,其关系如图所示:
已知:NO的去除率=(1-
 )×100%
)×100%①要使NO的去除率更高,应控制的条件是
②当溶液pH>7时,NO的去除率增大的原因是ClO2与NaOH溶液反应生成更强的吸收剂NaClO2,写出碱性条件下NaClO2脱除NO反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某小组同学研究氯及其化合物的制备和性质。
Ⅰ.氯水具有多种性质,该小组同学用氯水分别与紫色石蕊溶液,Na2SO3溶液反应。完成下列问题:
(1)向紫色石蕊溶液中滴加氯水的现象是______________ ,证明氯水中含有的微粒有______ 。
(2)向 Na2SO3溶液中滴加少量氯水,证明氯水有氧化性的实验方案是:取适量反应后溶液于试管中,______________ ,则证明氯水具有氧化性。
(3)氯水光照后黄绿色逐渐消失,产生无色气体,用化学方程式表示这个过程中发生的反应:______________ 、 ______________ 。
Ⅱ.某学生设计下列实验装置利用 MnO2和浓盐酸制备氯气,并用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:
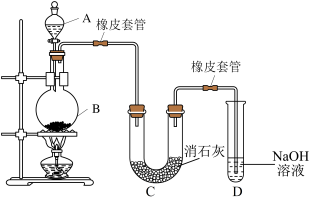
请回答下列问题:
(4)写出装置 B 中制取氯气的化学方程式:______________ 。
(5)漂白粉在 U 形管中生成,实验结果所得漂白粉 Ca(ClO)2 产率太低。经分析并查阅资料发现,主要原因是在 U 形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成 Ca(ClO3)2,写出该副反应的化学方程式__________ ,为避免发生该反应可采取的措施是______________ 。
②试判断另一个副反应是______________ (写出此反应方程式)。为避免此副反应的发生,可采取的措施是在 B、C 之间连接一个盛有______________ 的洗气瓶。
Ⅰ.氯水具有多种性质,该小组同学用氯水分别与紫色石蕊溶液,Na2SO3溶液反应。完成下列问题:
(1)向紫色石蕊溶液中滴加氯水的现象是
(2)向 Na2SO3溶液中滴加少量氯水,证明氯水有氧化性的实验方案是:取适量反应后溶液于试管中,
(3)氯水光照后黄绿色逐渐消失,产生无色气体,用化学方程式表示这个过程中发生的反应:
Ⅱ.某学生设计下列实验装置利用 MnO2和浓盐酸制备氯气,并用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:

请回答下列问题:
(4)写出装置 B 中制取氯气的化学方程式:
(5)漂白粉在 U 形管中生成,实验结果所得漂白粉 Ca(ClO)2 产率太低。经分析并查阅资料发现,主要原因是在 U 形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成 Ca(ClO3)2,写出该副反应的化学方程式
②试判断另一个副反应是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】判断正误。
1.必须用浓盐酸与MnO2反应制Cl2,因为稀盐酸与MnO2不反应。_______
2.为了减少制得的Cl2中HCl的含量,加热温度不宜过高,以减少HCl的挥发。_______
3.除去Cl2中少量HCl气体,可用饱和食盐水,也可用饱和碳酸氢钠溶液。_______
4.检验氯气可用湿润的淀粉—碘化钾试纸。_______
5.氯气在饱和食盐水中的溶解度小于在纯水中的溶解度。_______
6.实验室快速制取氯气可以采用高锰酸钾与浓盐酸的反应。_______
7.用NaOH溶液吸收多余的Cl2时,为防止倒吸,导气管不能伸入液面以下。_______
1.必须用浓盐酸与MnO2反应制Cl2,因为稀盐酸与MnO2不反应。
2.为了减少制得的Cl2中HCl的含量,加热温度不宜过高,以减少HCl的挥发。
3.除去Cl2中少量HCl气体,可用饱和食盐水,也可用饱和碳酸氢钠溶液。
4.检验氯气可用湿润的淀粉—碘化钾试纸。
5.氯气在饱和食盐水中的溶解度小于在纯水中的溶解度。
6.实验室快速制取氯气可以采用高锰酸钾与浓盐酸的反应。
7.用NaOH溶液吸收多余的Cl2时,为防止倒吸,导气管不能伸入液面以下。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氯、氮、硫的化合物与人类生活和生产有着密切的联系。请回答下列问题:
(1)瑞典化学家舍勒将软锰矿(主要成分是MnO2)与浓盐酸混合加热,在世界上首先制得了氯气。反应的化学方程式为____ 。其中,氧化剂与还原剂物质的量之比为____ 。若实验室制得标准状况下4.48L氯气,则转移电子的数目为____ 个。
(2)请写出铜与浓硝酸反应的离子方程式____ ,请写出铜与稀硝酸反应的离子方程式____ 。
(3)请配平浓硫酸在加热时与碳发生反应的化学方程式:____ 。
______C+______H2SO4(浓)=_____CO2↑+______SO2↑+______H2O。
在该反应中,浓H2SO4表现出____ (填“吸水”、“脱水”或“氧化”)性。
(1)瑞典化学家舍勒将软锰矿(主要成分是MnO2)与浓盐酸混合加热,在世界上首先制得了氯气。反应的化学方程式为
(2)请写出铜与浓硝酸反应的离子方程式
(3)请配平浓硫酸在加热时与碳发生反应的化学方程式:
______C+______H2SO4(浓)=_____CO2↑+______SO2↑+______H2O。
在该反应中,浓H2SO4表现出
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】现有A、B、C、D、E五种常见短周期元素,已知:
①元素的原子序数按A、B、C、D、E依次增大,原子半径按D、E、B、C、A顺序依次减小;
②A、D同主族,A是所有元素中原子半径最小的元素;B与C的位置相邻;C元素原子最外层电子数是次外层电子数的3倍;
③B、D、E三者的最高价氧化物有水化物依次为甲、乙、丙,它们两两之间均可反应生成可溶性盐和水,且所得盐中均含C元素;
④B、E两种元素原子最外层电子数之和等于A、C、D三种元素原子最外层电子数之和。
请填写下列空白:
(1)写出乙+丙在溶液中反应的离子方程式_________________________________ 。
(2)化合物BA3与BC在加热和有催化剂存在的条件下能发生反应,生成两种无毒物质,其反应的化学方程式为:___________________________________________ 。
(3)用电子式表示化合物D2C的形成过程_________________________________________ 。
(4)某原电池中,电解质为KOH溶液,分别向负极通入碳元素与元素C(原子物质的量之比1:1)形成的化合物,向正极通入元素C最常见的单质,试完成下列问题:
正极反应:________________________ ;负极反应:________________________ ;
①元素的原子序数按A、B、C、D、E依次增大,原子半径按D、E、B、C、A顺序依次减小;
②A、D同主族,A是所有元素中原子半径最小的元素;B与C的位置相邻;C元素原子最外层电子数是次外层电子数的3倍;
③B、D、E三者的最高价氧化物有水化物依次为甲、乙、丙,它们两两之间均可反应生成可溶性盐和水,且所得盐中均含C元素;
④B、E两种元素原子最外层电子数之和等于A、C、D三种元素原子最外层电子数之和。
请填写下列空白:
(1)写出乙+丙在溶液中反应的离子方程式
(2)化合物BA3与BC在加热和有催化剂存在的条件下能发生反应,生成两种无毒物质,其反应的化学方程式为:
(3)用电子式表示化合物D2C的形成过程
(4)某原电池中,电解质为KOH溶液,分别向负极通入碳元素与元素C(原子物质的量之比1:1)形成的化合物,向正极通入元素C最常见的单质,试完成下列问题:
正极反应:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据下列叙述,写出元素名称并画出原子结构示意图:
| 信息 | 元素名称 | 原子结构示意图 |
| A元素原子核外M层电子数是L层电子数的一半 | ||
| B元素原子最外层电子数是次外层电子数的1.5倍 | ||
| C元素+1价离子C+的电子层排布与Ne相同 | ||
D元素原子次外层电子数是最外层电子数的 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】现有部分短周期元素的性质或原子结构如下表:
(1)写出元素X的离子结构示意图____________ 。
(2)写出Y元素最高价氧化物的水化物与NaOH溶液反应的离子方程式______________
(3)写出Y的价电子排布式_________________________ 。
(4)元素T与氯元素相比,非金属性较强的是_______ (用元素符号表示),下列表述中能用于证明这一事实的是_______ (填字母代号)。
A.气态氢化物的挥发性 B.两元素的电负性
C.含氧酸的酸性 D.氢化物中X—H键的键长(X代表T和Cl两种元素)
(5)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是___ (填元素符号)
| 元素编号 | 元素性质或原子结构 |
| T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| X | L层p电子数比s电子数多2个 |
| Y | 第三周期元素的简单离子中半径最小 |
| Z | L层有三个未成对电子 |
(1)写出元素X的离子结构示意图
(2)写出Y元素最高价氧化物的水化物与NaOH溶液反应的离子方程式
(3)写出Y的价电子排布式
(4)元素T与氯元素相比,非金属性较强的是
A.气态氢化物的挥发性 B.两元素的电负性
C.含氧酸的酸性 D.氢化物中X—H键的键长(X代表T和Cl两种元素)
(5)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】请回答下列问题:
(1)写出漂白粉中有效成分的化学式_______ 。
(2)写出中子数为8的碳原子符号_______ 。
(3)写出碳酸钾的电离方程式_______ 。
(4)写出过氧化钠和水的化学方程式_______ 。
(1)写出漂白粉中有效成分的化学式
(2)写出中子数为8的碳原子符号
(3)写出碳酸钾的电离方程式
(4)写出过氧化钠和水的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】砷(As)与N、P是同主族元素,远古时期人们就开始开发利用砷的性质,现代技术中砷仍然起着非常重要的作用。请回答下列问题:
(1)砷只有一种稳定的同位素 ,其原子核内的中子数比核外电子数多
,其原子核内的中子数比核外电子数多_______ (填数值)。
(2)下列事实中,能说明As元素的非金属性弱于N元素的是_______(填标号)。
(3)Marsh试砷法和Gutzeit试砷法是法医学上鉴定砷的重要方法。其原理是先将 (剧毒)转化为
(剧毒)转化为 ,前者让:
,前者让: 分解产生黑亮的砷镜(As),后者让
分解产生黑亮的砷镜(As),后者让 被
被 溶液氧化为
溶液氧化为 ,同时还生成Ag单质。
,同时还生成Ag单质。
① 的电子式为
的电子式为_______ 。
②Gutzeit试砷法中 被氧化的离子方程式为
被氧化的离子方程式为_______ 。
(4)砷化镓(GaAs)是现代科技中制造芯片的一种原料,可用 溶液对其进行刻蚀,As元素的化合价变为+5价,则该反应中还原剂与氧化剂的物质的量之比为
溶液对其进行刻蚀,As元素的化合价变为+5价,则该反应中还原剂与氧化剂的物质的量之比为_______ ;砷化镓也可用于制造太阳能电池,该电池工作时的能量转化形式为_______ 。
(1)砷只有一种稳定的同位素
 ,其原子核内的中子数比核外电子数多
,其原子核内的中子数比核外电子数多(2)下列事实中,能说明As元素的非金属性弱于N元素的是_______(填标号)。
A.沸点: |
B.等物质的量浓度溶液的酸性: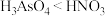 |
C.分解温度: |
D.相对分子质量: |
 (剧毒)转化为
(剧毒)转化为 ,前者让:
,前者让: 分解产生黑亮的砷镜(As),后者让
分解产生黑亮的砷镜(As),后者让 被
被 溶液氧化为
溶液氧化为 ,同时还生成Ag单质。
,同时还生成Ag单质。①
 的电子式为
的电子式为②Gutzeit试砷法中
 被氧化的离子方程式为
被氧化的离子方程式为(4)砷化镓(GaAs)是现代科技中制造芯片的一种原料,可用
 溶液对其进行刻蚀,As元素的化合价变为+5价,则该反应中还原剂与氧化剂的物质的量之比为
溶液对其进行刻蚀,As元素的化合价变为+5价,则该反应中还原剂与氧化剂的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)现有以下物质:①NaCl晶体 ②液态SO3 ③液态的醋酸 ④汞 ⑤BaSO4固体 ⑥蔗糖(C12H22O11) ⑦酒精(C2H5OH) ⑧熔化K2SO4 请回答下列问题(用序号):
①以上物质中属于电解质的是____________ ;
②以上物质中属于非电解质的是___________ ;
(2)碘元素的一种核素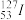 I可用于治疗肿瘤。该核素的质子数为
I可用于治疗肿瘤。该核素的质子数为_________ ,中子数为___________ ,质量数为______________ ,核外电子数为______________ 。
(3)在一定条件下,21.6gA单质与1.20molCl2完全反应,生成0.800molAClx,则X=____________ ,A的摩尔质量为_______________ 。
(4)有反应如下:Al2O3+N2+3C=2AlN+3CO
①标出该反应中电子转移的方向和数目______________ 。
②在该反应中,氧化剂是___________ ,还原剂是_________________ 。
①以上物质中属于电解质的是
②以上物质中属于非电解质的是
(2)碘元素的一种核素
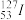 I可用于治疗肿瘤。该核素的质子数为
I可用于治疗肿瘤。该核素的质子数为(3)在一定条件下,21.6gA单质与1.20molCl2完全反应,生成0.800molAClx,则X=
(4)有反应如下:Al2O3+N2+3C=2AlN+3CO
①标出该反应中电子转移的方向和数目
②在该反应中,氧化剂是
您最近一年使用:0次



