请回答下列问题:
(1)工业冶炼镁时采用电解冶炼氯化镁而不是氧化镁的主要原因是___________ 。
(2)已知:①具有相同核外电子数和原子核数的微粒结构相似;②HN3是一元弱酸,HN3 H++N
H++N ;试写出HN3的可能结构式:
;试写出HN3的可能结构式:___________ 。
(1)工业冶炼镁时采用电解冶炼氯化镁而不是氧化镁的主要原因是
(2)已知:①具有相同核外电子数和原子核数的微粒结构相似;②HN3是一元弱酸,HN3
 H++N
H++N ;试写出HN3的可能结构式:
;试写出HN3的可能结构式:
更新时间:2021-10-31 13:07:31
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)①写出石英的化学式_______ ;
②写出氮气的电子式_______ ;
(2)写出镁在氮气中燃烧的化学方程式_______ ;
(3)写出氨的催化氧化化学方程式_______ ;
(4)写出工业上合成氨的化学方程式_______ ;
(5)写出硫代硫酸钠与稀硫酸反应的离子方程式_______ ;
②写出氮气的电子式
(2)写出镁在氮气中燃烧的化学方程式
(3)写出氨的催化氧化化学方程式
(4)写出工业上合成氨的化学方程式
(5)写出硫代硫酸钠与稀硫酸反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下列几种物质:①MgCl2②H2O③Al④H2O2⑤Na2O2⑥Ca(OH)2⑦HClO⑧I2
(1)只含有离子键的是(选填序号,下同)___________ 。
(2)含有共价键的离子化合物是___________ 。
(3)属于共价化合物的是___________ 。
(4)熔融状态时和固态时,都能导电的是___________ 。
(5)HClO的电子式___________ 。
(6)用电子式表示MgCl2的形成过程___________ 。
(1)只含有离子键的是(选填序号,下同)
(2)含有共价键的离子化合物是
(3)属于共价化合物的是
(4)熔融状态时和固态时,都能导电的是
(5)HClO的电子式
(6)用电子式表示MgCl2的形成过程
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图是元素周期表的一部分,表中列出了八种元素的位置:
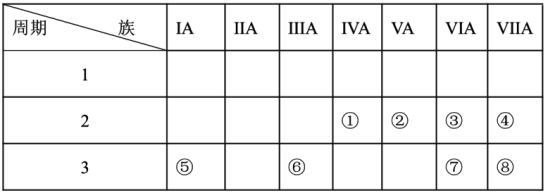
请回答下列问题:
(1)①元素的最简单氢化物的电子式为___________ 。
(2)在元素①-⑧中,金属性最强的元素是___________ (填元素符号);在元素⑤-⑧中,最高价含氧酸酸性最强的是___________ (填化学式)。
(3)③、④、⑤三种元素的原子半径由大到小的顺序是___________ (填元素符号),③和⑦的简单氢化物的稳定性较强的是___________ (填化学式)。
(4)④和⑤所形成的化合物属于___________ (填“离子”或“共价”)化合物。
(5)将等物质的量的①的最简单的氢化物和⑧的单质混合后,在漫射光的照射下充分反应,生成物中物质的量最大的是___________ (写分子式);
(6)⑤和⑥的最高价氧化物对应的水化物之间发生反应的离子方程式为___________ 。

请回答下列问题:
(1)①元素的最简单氢化物的电子式为
(2)在元素①-⑧中,金属性最强的元素是
(3)③、④、⑤三种元素的原子半径由大到小的顺序是
(4)④和⑤所形成的化合物属于
(5)将等物质的量的①的最简单的氢化物和⑧的单质混合后,在漫射光的照射下充分反应,生成物中物质的量最大的是
(6)⑤和⑥的最高价氧化物对应的水化物之间发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】钛及其化合物在人们的生活中起着十分重要的作用。尤其是二氧化钛、四氯化钛、钛酸钡等应用极广,回答下列问题:
(1)基态钛原子的价电子排布式为___________ ,该基态原子中含___________ 对电子对。
(2)二氧化钛是世界上最白的东西,1g二氧化钛可以把450多平方厘米的面积涂得雪白,是调制白油漆的最好颜料。基态Ti4+中的核外电子占据的原子轨道数为___________ 。
(3)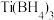 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。
反应制得。
①LiBH4由 和
和 构成,
构成, 的空间构型是
的空间构型是___________ ,B原子的杂化轨道类型是___________ ,写出一种与该阴离子互为等电子体的微粒是___________ 。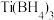 中各元素的电负性大小顺序为
中各元素的电负性大小顺序为___________ 。
②某储氢材料是第三周期金属元素M的氢化物,M的部分电离能如表所示。M是___________ (填元素符号),判断理由为___________ 。
(1)基态钛原子的价电子排布式为
(2)二氧化钛是世界上最白的东西,1g二氧化钛可以把450多平方厘米的面积涂得雪白,是调制白油漆的最好颜料。基态Ti4+中的核外电子占据的原子轨道数为
(3)
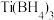 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。
反应制得。①LiBH4由
 和
和 构成,
构成, 的空间构型是
的空间构型是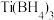 中各元素的电负性大小顺序为
中各元素的电负性大小顺序为②某储氢材料是第三周期金属元素M的氢化物,M的部分电离能如表所示。M是
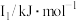 | 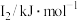 | 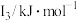 | 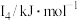 | 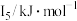 |
| 738 | 1451 | 7733 | 10540 | 13630 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氧族元素和卤族元素都能形成多种物质,我们可以利用所学物质结构的相关知识去认识和理解。
(1)H+可与H2O形成H3O+,H3O+ 立体构型为_________ 。H3O+中H﹣O﹣H键角比H2O中H﹣O﹣H键角大,原因为_________________________________________ 。
(2)COCl2的空间构型为____________ ;溴的价电子排布式为________________ 。
(3)根据已经掌握的共价键知识判断,键的极性F-H_______ O-H(“>”,“=”或“<”)
(4)溴化碘和水反应生成了一种三原子分子,该分子的结构式为____________________ ,中心原子杂化轨道类型为________________ 。
(5)根据下表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是________ 。
(6)下列分子既不存在sp σ键,也不存在pp π键的是________ 。
A.HCl B.HF C.SO2 D.SCl2
(7)ClO2-立体构型为____________ ,写出与ClO2-互为等电子体的一种分子为______ 。
(1)H+可与H2O形成H3O+,H3O+ 立体构型为
(2)COCl2的空间构型为
(3)根据已经掌握的共价键知识判断,键的极性F-H
(4)溴化碘和水反应生成了一种三原子分子,该分子的结构式为
(5)根据下表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是
| 氟 | 氯 | 溴 | 碘 | |
| 第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
(6)下列分子既不存在sp σ键,也不存在pp π键的是
A.HCl B.HF C.SO2 D.SCl2
(7)ClO2-立体构型为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】根据要求回答下列问题:
(1)在第二周期主族元素,第一电离能介于B和N之间的元素有___________ 种。
(2)嫦娥五号实现了我国首次地外天体采样返回,带回的月壤中包含了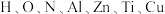 等多种元素,N的第一电离能大于O的,请说明理由:
等多种元素,N的第一电离能大于O的,请说明理由:_______ 。
(3)已知电离能: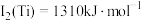 ,
,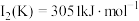 ,
,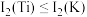 ,其原因为
,其原因为___________ 。
(4)橙红色晶体羰基钴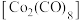 的熔点为
的熔点为 ,可溶于多数有机溶剂。该晶体中三种元素电负性由大到小的顺序为
,可溶于多数有机溶剂。该晶体中三种元素电负性由大到小的顺序为_________ (填元素符号)。配体 中
中 键与
键与 键数目之比是
键数目之比是___________ 。
(5) 中键与键之间的夹角为
中键与键之间的夹角为 ,并有对称性,分子中每个原子最外层均满足8电子稳定结构,其结构式为
,并有对称性,分子中每个原子最外层均满足8电子稳定结构,其结构式为___________ ,1个分子中含有___________ 个 键。
键。
(6)此后,等电子原理又有所发展。例如,由短周期元素组成的微粒,只要其原子数相同,各原子最外层电子数之和相同,也可互称为等电子体,它们也具有相似的结构特征。在短周期元素组成的物质中,与 互为等电子体的分子有
互为等电子体的分子有___________ 、___________ 。
(1)在第二周期主族元素,第一电离能介于B和N之间的元素有
(2)嫦娥五号实现了我国首次地外天体采样返回,带回的月壤中包含了
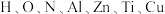 等多种元素,N的第一电离能大于O的,请说明理由:
等多种元素,N的第一电离能大于O的,请说明理由:(3)已知电离能:
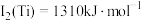 ,
,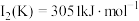 ,
,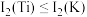 ,其原因为
,其原因为(4)橙红色晶体羰基钴
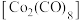 的熔点为
的熔点为 ,可溶于多数有机溶剂。该晶体中三种元素电负性由大到小的顺序为
,可溶于多数有机溶剂。该晶体中三种元素电负性由大到小的顺序为 中
中 键与
键与 键数目之比是
键数目之比是(5)
 中键与键之间的夹角为
中键与键之间的夹角为 ,并有对称性,分子中每个原子最外层均满足8电子稳定结构,其结构式为
,并有对称性,分子中每个原子最外层均满足8电子稳定结构,其结构式为 键。
键。(6)此后,等电子原理又有所发展。例如,由短周期元素组成的微粒,只要其原子数相同,各原子最外层电子数之和相同,也可互称为等电子体,它们也具有相似的结构特征。在短周期元素组成的物质中,与
 互为等电子体的分子有
互为等电子体的分子有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】有 、
、 、
、 三种晶体,分别由
三种晶体,分别由 、
、 、
、 、
、 四种元素中的一种或几种形成,对这三种晶体进行实验,结果如表所示。
四种元素中的一种或几种形成,对这三种晶体进行实验,结果如表所示。
(1)晶体的化学式分别为
______ ;
______ 。
(2)晶体的类型分别为
______ ;
______ ,
______ 。
(3) 、
、 晶体中粒子间的作用力分别为
晶体中粒子间的作用力分别为______ 、______ 。
 、
、 、
、 三种晶体,分别由
三种晶体,分别由 、
、 、
、 、
、 四种元素中的一种或几种形成,对这三种晶体进行实验,结果如表所示。
四种元素中的一种或几种形成,对这三种晶体进行实验,结果如表所示。| 晶体 | 熔点/℃ | 硬度 | 水溶性 | 导电性 | 水溶液与 反应 反应 |
 | 801 | 较大 | 易溶 | 水溶液(或熔融)导电 | 白色沉淀 |
 | 3500 | 很大 | 不溶 | 不导电 | 不反应 |
 | 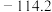 | 很小 | 易溶 | 液态不导电 | 白色沉淀 |
(1)晶体的化学式分别为


(2)晶体的类型分别为



(3)
 、
、 晶体中粒子间的作用力分别为
晶体中粒子间的作用力分别为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】二氧化碳、二氧化硅和氧化镁的晶体结构或晶胞如下图。
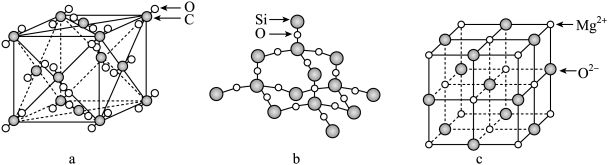
回答下列问题:
(1)每个晶胞a中平均含有_______ 个CO2分子。
(2)晶体b中粒子间作用力是_______ ,其中Si原子与Si-O键的数目比是_______ 。
(3)晶胞c中,O2-的配位数为_______ 。
(4)二氧化碳与二氧化硅比较,熔点较高的是_______ (填化学式)。

回答下列问题:
(1)每个晶胞a中平均含有
(2)晶体b中粒子间作用力是
(3)晶胞c中,O2-的配位数为
(4)二氧化碳与二氧化硅比较,熔点较高的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】下列关于碳和碳的化合物的结构和性质中
(1)和碳同一主族的硅原子中能量最高的电子处在______ 电子层上(填写电子层符号),最外层有___ 种运动状态不同的电子,碳原子核外有______ 种能量不同的电子,有______ 种不同形状的电子云.
(2)1个C原子的单键氢化物分子是CH4,2个C原子的单键氢化物分子则为C2H6.以下各对分子间不存在类似关系的是_________
A.NH3与N2H4 B.H2O与H2O2 C.SF6与S2F10 D.SCl4与S2Cl2
(3)金刚石的熔点低于石墨,原因可能是________
A.石墨中还有范德华力
B.石墨熔化也要破坏共价键,且键长更短
C.石墨热稳定性更好
(4)已知常温下,H2CO3:Ki1=4.3x10﹣7、Ki2=5.6x10﹣11.结合H+的能力Na2CO3溶液______ (填”>”、”<”或“=”)NaHCO3溶液,设计简单实验证明:______ .
(5)在1L 0.3mol/L的NaOH溶液中,通入4.48LCO2(标准状况),反应后所得溶液中离子的浓度之间有一些等量关系,例如:.c(Na+)+c(H+)=c(HCO3﹣)+2c(CO32﹣)+c(OH﹣),另外对此溶液中存在的离子按浓度由大到小排序为______ .
(1)和碳同一主族的硅原子中能量最高的电子处在
(2)1个C原子的单键氢化物分子是CH4,2个C原子的单键氢化物分子则为C2H6.以下各对分子间不存在类似关系的是
A.NH3与N2H4 B.H2O与H2O2 C.SF6与S2F10 D.SCl4与S2Cl2
(3)金刚石的熔点低于石墨,原因可能是
A.石墨中还有范德华力
B.石墨熔化也要破坏共价键,且键长更短
C.石墨热稳定性更好
(4)已知常温下,H2CO3:Ki1=4.3x10﹣7、Ki2=5.6x10﹣11.结合H+的能力Na2CO3溶液
(5)在1L 0.3mol/L的NaOH溶液中,通入4.48LCO2(标准状况),反应后所得溶液中离子的浓度之间有一些等量关系,例如:.c(Na+)+c(H+)=c(HCO3﹣)+2c(CO32﹣)+c(OH﹣),另外对此溶液中存在的离子按浓度由大到小排序为
您最近一年使用:0次



