为了达到下列的实验要求,请从供选择的化学试剂或实验方法中选出合适的,将其编号填入对应的空格中,并按要求写出相应的方程式。
供选择的化学试剂或实验方法如下:
A.加入NaOH溶液,过滤、洗涤、干燥 B.通入适量的CO2
C.通入Cl2气体 D.加入适量铁粉
E.加入CaCl2溶液,观察 F.加入澄清石灰水,观察
G.丁达尔效应
(1)鉴别Fe(OH)3胶体和FeCl3溶液:________
(2)除去镁粉中的少量铝粉杂质:_______
(3)除去FeCl3溶液中FeCl2:_____ , 离子方程式____________________
(4)实验室保存FeSO4溶液时要加入____ ;
(5)除去NaHCO3溶液中的少量Na2CO3杂质:________ , 化学方程式:___________________
供选择的化学试剂或实验方法如下:
A.加入NaOH溶液,过滤、洗涤、干燥 B.通入适量的CO2
C.通入Cl2气体 D.加入适量铁粉
E.加入CaCl2溶液,观察 F.加入澄清石灰水,观察
G.丁达尔效应
(1)鉴别Fe(OH)3胶体和FeCl3溶液:
(2)除去镁粉中的少量铝粉杂质:
(3)除去FeCl3溶液中FeCl2:
(4)实验室保存FeSO4溶液时要加入
(5)除去NaHCO3溶液中的少量Na2CO3杂质:
更新时间:2020-10-07 07:01:44
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】请回答下列问题:
(1)云、雾属于胶体,鉴别胶体和溶液的方法是___________ ,胶体和溶液的本质区别是___________ 。
(2)钠的焰色试验的焰色为___________ 色;钠着火了不能用水而需要用干燥的沙土来灭火,请用离子方程式来表示其原因___________ 。
(3)过氧化钠是一种___________ 色的固体,可作漂白剂和呼吸面具中的供氧剂,写出过氧化钠和二氧化碳反应的化学方程式,并用双线桥法表示电子转移的方向和数目:___________ 。
(4)小苏打可用于治疗胃酸过多,其原理用离子反应方程式表示为___________
(5)漂白粉是将氯气通入冷的石灰乳中制得的,写出该制备原理的化学方程式___________ 。
(1)云、雾属于胶体,鉴别胶体和溶液的方法是
(2)钠的焰色试验的焰色为
(3)过氧化钠是一种
(4)小苏打可用于治疗胃酸过多,其原理用离子反应方程式表示为
(5)漂白粉是将氯气通入冷的石灰乳中制得的,写出该制备原理的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】对于数以千万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。现有以下物质:①熔融NaCl ②Cu ③醋酸溶液 ④Fe(OH)3胶体 ⑤蔗糖 ⑥CO2 ⑦稀硫酸 ⑧NaHSO4固体
(1)能导电的是__________________ (填序号,下同);属于电解质的是_____________ ,属于非电解质的是_______________ 。
(2)写出实验室制备④的离子方程式______________ ;向④中逐滴滴加⑦,可观察到的现象是_________________ ,写出相关离子方程式:_______________________ 。
(3)物质⑧在水溶液中的电离方程式为___________________________ 。
(1)能导电的是
(2)写出实验室制备④的离子方程式
(3)物质⑧在水溶液中的电离方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)现有下列状态的物质:
①干冰 ② 晶体 ③
晶体 ③ ④纯醋酸 ⑤
④纯醋酸 ⑤ 溶液 ⑥铜 ⑦熔融的KOH ⑧蔗糖 ⑨稀硫酸 ⑩
溶液 ⑥铜 ⑦熔融的KOH ⑧蔗糖 ⑨稀硫酸 ⑩ 晶体
晶体
能导电的是___________ (填写序号,下同)其中属于电解质的是___________ ,属于强电解质的是___________ 。
(2)胶体是一种常见的分散系,回答下列问题:
①向煮沸的蒸馏水中逐滴加入饱和 溶液,继续煮沸至
溶液,继续煮沸至___________ ,停止加热,可制得 胶体,制取
胶体,制取 胶体化学反应方程式为
胶体化学反应方程式为___________ 。
②区分胶体和溶液常用的方法叫做___________ 。
(1)现有下列状态的物质:
①干冰 ②
 晶体 ③
晶体 ③ ④纯醋酸 ⑤
④纯醋酸 ⑤ 溶液 ⑥铜 ⑦熔融的KOH ⑧蔗糖 ⑨稀硫酸 ⑩
溶液 ⑥铜 ⑦熔融的KOH ⑧蔗糖 ⑨稀硫酸 ⑩ 晶体
晶体能导电的是
(2)胶体是一种常见的分散系,回答下列问题:
①向煮沸的蒸馏水中逐滴加入饱和
 溶液,继续煮沸至
溶液,继续煮沸至 胶体,制取
胶体,制取 胶体化学反应方程式为
胶体化学反应方程式为②区分胶体和溶液常用的方法叫做
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】金属钠是在1807年通过电解氢氧化钠制得的,这个原理应用于工业生产,约在1891年才获得成功。1921年实现了电解氯化钠制钠的工业方法,其反应原理是2NaCl(熔融) 2Na+Cl2↑。回答下列有关单质钠的问题:
2Na+Cl2↑。回答下列有关单质钠的问题:
(1)保存金属钠的正确方法是___________。
(2)将一小块钠放在水平放置的试管中部,用酒精灯加热充分反应(如图所示),请写出该反应的化学方程式:___________ ,生成物的颜色为___________ 。

(3)Na、NaOH久置于空气中最终都变为___________ (填化学式)。
(4)除去碳酸钠粉末中混有的少量碳酸氢钠固体的最适宜的方法为___________ ,所涉及到的化学方程式为___________ 。
(5)工业上以NaCl、NH3、CO2等为原料先制得NaHCO3,反应的化学方程式为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl,进而生产纯碱。
某活动小组根据上述原理,制备碳酸氢钠。实验装置如图所示(夹持、固定用仪器未画出)。

乙装置中的试剂是___________ ;实验中分离出NaHCO3晶体的操作是___________ (填分离操作名称)。
 2Na+Cl2↑。回答下列有关单质钠的问题:
2Na+Cl2↑。回答下列有关单质钠的问题:(1)保存金属钠的正确方法是___________。
| A.放在棕色瓶中 | B.放在细沙中 | C.放在水中 | D.放在煤油中 |

(3)Na、NaOH久置于空气中最终都变为
(4)除去碳酸钠粉末中混有的少量碳酸氢钠固体的最适宜的方法为
(5)工业上以NaCl、NH3、CO2等为原料先制得NaHCO3,反应的化学方程式为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl,进而生产纯碱。
某活动小组根据上述原理,制备碳酸氢钠。实验装置如图所示(夹持、固定用仪器未画出)。

乙装置中的试剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请按照要求填写:
(1)除去Fe2O3粉末中的A12O3,所选试剂为_______ ,相关的化学方程式为_______ 。
(2)除去FeCl2溶液中的CuCl2,所选试剂为_______ ,相关的离子方程式为_______ 。
(3)除去Na2CO3固体中的NaHCO3除杂方法为_______ 。相关的化学反应方程式为_______ 。
(4)FeCl3溶液腐蚀铜板的离子方程式为_______ 。
(5)为防止FeSO4溶液变质,一般在溶液中加入少量铁粉,其原因是_______ 。
(1)除去Fe2O3粉末中的A12O3,所选试剂为
(2)除去FeCl2溶液中的CuCl2,所选试剂为
(3)除去Na2CO3固体中的NaHCO3除杂方法为
(4)FeCl3溶液腐蚀铜板的离子方程式为
(5)为防止FeSO4溶液变质,一般在溶液中加入少量铁粉,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】我国科学家侯德榜发明了联合制碱法。以氯化钠、氨及二氧化碳为原料,同时生产纯碱和氯化铵两种产品,又称“侯氏制碱法”,对世界制碱工业作出了卓越贡献。根据要求回答下列问题:
I、用纯净的碳酸钠固体配制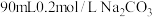 溶液。
溶液。
(1)用托盘天平称取 固体的质量是
固体的质量是_____ 
(2)本实验中需要用到的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和_____ 。
(3)下列说法中,正确的是_____(填字母)。
II、生成纯碱的流程如下: 、
、 、
、 ,依次加入的试剂是_____、_____、_____、过滤、_____。备用的除杂试剂有:①足量
,依次加入的试剂是_____、_____、_____、过滤、_____。备用的除杂试剂有:①足量 溶液;②足量
溶液;②足量 溶液;③适量稀盐酸;④足量的
溶液;③适量稀盐酸;④足量的 溶液。则正确的试剂添加顺序_____(填字母)。
溶液。则正确的试剂添加顺序_____(填字母)。
(5)已知:
写出装置I中反应的化学方程式:_____ 。
(6)制出的纯碱中只含有杂质 ,下列实验方案中,不能测定出混合物中
,下列实验方案中,不能测定出混合物中 质量分数的是_____(填字母)。
质量分数的是_____(填字母)。
(7)将碳酸钠和碳酸氢钠的混合物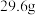 ,加热到质量不再变化时,剩余物质的质量
,加热到质量不再变化时,剩余物质的质量 ,则混合物中碳酸钠的质量分数
,则混合物中碳酸钠的质量分数_____  (精确到0.1)。
(精确到0.1)。
I、用纯净的碳酸钠固体配制
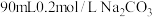 溶液。
溶液。(1)用托盘天平称取
 固体的质量是
固体的质量是
(2)本实验中需要用到的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和
(3)下列说法中,正确的是_____(填字母)。
| A.定容时仰视刻度线,会导致配制的溶液浓度偏小 |
| B.定容时如果加水超过刻度线,要用滴管吸出 |
| C.摇匀后发现凹液面下降,再加水至刻度线 |
| D.转移时溶液倒出容量瓶外,要重新配制溶液 |
II、生成纯碱的流程如下:

 、
、 、
、 ,依次加入的试剂是_____、_____、_____、过滤、_____。备用的除杂试剂有:①足量
,依次加入的试剂是_____、_____、_____、过滤、_____。备用的除杂试剂有:①足量 溶液;②足量
溶液;②足量 溶液;③适量稀盐酸;④足量的
溶液;③适量稀盐酸;④足量的 溶液。则正确的试剂添加顺序_____(填字母)。
溶液。则正确的试剂添加顺序_____(填字母)。| A.①②③④ | B.②①④③ | C.②④①③ | D.④②①③ |
(5)已知:
 |  |  |  | |
| 溶解度(20℃) | 36.0 | 21.7 | 9.6 | 37.2 |
(6)制出的纯碱中只含有杂质
 ,下列实验方案中,不能测定出混合物中
,下列实验方案中,不能测定出混合物中 质量分数的是_____(填字母)。
质量分数的是_____(填字母)。A.取 混合物充分加热,质量减少 混合物充分加热,质量减少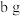 |
B.取 混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到 混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到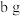 固体 固体 |
C.取 混合物与足量 混合物与足量 溶液充分反应,沉淀经过滤、洗涤、干燥得到 溶液充分反应,沉淀经过滤、洗涤、干燥得到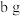 固体 固体 |
D.取 混合物与足量稀盐酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加 混合物与足量稀盐酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加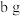 |
(7)将碳酸钠和碳酸氢钠的混合物
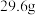 ,加热到质量不再变化时,剩余物质的质量
,加热到质量不再变化时,剩余物质的质量 ,则混合物中碳酸钠的质量分数
,则混合物中碳酸钠的质量分数 (精确到0.1)。
(精确到0.1)。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据铁元素化合物的知识:
(1)在配制含有Fe2+溶液时,常常需要向溶液中加入少量铁粉,其原因是____ ;反应的离子方程式为____ 。
(2)为除去废水中的Fe2+,常加____ 将废水中的Fe2+氧化,再调节pH使Fe3+转化为_____ 除去。
(1)在配制含有Fe2+溶液时,常常需要向溶液中加入少量铁粉,其原因是
(2)为除去废水中的Fe2+,常加
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)写出N2的结构式:_______ 。
(2)FeSO4溶液保存时,为防止其氧化变质,应在溶液中加入少量_______ 。
(3)写出铁粉与水蒸气高温下反应的化学方程式_______ 。
(4)写出金属铝与氢氧化钠溶液反应的离子方程式_______ 。
(5)除去Na2CO3粉末中少量NaHCO3的方法_______ 。
(1)写出N2的结构式:
(2)FeSO4溶液保存时,为防止其氧化变质,应在溶液中加入少量
(3)写出铁粉与水蒸气高温下反应的化学方程式
(4)写出金属铝与氢氧化钠溶液反应的离子方程式
(5)除去Na2CO3粉末中少量NaHCO3的方法
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)在我国使用最早的合金是________ ,目前用量最大,用途最广泛的合金是________ .
(2)0.5mol H2O 的质量为________ g,共有________ 个原子.
(3)质量都是50g 的Cl2、NH3、CO2、O2 四种气体中,含有分子数最少的是________ ;在相同的温度和压强下,体积最大的是________ .
(4)配制100mL 0.2mol/L CuSO4溶液,需要CuSO4•5H2O________ g.
(5)在配制硫酸亚铁溶液时,常常加入铁粉,请说明原因________ (用离子方程式表示)
(6)过氧化钠跟水反应的化学方程式是________ .
(2)0.5mol H2O 的质量为
(3)质量都是50g 的Cl2、NH3、CO2、O2 四种气体中,含有分子数最少的是
(4)配制100mL 0.2mol/L CuSO4溶液,需要CuSO4•5H2O
(5)在配制硫酸亚铁溶液时,常常加入铁粉,请说明原因
(6)过氧化钠跟水反应的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】欲除去下列物质中的少量杂质,请填写所用方法及反应的化学方程式:
(1) 固体中的
固体中的 :方法是
:方法是_______ ,化学方程式为_______ 。
(2)NaCl溶液中的 :方法是
:方法是_______ ,化学方程式为_______ 。
(3)NaOH溶液中的 :方法是
:方法是_______ ,化学方程式为_______ 。
(4) 气体中的HCl:方法是
气体中的HCl:方法是_______ ,化学方程式为_______ 。
(5) 溶液中的
溶液中的 :方法是
:方法是_______ ,化学方程式为_______ 。
(1)
 固体中的
固体中的 :方法是
:方法是(2)NaCl溶液中的
 :方法是
:方法是(3)NaOH溶液中的
 :方法是
:方法是(4)
 气体中的HCl:方法是
气体中的HCl:方法是(5)
 溶液中的
溶液中的 :方法是
:方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请按要求填空:
(1)除去乙醇中溶解的食盐,方法是________ 。
(2)除去KNO3晶体中少量的NaCl,所进行的实验操作依次是________ 、蒸发、结晶、_____ 。
(3)除去CO2中少量的HCl通入________ 溶液洗气。
(4)除去Ca(OH)2溶液中悬浮的CaCO3颗粒用________ 操作。
(5)除去KCl溶液中的SO42-离子,依次加入的溶液为(填化学式):_____ 、_____ 、_______ 。
(1)除去乙醇中溶解的食盐,方法是
(2)除去KNO3晶体中少量的NaCl,所进行的实验操作依次是
(3)除去CO2中少量的HCl通入
(4)除去Ca(OH)2溶液中悬浮的CaCO3颗粒用
(5)除去KCl溶液中的SO42-离子,依次加入的溶液为(填化学式):
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】除杂:
①NaCl溶液中有少量的NaHCO3
方法____________________ 方程式为 ____________________
②小苏打溶液中有少量的苏打
方法____________________ 方程式为 ____________________
③碳酸钠溶液中有少量的碳酸氢钠
方法____________________ 方程式为 ____________________
④碳酸氢钠固体中有少量碳酸钠固体
方法____________________ 方程式为____________________
①NaCl溶液中有少量的NaHCO3
方法
②小苏打溶液中有少量的苏打
方法
③碳酸钠溶液中有少量的碳酸氢钠
方法
④碳酸氢钠固体中有少量碳酸钠固体
方法
您最近一年使用:0次



