(1)醋酸可通过分子间氢键双聚形成八元环,画出该结构_______________ 。(以O…H—O表示氢键)
(2)已知碳化镁Mg2C3可与水反应生成丙炔,画出Mg2C3的电子式__________________ 。
(3)工业上,异丙苯主要通过苯与丙烯在无水三氯化铝催化下反应获得,写出该反应方程式_______________ 。
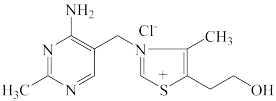
(4)维生素B1的结构简式如图所示,维生素B1晶体溶于水的过程,需要克服的微粒间作用力,除范德华力外还有________ 。
(2)已知碳化镁Mg2C3可与水反应生成丙炔,画出Mg2C3的电子式
(3)工业上,异丙苯主要通过苯与丙烯在无水三氯化铝催化下反应获得,写出该反应方程式
(4)维生素B1的结构简式如图所示,维生素B1晶体溶于水的过程,需要克服的微粒间作用力,除范德华力外还有

更新时间:2020-10-12 23:08:32
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】黄河是中华民族的母亲河,主要含有的离子有HCO 、SO
、SO 、Cl-、Ca2+、Mg2+、Na+。
、Cl-、Ca2+、Mg2+、Na+。
完成下列填空:
(1)上述离子所涉及元素:某元素原子的K层与M层电子数之和等于L层上电子数,其简单离子的电子式为_______________ ,与该离子具有相同电子数的四核微粒有______ (写出2种)。
(2)为了确定黄河水中的负离子,某研究小组进行了如下实验,请你参与探究与分析。
(3)某制碱工厂的废液中含有大量OH-,会对黄河原有的哪些离子产生影响:__________ 。
(4)工厂常利用石灰乳做高浓度含氟离子废水的处理剂。已知:氟化钙难溶于水,请写出石灰乳用于处理含氟离子废水的离子方程式。_________________________________
(5)某金属矿场的废液中含Au3+,可以在强碱性条件下,用NaBH4(已知H为-1价)处理,生成单质Au。已知:反应后硼元素以BO 形式存在,反应前后硼元素化合价不变,且无气体生成。补全下列方程式并配平。
形式存在,反应前后硼元素化合价不变,且无气体生成。补全下列方程式并配平。_____ 。
___Au3++___BH +__ ______=______+__ ______+__H2O
+__ ______=______+__ ______+__H2O
 、SO
、SO 、Cl-、Ca2+、Mg2+、Na+。
、Cl-、Ca2+、Mg2+、Na+。完成下列填空:
(1)上述离子所涉及元素:某元素原子的K层与M层电子数之和等于L层上电子数,其简单离子的电子式为
(2)为了确定黄河水中的负离子,某研究小组进行了如下实验,请你参与探究与分析。
| 实验步骤 | 实验操作 | 实验目的 | 反应的离子方程式 |
| 第一步 | 取样,滴加过量的HNO3溶液 | 检验 | |
| 第二步 | 再滴加过量的 | 检验 的存在 的存在 | Ba2++SO =BaSO4↓ =BaSO4↓ |
| 第三步 | 过滤,取滤液少许,滴加 | 检验 | Ag++Cl-=AgCl↓ |
黄河流域沿途工业污水的任意排放是造成黄河水质恶化的最大隐患。
(3)某制碱工厂的废液中含有大量OH-,会对黄河原有的哪些离子产生影响:
(4)工厂常利用石灰乳做高浓度含氟离子废水的处理剂。已知:氟化钙难溶于水,请写出石灰乳用于处理含氟离子废水的离子方程式。
(5)某金属矿场的废液中含Au3+,可以在强碱性条件下,用NaBH4(已知H为-1价)处理,生成单质Au。已知:反应后硼元素以BO
 形式存在,反应前后硼元素化合价不变,且无气体生成。补全下列方程式并配平。
形式存在,反应前后硼元素化合价不变,且无气体生成。补全下列方程式并配平。___Au3++___BH
 +__ ______=______+__ ______+__H2O
+__ ______=______+__ ______+__H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求完成下列问题。
(1) 精确包含
精确包含 个基本单元,计算时约为
个基本单元,计算时约为 个,
个,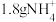 所含的电子数约为
所含的电子数约为_____ 个。在标准状况下,11克 的体积是
的体积是___  。
。
(2)同温同压下,等质量的 、
、 、
、 、
、 四种气体中,体积最大的是
四种气体中,体积最大的是______ ;同温同压下, 和
和 以体积比
以体积比 混合,求混合气体对
混合,求混合气体对 的相对密度是
的相对密度是_______ 。
(3)下列八种物质:① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ,其中含有共价键的离子化合物的是
,其中含有共价键的离子化合物的是______ ,属于共价化合物的是______ ,写出 的电子式
的电子式_____ 。
(1)
 精确包含
精确包含 个基本单元,计算时约为
个基本单元,计算时约为 个,
个,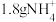 所含的电子数约为
所含的电子数约为 的体积是
的体积是 。
。(2)同温同压下,等质量的
 、
、 、
、 、
、 四种气体中,体积最大的是
四种气体中,体积最大的是 和
和 以体积比
以体积比 混合,求混合气体对
混合,求混合气体对 的相对密度是
的相对密度是(3)下列八种物质:①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ,其中含有共价键的离子化合物的是
,其中含有共价键的离子化合物的是 的电子式
的电子式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】短周期元素在周期表中的位置如图所示。请按要求回答下列问题。
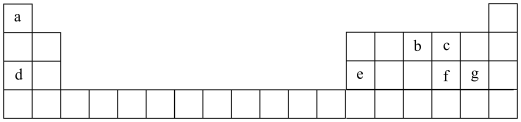
(1)由a、c、d形成的化合物的电子式为___________ ,该物质属于___________ 化合物(填“离子”或“共价”)。可能含有的化学键类型有___________ 。
(2)a与b形成的二元化合物中,所含电子数为10的分子的电子式为___________ ,a与c形成的二元化合物中,所含电子数为18的物质的结构式为___________ 。
(3)在全国抗击“新冠肺炎”的“战疫”中用了大量的“84”来消毒杀菌,84消毒液和洁厕灵混合使用时产生了一种有毒气体,写出两者混合时的化学反应方程式:___________ 。
(4)写出d与e两种元素的最高价氧化物对应的水化物相互反应的离子方程式:___________ 。

(1)由a、c、d形成的化合物的电子式为
(2)a与b形成的二元化合物中,所含电子数为10的分子的电子式为
(3)在全国抗击“新冠肺炎”的“战疫”中用了大量的“84”来消毒杀菌,84消毒液和洁厕灵混合使用时产生了一种有毒气体,写出两者混合时的化学反应方程式:
(4)写出d与e两种元素的最高价氧化物对应的水化物相互反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】3种有机物 ① 、②CH3CH2OH、③ CH3COOH,能用于医用消毒的是
、②CH3CH2OH、③ CH3COOH,能用于医用消毒的是________ (填序号,下同),能使紫色石蕊变红是__________ ,能发生取代和加成反应的是__________ 。
 、②CH3CH2OH、③ CH3COOH,能用于医用消毒的是
、②CH3CH2OH、③ CH3COOH,能用于医用消毒的是
您最近一年使用:0次
【推荐2】苯的化学性质
苯的结构稳定,苯不与酸性KMnO4溶液、溴水反应。但苯可以萃取溴水中的溴。
(1)氧化反应:苯有可燃性,空气里燃烧产生_______ ,化学方程式为_______ 。
(2)取代反应(写出有关化学反应方程式,后同)
①溴代反应:_______ 。
②硝化反应:_______ 。
③磺化反应:_______ 。
(3)加成反应(与H2加成):_______ 。
苯的结构稳定,苯不与酸性KMnO4溶液、溴水反应。但苯可以萃取溴水中的溴。
(1)氧化反应:苯有可燃性,空气里燃烧产生
(2)取代反应(写出有关化学反应方程式,后同)
①溴代反应:
②硝化反应:
③磺化反应:
(3)加成反应(与H2加成):
您最近一年使用:0次
填空题
|
适中
(0.65)
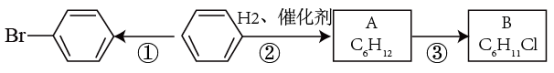
【推荐1】观察下图中物质分子的比例模型及其变化,回答下列问题。

(1)A是乙醇,则B的名称是______ ,C的结构简式是______ 。
(2)上图所示化学方程式中的“反应条件”是______ 。
(3)反应物中只有乙醇分子中的氧原子是18O,生成物中含这种氧原子的物质是(写物质名称)______ 。
(4)在B的分子中,最外层电子数为8的原子共有______ 个。

(1)A是乙醇,则B的名称是
(2)上图所示化学方程式中的“反应条件”是
(3)反应物中只有乙醇分子中的氧原子是18O,生成物中含这种氧原子的物质是(写物质名称)
(4)在B的分子中,最外层电子数为8的原子共有
您最近一年使用:0次
【推荐2】有下列3种有机化合物A:乙烯、B:乙醇、C:乙酸。
(1)写出化合物A、B、C中官能团的名称____ 、____ 、___ 。
(2)3种化合物中能使溴的四氯化碳溶液褪色的是___ (写结构简式);丙烯与乙烯具有相似的化学性质。丙烯通入溴水中的反应方程式为___ ;反应类型为___ 。
(3)B在铜和氧气中加热的方程式:___ ;反应类型为___ 。
(1)写出化合物A、B、C中官能团的名称
(2)3种化合物中能使溴的四氯化碳溶液褪色的是
(3)B在铜和氧气中加热的方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ、体育比赛中当运动员肌肉挫伤或扭伤时,队医常用药剂氯乙烷(CH3CH2Cl)(沸点为12.27 ℃)对受伤部位进行局部冷却麻醉处理,工业上制取氯乙烷有两种方案:
a.CH3CH3+Cl2 CH3CH2Cl+HCl b.CH2=CH2+HCl
CH3CH2Cl+HCl b.CH2=CH2+HCl CH3—CH2Cl
CH3—CH2Cl
(1)你认为制备氯乙烷的最好方案为___________ (填“a”或“b”)。
Ⅱ、乙醇和乙酸是生活中常见的有机物。
(2)如图所示为乙醇的___________ (“空间充填”或“球棍”)模型。
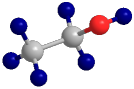
(3)乙醇中所含有的官能团的名称为___________ ,乙酸属于___________ (填“电解质”或“非电解质”)。
(4)用结构简式补全如图所示装置中乙醇和乙酸反应的化学方程式:CH3CH2OH+CH3COOH
___________ +H2O,该反应的类型为___________ 反应(填“取代”或“加成”),右侧小试管中应装有___________ 溶液(填“饱和Na2CO3”或“饱和NaOH”)。

a.CH3CH3+Cl2
 CH3CH2Cl+HCl b.CH2=CH2+HCl
CH3CH2Cl+HCl b.CH2=CH2+HCl CH3—CH2Cl
CH3—CH2Cl(1)你认为制备氯乙烷的最好方案为
Ⅱ、乙醇和乙酸是生活中常见的有机物。
(2)如图所示为乙醇的

(3)乙醇中所含有的官能团的名称为
(4)用结构简式补全如图所示装置中乙醇和乙酸反应的化学方程式:CH3CH2OH+CH3COOH


您最近一年使用:0次
【推荐1】有如下几种物质:
A.金刚石 B.MgF2 C.NH4Cl D.NaNO3 E.干冰 F.固体碘
选取适当物质填写下列空白。
(1)熔化时不需破坏化学键的是_______ ,熔化时只需破坏共价键的是_____ ,熔点最高的是________ ,熔点最低的是________ 。
(2)晶体中既存在离子键又存在共价键的是_______ ,只存在离子键的是_____ 。
(3)由极性键构成的非极性分子有________ 。
(4)可溶于CCl4的有________ 。
A.金刚石 B.MgF2 C.NH4Cl D.NaNO3 E.干冰 F.固体碘
选取适当物质填写下列空白。
(1)熔化时不需破坏化学键的是
(2)晶体中既存在离子键又存在共价键的是
(3)由极性键构成的非极性分子有
(4)可溶于CCl4的有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铜及其合金是人类最早使用的金属材料,铜的化合物在现代生活和生产中有着广泛的应用。
(1)铜的熔点比钙的高,其原因是____________________ 。
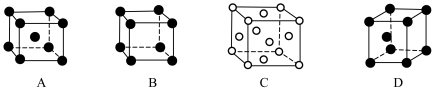
(2)金属铜的堆积方式为如图中的_____________ (填字母序号)。
(3)某磷青铜晶胞结构如图所示。
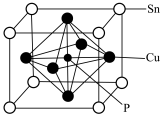
①则其化学式为_____________ 。
②该晶体中距离Cu原子最近的Sn原子有_____ 个,这些Sn原子所呈现的构型为____
(4)磷化铜与水作用产生有毒的磷化氢(PH3)。P与N同主族,其最高价氧化物对应水化物的酸性:HNO3________ H3PO4(填“>”或“<”),从结构的角度说明理由:_________________ 。
(1)铜的熔点比钙的高,其原因是
(2)金属铜的堆积方式为如图中的

(3)某磷青铜晶胞结构如图所示。

①则其化学式为
②该晶体中距离Cu原子最近的Sn原子有
(4)磷化铜与水作用产生有毒的磷化氢(PH3)。P与N同主族,其最高价氧化物对应水化物的酸性:HNO3
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Cl2与NaOH溶液反应可生成NaCl、NaClO和NaClO3(Cl-和ClO-的比值与反应的温度有关),用24.0g NaOH配成的250mL溶液,与Cl2恰好完全反应(忽略Cl2与水的反应、盐类的水解及溶液体积变化):
(1)请选出下列物质所含有的化学键类型:
Cl2:___________ ;NaOH:___________ 。
A.离子键 B.共价键 C.氢键 D.分子间作用力
(2)配制NaOH溶液时,除了下列仪器外,还需要用到的玻璃仪器是___________ 。
A.烧杯 B.玻璃棒 C.胶头滴管 D.托盘天平
(3)配得的NaOH溶液物质的量浓度为___________ 。
(4)某温度下,反应后溶液中c(Cl-)=6c(ClO-),则溶液中c(ClO-) =___________ mol/L
(1)请选出下列物质所含有的化学键类型:
Cl2:
A.离子键 B.共价键 C.氢键 D.分子间作用力
(2)配制NaOH溶液时,除了下列仪器外,还需要用到的玻璃仪器是
A.烧杯 B.玻璃棒 C.胶头滴管 D.托盘天平
(3)配得的NaOH溶液物质的量浓度为
(4)某温度下,反应后溶液中c(Cl-)=6c(ClO-),则溶液中c(ClO-) =
您最近一年使用:0次