如图为氢氧燃料电池示意图,按此图的提示,回答下列问题:
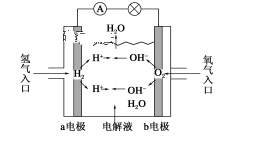
(1)a电极是__________ ,b电极是___________ 。
(2)不管燃料电池的电解液是酸性的还是碱性的,放电后电解质溶液的pH___________ (填“增大”“减小”或“不变”)
(3)当电解质溶液为碱性时,b电极发生的电极反应为:__________________________________________ pH_____________________
(4)氢氧燃料电池是一种______ (填“需要”或“不需要”)将还原剂和氧化剂全部储藏在电池内的新型发电装置

(1)a电极是
(2)不管燃料电池的电解液是酸性的还是碱性的,放电后电解质溶液的pH
(3)当电解质溶液为碱性时,b电极发生的电极反应为:
(4)氢氧燃料电池是一种
18-19高一下·甘肃庆阳·期中 查看更多[1]
(已下线)甘肃省宁县二中2018-2019高一下学期期中考试化学试卷
更新时间:2019-05-31 09:30:34
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题。
I.现有以下物质:①NaOH溶液;②蔗糖;③Ba(OH)2固体;④熔融KHSO4;⑤Fe(OH)3胶体;⑥NaHCO3;⑦CO2;⑧CH3COOH;⑨石墨。
(1)以上物质中属于电解质的是________ (填序号,下同);属于非电解质的是_______ 。
(2)以上物质属于纯净物且能导电的是________ 。
II.在如图所示的串联装置中,发现灯泡不亮,但若向其中一个烧杯中加水,则灯泡会亮起来:

(3)加水的烧杯为________ 。
(4)向烧杯A滴入Ba(OH)2溶液,溶液导电性________ 。
(5)H3PO4是三元酸,能生成NaH2PO4、Na2HPO4两种酸式盐和Na3PO4一种正盐。磷还有一种含氧酸叫亚磷酸(H3PO3)。已知:H3PO3与NaOH反应只生成NaH2PO3和Na2HPO3两种盐。那么Na2HPO3为________ (填“正盐”或“酸式盐”);写出H3PO3与少量NaOH溶液反应的离子方程式________ 。
I.现有以下物质:①NaOH溶液;②蔗糖;③Ba(OH)2固体;④熔融KHSO4;⑤Fe(OH)3胶体;⑥NaHCO3;⑦CO2;⑧CH3COOH;⑨石墨。
(1)以上物质中属于电解质的是
(2)以上物质属于纯净物且能导电的是
II.在如图所示的串联装置中,发现灯泡不亮,但若向其中一个烧杯中加水,则灯泡会亮起来:

(3)加水的烧杯为
(4)向烧杯A滴入Ba(OH)2溶液,溶液导电性
| A.变强 | B.变弱 | C.先变弱后变强 | D.先变强后变弱 |
(5)H3PO4是三元酸,能生成NaH2PO4、Na2HPO4两种酸式盐和Na3PO4一种正盐。磷还有一种含氧酸叫亚磷酸(H3PO3)。已知:H3PO3与NaOH反应只生成NaH2PO3和Na2HPO3两种盐。那么Na2HPO3为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知原电池的总反应式:Cu+2FeCl3=CuCl2+2FeCl2,请写出电极反应式:
(1)正极反应式为_______ ,
(2)负极反应式为_______ 。
(1)正极反应式为
(2)负极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】CO、NOx、SO2都是大气污染物,可利用化学反应原理给予消除。
(1)在一定条件下利用反应2CO(g)+SO2(g)=2CO2(g)+S(s)消除CO、SO2,并获得硫黄。已知常温常压下,硫黄的燃烧热△H=-296kJ·mol-1,CO的燃烧热△H=-283kJ·mol-1,则2CO(g)+SO2(g)=2CO2(g)+S(s) △H=____ 。
(2)利用CO还原NO的反应可消除汽车尾气引起的污染并获得电能,其简易装置如图所示(Na+交换膜两侧为等体积等浓度的NaOH溶液):
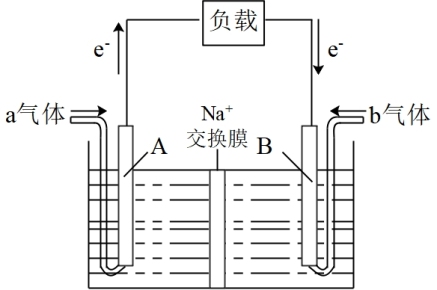
①电极A的电极反应式为____ 。
②工作一段时间后,若B极区与A极区相差0.02molNa+时,外电路中转移电子的物质的量是____ mol。
(3)利用如图所示的电化学装置可消除雾霾中的NO、SO2。

①该装置中电子的流向是____ (填“A→C”或“C→A”)。
②电极B的电极反应式为____ 。
(1)在一定条件下利用反应2CO(g)+SO2(g)=2CO2(g)+S(s)消除CO、SO2,并获得硫黄。已知常温常压下,硫黄的燃烧热△H=-296kJ·mol-1,CO的燃烧热△H=-283kJ·mol-1,则2CO(g)+SO2(g)=2CO2(g)+S(s) △H=
(2)利用CO还原NO的反应可消除汽车尾气引起的污染并获得电能,其简易装置如图所示(Na+交换膜两侧为等体积等浓度的NaOH溶液):

①电极A的电极反应式为
②工作一段时间后,若B极区与A极区相差0.02molNa+时,外电路中转移电子的物质的量是
(3)利用如图所示的电化学装置可消除雾霾中的NO、SO2。

①该装置中电子的流向是
②电极B的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】燃料电池是利用燃料与氧气反应从而将化学能转化为电能的装置。
(1)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。

①A为生物燃料电池的________ (填“正”或“负”)极。
②正极反应式为_____________ 。
③放电过程中,H+由________ 极区向________ 极区迁移(填“正”或“负”)。
④在电池反应中,每消耗1 mol氧气,理论上生成标准状况下二氧化碳的体积是________ 。
(2)一氧化碳无色无味有毒,世界各国每年均有不少人因一氧化碳中毒而失去生命。一种一氧化碳分析仪的工作原理如图所示,该装置中电解质为氧化钇—氧化钠,其中O2-可以在固体介质NASICON中自由移动。传感器中通过的电流越大,尾气中一氧化碳的含量越高。

请回答:
①a极电极反应式为______________ ;
②工作时,O2-由电极________ 向电极________ 移动(填“a”或“b”);
③电子由电极________ 通过传感器流向电极________ (填“a”或“b”)。
(1)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。

①A为生物燃料电池的
②正极反应式为
③放电过程中,H+由
④在电池反应中,每消耗1 mol氧气,理论上生成标准状况下二氧化碳的体积是
(2)一氧化碳无色无味有毒,世界各国每年均有不少人因一氧化碳中毒而失去生命。一种一氧化碳分析仪的工作原理如图所示,该装置中电解质为氧化钇—氧化钠,其中O2-可以在固体介质NASICON中自由移动。传感器中通过的电流越大,尾气中一氧化碳的含量越高。

请回答:
①a极电极反应式为
②工作时,O2-由电极
③电子由电极
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】能源、资源问题是当前人类社会面临的一项重大课题。
(1)燃料电池将能量转化效率比直接燃烧效率高,如图为某种燃料电池的工作原理示意图,a、b均为惰性电极。

使用时,空气从_______ 口通入(填“A”或“B”);
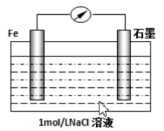
(2)钢铁的腐蚀现象非常普遍,电化学腐蚀是造成钢铁腐蚀的主要原因,某同学按下图进行钢铁腐蚀的模拟,则正极的电极反应式为:_________________ ,当导线中有3.01×1023个电子流过,被腐蚀的铁元素为_______ g。[ 提示:电化学的总反应式为2Fe+2H2O+O2=2Fe(OH)2 ]
(3)海水化学资源的开发利用具有重要的意义和作用,下图是海带中提取碘的示意图:
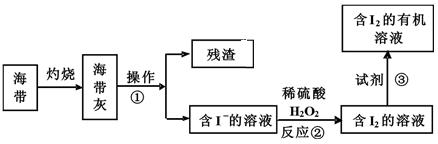
①中操作的名称是_______ ;下述物质中不可做试剂③的是________ 。
A.乙醇 B.苯 C.乙酸 D.四氯化碳
(1)燃料电池将能量转化效率比直接燃烧效率高,如图为某种燃料电池的工作原理示意图,a、b均为惰性电极。

使用时,空气从
(2)钢铁的腐蚀现象非常普遍,电化学腐蚀是造成钢铁腐蚀的主要原因,某同学按下图进行钢铁腐蚀的模拟,则正极的电极反应式为:

(3)海水化学资源的开发利用具有重要的意义和作用,下图是海带中提取碘的示意图:

①中操作的名称是
A.乙醇 B.苯 C.乙酸 D.四氯化碳
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】科学家预言,燃料电池将是21世纪获得电力的重要途径,美国已计划将甲醇燃料电池用于军事目的。一种甲醇(CH3OH)燃料电池是采用铂或碳化钨作为电极催化剂,在稀硫酸电解液中直接加入纯化后的甲醇,同时向一个电极通入空气。回答下列问题:
(1)这种电极放电时发生的总反应是______________________________________ 。
(2)此电极的正极发生的电极反应式是__________________________ ;
负极发生的电极反应式是_______________________________ 。
(3)电解液中的H+离子向_________ 极(正极或负极)移动;通入正极的气体是________ .
(1)这种电极放电时发生的总反应是
(2)此电极的正极发生的电极反应式是
负极发生的电极反应式是
(3)电解液中的H+离子向
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)如图为氢氧燃料电池的构造示意图,根据电子运动方向,可知氧气从__ 口通入(填“a”或“b”),X极为电池的___ (填“正”或“负”)极。
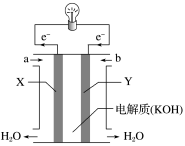
(2)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为
A极:2H2+2O2--4e-=2H2O
B极:O2+4e-=2O2-
则A极是电池的___ 极;电子从该极__ (填“流入”或“流出”)。电池总反应为:___ 。

(2)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为
A极:2H2+2O2--4e-=2H2O
B极:O2+4e-=2O2-
则A极是电池的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据化学反应原理,解决以下问题:
(1)用离子反应方程式表示工业上制烧碱的原理:___________ 。
(2)写出工业上冶炼铝的化学反应方程式:___________ 。
(3)氢氧碱性燃料电池负极的电极反应式为:___________ 。
(4)若适量的NO和O2完全反应,每生成92g NO2需要放出67.8kJ热量,则表示该反应的热化学方程式为___________ 。
(5)已知:Al2O3(s)+3C(s)=2Al(s)+3CO(g) ΔH1=+1344.1 kJ·mol-1
2AlCl3(g)=2Al(s)+3Cl2(g) ΔH2=+1169.2 kJ·mol-1
由Al2O3、C和Cl2反应生成AlCl3的热化学方程式为___________ 。
(1)用离子反应方程式表示工业上制烧碱的原理:
(2)写出工业上冶炼铝的化学反应方程式:
(3)氢氧碱性燃料电池负极的电极反应式为:
(4)若适量的NO和O2完全反应,每生成92g NO2需要放出67.8kJ热量,则表示该反应的热化学方程式为
(5)已知:Al2O3(s)+3C(s)=2Al(s)+3CO(g) ΔH1=+1344.1 kJ·mol-1
2AlCl3(g)=2Al(s)+3Cl2(g) ΔH2=+1169.2 kJ·mol-1
由Al2O3、C和Cl2反应生成AlCl3的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如图是某同学设计的一个简易的原电池装置,请回答下列问题。
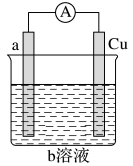
(1)若a电极材料为碳、b溶液为FeCl3溶液,则正极的电极反应式为___________________ ,当有3.2g的负极材料溶解时,导线中转移的电子的数目为________ 。
(2)氢氧燃料电池已用于航天飞机。这种电池以30%KOH溶液为电解质溶液,供电时总反应为2H2+O2===2H2O,则正极的电极反应式为_________________ ,该燃料电池的优点是_______________________ 。
(3)已知H—H键、N—H键、N≡N键的键能分别为436kJ·mol-1、391kJ·mol-1、946kJ·mol-1,关于工业合成氨的反应,请根据键能的数据判断下列问题:
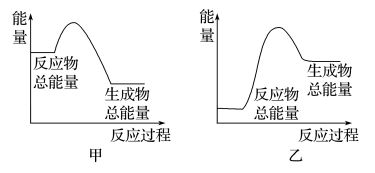
若有1molNH3生成,可________ (填“吸收”或“放出”)热量________ kJ;该反应的能量变化可用图______ (填“甲“或“乙”)表示。

(1)若a电极材料为碳、b溶液为FeCl3溶液,则正极的电极反应式为
(2)氢氧燃料电池已用于航天飞机。这种电池以30%KOH溶液为电解质溶液,供电时总反应为2H2+O2===2H2O,则正极的电极反应式为
(3)已知H—H键、N—H键、N≡N键的键能分别为436kJ·mol-1、391kJ·mol-1、946kJ·mol-1,关于工业合成氨的反应,请根据键能的数据判断下列问题:
若有1molNH3生成,可

您最近一年使用:0次



