下列离子方程式正确的是
| A.铝与盐酸反应:Al + 6H+ = Al3+ + H2↑ |
| B.NaOH溶液与稀醋酸反应:H+ + OH- = H2O |
C.硫酸与氢氧化钡溶液的反应:2H++ +2OH-+Ba2+=BaSO4↓+2H2O +2OH-+Ba2+=BaSO4↓+2H2O |
D.碳酸氢钠溶液中加入盐酸: + 2H+ = CO2↑ + H2O + 2H+ = CO2↑ + H2O |
更新时间:2020-10-21 22:35:15
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】根据酸碱质子理论,给出质子(H+)的物质是酸,给出质子的能力越强,酸性越强,已知:酸性强弱顺序 >
>  >
> >
> ,一定条件下,下列反应合理的是
,一定条件下,下列反应合理的是
 >
>  >
> >
> ,一定条件下,下列反应合理的是
,一定条件下,下列反应合理的是A. + +  → → + + |
B. + + → → + + |
C. + + → → + + |
D. + + → → + + |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列各组离子在指定溶液中一定能大量共存的是
A.使酚酞溶液变红的溶液: 、 、 、 、 、 、 |
B.使紫色石蕊溶液变红的溶液: 、 、 、 、 、 、 |
C.由水电离出的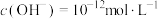 的溶液: 的溶液: 、 、 、 、 、 、 |
D.碳酸铵溶液: 、 、 、 、 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】向盛有少量CuCl2溶液的试管中滴入少量NaOH溶液,再滴入适量浓氨水,下列叙述不正确的是
| A.开始生成蓝色沉淀,加入适量浓氨水后,形成无色溶液 |
| B.Cu(OH)2溶于浓氨水的离子方程式是:Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH- |
| C.开始生成蓝色沉淀,加入适量浓氨水后,沉淀溶解形成深蓝色溶液 |
| D.开始生成Cu(OH)2,之后生成更稳定的配合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】利用含镍电极废料制备 的过程可表示为:
的过程可表示为:

已知:①含镍电极废料中除 外还含有少量
外还含有少量 ,
, 和不溶性杂质
和不溶性杂质
②“酸浸”后溶液中含有 和少量的
和少量的 和
和 ,除杂后方可氧化
,除杂后方可氧化
下列说法错误的是
 的过程可表示为:
的过程可表示为:
已知:①含镍电极废料中除
 外还含有少量
外还含有少量 ,
, 和不溶性杂质
和不溶性杂质②“酸浸”后溶液中含有
 和少量的
和少量的 和
和 ,除杂后方可氧化
,除杂后方可氧化下列说法错误的是
A.由工业流程可知: 的氧化性大于 的氧化性大于 |
B.氧化过程的离子方程式: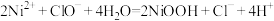 |
C.除杂过程中利用了 、 、 和 和 的溶度积的不同通过调节 的溶度积的不同通过调节 后过滤 后过滤 |
D.利用电解碱性 悬浊液也可以制备 悬浊液也可以制备 ,为提高电解效率可以适当加入一定量 ,为提高电解效率可以适当加入一定量 溶液 溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列离子方程式正确的是
A.氯化铝溶液中加入足量氨水:Al3++4NH3·H2O=AlO +2H2O+4NH +2H2O+4NH |
| B.硫酸亚铁在空气中变质:4Fe2++O2+2H2O=4Fe3++4OH- |
C.澄清石灰水通入过量二氧化碳:OH-+CO2=HCO |
D.少量氯水滴入到碳酸钠溶液中:Cl2+CO =Cl-+ClO-+CO2 =Cl-+ClO-+CO2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列离子方程式正确的是
A.向硅酸钠溶液中通入过量二氧化碳: SiO + 2CO2+ 2H2O = H2SiO3↓+2HCO + 2CO2+ 2H2O = H2SiO3↓+2HCO |
| B.工业上制漂白粉: Cl2+ 2OH- =Cl-+ ClO-+ H2O |
C.明矾溶液与过量氨水混合: Al3++ 4NH3+ 2H2O = AlO +4NH +4NH |
| D.硫化钠溶液与氯化铁溶液反应: 2Fe3+ +3S2-= Fe2S3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列离子方程式书写正确且能用来解释相应实验现象的是
| 实验现象 | 离子方程式 | |
| A | 二氧化硫使酸性高锰酸钾溶液褪色 |  |
| B | 向沸水中滴加饱和氯化铁溶液得到红褐色液体 |  |
| C | 向氢氧化镁悬浊液中滴加氯化铵溶液,沉淀溶解 |  |
| D | 氧化亚铁溶于稀硝酸 | 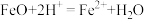 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】用如图所示的装置分别进行如下实验,各离子方程式书写正确且各组物质反应后灯泡亮度变化不大的是


A.向硝酸银溶液中通入少量氯化氢: |
B.向氢氧化钠溶液中通入足量 : : |
C.向 中加入 中加入 : : |
D.向稀硫酸溶液中加入足量铁粉: |
您最近一年使用:0次




