(1)1LAl2(SO4)3和MgSO4的混合溶液中,含Mg2+2.4g,SO 的物质的量浓度为1mol·L-1,则Al3+的物质的量浓度是
的物质的量浓度为1mol·L-1,则Al3+的物质的量浓度是___ ,将该混合液加水稀释至体积为100L,稀释后溶液中MgSO4的物质的量浓度为___ mol·L-1。
(2)若一氧化碳和二氧化碳的混合气体的密度与同温同压下氧气的密度相同,混合气体中二氧化碳所占的质量分数为( )
A.75.0% B.25.0% C.65.625% D.34.375%
 的物质的量浓度为1mol·L-1,则Al3+的物质的量浓度是
的物质的量浓度为1mol·L-1,则Al3+的物质的量浓度是(2)若一氧化碳和二氧化碳的混合气体的密度与同温同压下氧气的密度相同,混合气体中二氧化碳所占的质量分数为
A.75.0% B.25.0% C.65.625% D.34.375%
更新时间:2020-10-23 01:09:23
|
相似题推荐
填空题
|
较难
(0.4)
名校
【推荐1】(1)一个密闭容器,中间有一可自由滑动的隔板(厚度可忽略)将容器分成两部分,当左边充入1molN2,右边充入CO和CO2的混合气体共8g时,隔板处于如图位置(左、右两侧温度相同)。右侧CO与CO2分子数之比为________________ ;

(2)已知质量分数为28%的氨水物质的量浓度为12 mol·L-l,则质量分数为14%的氨水物质的量浓度_____ (填“大于”、“小于”或“等于”) 6 mol·L-l;已知4 mol·L-l 的硫酸溶液密度为 ,2 mol·L-l 的硫酸溶液密度为
,2 mol·L-l 的硫酸溶液密度为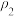 。100g浓度为4mol·L-l 的硫酸溶液与
。100g浓度为4mol·L-l 的硫酸溶液与________ mL水混合,使硫酸的物质的量浓度减小到2 mol·L-l 。(用含 、
、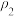 的式子表示)
的式子表示)

(2)已知质量分数为28%的氨水物质的量浓度为12 mol·L-l,则质量分数为14%的氨水物质的量浓度
 ,2 mol·L-l 的硫酸溶液密度为
,2 mol·L-l 的硫酸溶液密度为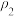 。100g浓度为4mol·L-l 的硫酸溶液与
。100g浓度为4mol·L-l 的硫酸溶液与 、
、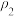 的式子表示)
的式子表示)
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】碳及其化合物广泛存在于自然界中,试回答下列问题:
(1)某处碳循环如图所示,CaCO3转化为HCO3-的离子方程式为_____________ 。
(2)常温常压下,空气中的CO2溶于水,达到平衡时,无机碳在浓液中以4种形式存在,其转化关系如下:
①CO2(g)+H2O H2CO3 K=10-2.8
H2CO3 K=10-2.8
②H2CO3 H++HCO3- K1=10-3.5,
H++HCO3- K1=10-3.5,
③HCO3- H++CO32- K2=10-10.3,
H++CO32- K2=10-10.3,
若溶液中。c(CO2)=1.0×10-5mol/L,且忽略水的电离及H2CO3的第二级电离,则溶液pH=_____ 。
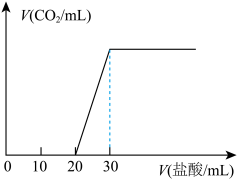
(3)某化学小组为了测量湖水中无机碳的含量,量取 100mL湖水,酸化后用N2吹出CO2,再用NaOH溶液吸收,将吸收液用0.10mol/L盐酸滴定,生成的V(CO2)随V (盐酸)变化关系如图所示,则吸收液中离子浓度由大到小的顺序为______________ (不用写出H+),湖水中无机碳的浓度为_______ mol/L。
(4)—定条件下,CO2和H2O可以转化为CO和H2,通过反应:CO(g)+2H2(g) CH3OH(g)制备甲醇,若起始时在密闭容器中按物质的量之比1:2充入CO和H2,测得平衡时CO转化率a (CO)随T、P的变化关系如图所示。
CH3OH(g)制备甲醇,若起始时在密闭容器中按物质的量之比1:2充入CO和H2,测得平衡时CO转化率a (CO)随T、P的变化关系如图所示。
①P1______ P2(填“大于”、“小于”或“等于”);
②该反应在195℃、P2条件下达到平衡后,c(H2)=0.5 mol/L ,则该反应的平衡常数为______ 。
③已知CH3OH和CO的燃烧热分别725.8kJ/mol、283.0 kJ/mol,1mol液态水变成气态水吸热44.0kJ,写出甲醇不完全燃烧生成一氧化碳和气态水的热化学方程式:_______ 。
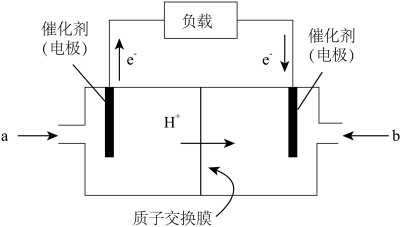
(5)用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图,则c电极的反应方程式为:__________ 。
(1)某处碳循环如图所示,CaCO3转化为HCO3-的离子方程式为
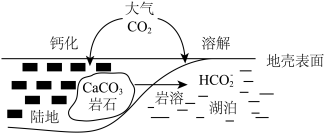
(2)常温常压下,空气中的CO2溶于水,达到平衡时,无机碳在浓液中以4种形式存在,其转化关系如下:
①CO2(g)+H2O
 H2CO3 K=10-2.8
H2CO3 K=10-2.8②H2CO3
 H++HCO3- K1=10-3.5,
H++HCO3- K1=10-3.5,③HCO3-
 H++CO32- K2=10-10.3,
H++CO32- K2=10-10.3,若溶液中。c(CO2)=1.0×10-5mol/L,且忽略水的电离及H2CO3的第二级电离,则溶液pH=
(3)某化学小组为了测量湖水中无机碳的含量,量取 100mL湖水,酸化后用N2吹出CO2,再用NaOH溶液吸收,将吸收液用0.10mol/L盐酸滴定,生成的V(CO2)随V (盐酸)变化关系如图所示,则吸收液中离子浓度由大到小的顺序为
(4)—定条件下,CO2和H2O可以转化为CO和H2,通过反应:CO(g)+2H2(g)
 CH3OH(g)制备甲醇,若起始时在密闭容器中按物质的量之比1:2充入CO和H2,测得平衡时CO转化率a (CO)随T、P的变化关系如图所示。
CH3OH(g)制备甲醇,若起始时在密闭容器中按物质的量之比1:2充入CO和H2,测得平衡时CO转化率a (CO)随T、P的变化关系如图所示。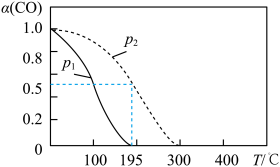
①P1
②该反应在195℃、P2条件下达到平衡后,c(H2)=0.5 mol/L ,则该反应的平衡常数为
③已知CH3OH和CO的燃烧热分别725.8kJ/mol、283.0 kJ/mol,1mol液态水变成气态水吸热44.0kJ,写出甲醇不完全燃烧生成一氧化碳和气态水的热化学方程式:
(5)用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图,则c电极的反应方程式为:
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】现取25.6g Cu与200ml某浓度的浓HNO3反应,当铜完全溶解后,收集到产生的NO和NO2混合气体在标准状况下的体积共11.2L,则:
(1)NO2的体积为__________ L。
(2)反应中消耗HNO3的物质的量为____________ mol。
(3)将盛有NO和NO2混合气体的容器倒扣在水中,容器内液面上升, 再通入标准状况下一定体积的O2,恰好使气体完全溶解,则通入O2的 体积是__________ L。
(4)向溶液中加入500ml、4mol•L-1NaOH溶液,恰好使溶液中的Cu2+全部转化为沉淀,则原硝酸溶液的浓度为__________ mol•L-1。
(1)NO2的体积为
(2)反应中消耗HNO3的物质的量为
(3)将盛有NO和NO2混合气体的容器倒扣在水中,容器内液面上升, 再通入标准状况下一定体积的O2,恰好使气体完全溶解,则通入O2的 体积是
(4)向溶液中加入500ml、4mol•L-1NaOH溶液,恰好使溶液中的Cu2+全部转化为沉淀,则原硝酸溶液的浓度为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】向1 L水中通入560 L NH3 (已折算为标准状况的体积),从而形成密度为 0.858g·cm-3的氨水(溶质为NH3),求:
(1)560 L氨气的物质的最为________ mol。
(2)氨水的质量分数为_____ (保留三位有效数字)。
(3)氨水的物质的量浓度_______ 。(列出计算过程)
(1)560 L氨气的物质的最为
(2)氨水的质量分数为
(3)氨水的物质的量浓度
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】向100mLBaCl2、AlCl3和FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生的沉淀的物质的量(n)和加入溶液B的体积(V)关系如图。
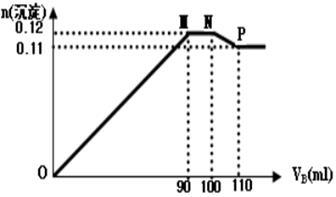
(1)当加入B溶液110mL时,溶液中的沉淀为(化学式)____________________
(2)从90 mL至100 mL之间加入10 mL B溶液时发生的离子反应方程式①_________________ ;②________________ ;并由此可以分析出溶液B中Na2SO4与NaOH物质的量浓度之比为________________ 。
(3)通过计算分析可知:
B溶液中NaOH物质的量浓度为_____________ mol/L;
A溶液中FeCl3物质的量浓度为______________ mol/L。

(1)当加入B溶液110mL时,溶液中的沉淀为(化学式)
(2)从90 mL至100 mL之间加入10 mL B溶液时发生的离子反应方程式①
(3)通过计算分析可知:
B溶液中NaOH物质的量浓度为
A溶液中FeCl3物质的量浓度为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】某结晶水合物A含有两种阳离子和一种阴离子。将溶有90.60gA的水溶液分成两等份,向第一份逐滴加入NaOH溶液,溶液先出现白色沉淀后完全溶解,此过程中产生2.24 L(标准状况)刺激性气味的气体。向第二份加入过量的Ba(OH)2溶液,过滤,用稀硝酸处理沉淀物,经洗涤和干燥,得到白色固体46.60 g。
请回答以下问题:
(1)A的摩尔质量为 。
(2)试通过计算确定该结晶水合物的化学式为 。
(3)若第二份加入75.00 mL2.00 mol·L-1的Ba(OH)2溶液,则得到的沉淀质量为 。
请回答以下问题:
(1)A的摩尔质量为 。
(2)试通过计算确定该结晶水合物的化学式为 。
(3)若第二份加入75.00 mL2.00 mol·L-1的Ba(OH)2溶液,则得到的沉淀质量为 。
您最近一年使用:0次



