下列与化学反应能量变化相关的叙述正确的是
| A.根据能量守恒定律,生成物总能量一定等于反应物总能量 |
| B.放热反应的反应速率一定大于吸热反应的反应速率 |
| C.表示中和热的热化学方程式:NaOH+HCl=NaCl+H2O ΔH=-57.3kJ∙mol﹣1 |
| D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH相同 |
更新时间:2020-10-29 14:33:26
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列叙述或书写正确的是
A.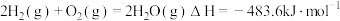 ,则1mol氢气的燃烧热小于 ,则1mol氢气的燃烧热小于 |
B.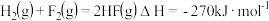 ,则相同条件下, ,则相同条件下,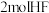 气体的能量小于1mol氢气和1mol氟气的能量之和 气体的能量小于1mol氢气和1mol氟气的能量之和 |
C.含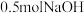 的稀溶液与稀盐酸完全中和,放出 的稀溶液与稀盐酸完全中和,放出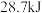 的热量,则表示该中和反应的热化学方程式为 的热量,则表示该中和反应的热化学方程式为 |
D. 、30MPa时,发生反应 、30MPa时,发生反应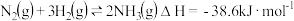 。在此条件下将 。在此条件下将 和过量 和过量 充分反应,放出热量 充分反应,放出热量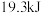 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】如图所示为某基元反应过程的能量变化(E1、E2、E3均大于0)。下列说法正确的是
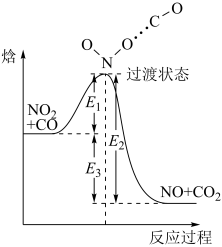

| A.该反应的正反应为吸热反应 |
| B.E1+E3为该反应的活化能 |
| C.图中对应的该反应的焓变△H=-E2 |
| D.NO2和CO分子发生有效碰撞才能形成过渡状态分子 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】在如图所示的装置中进行中和反应。通过测定反应过程中放出的热量可测定中和热。下列关于该实验的说法正确的是( )
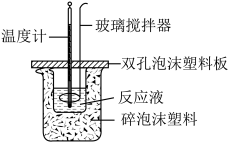

| A.烧杯间的碎泡沫塑料的作用是固定烧杯的位置 |
| B.如果没有环形玻璃搅拌棒,酸碱混合后可用温度计轻轻搅拌 |
| C.做完一次完整的中和热测定实验,温度计需要使用2次,混合液的初始温度和反应最高温度 |
| D.由H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ•mol-l可知,1mol稀H2SO4溶液与2molNaOH溶液反应的中和热为57.3kJ•mol-l |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列各组热化学方程式中,ΔH前者大于后者的是
| A.S(g)+O2(g)=SO2(g) ΔH1 S(s)+O2(g)=SO2(g) ΔH2 |
| B.CaCO3(s)=CaO(s)+CO2(g) ΔH1 CaO(s)+H2O(l)=Ca(OH)2(s) ΔH2 |
| C.1/2H2SO4(浓,aq)+NaOH(aq)=1/2Na2SO4(aq)+H2O(l) ΔH1 HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l) ΔH2 |
| D.C(s)+O2(g)=CO2(g) ΔH1 C(s)+1/2O2(g)=CO(g) ΔH2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】有关能量的判断或表示方法正确的是
A.从 ,可知:金刚石比石墨更稳定 ,可知:金刚石比石墨更稳定 |
B.已知中和热 ,则1mol硫酸与足量氢氧化钡溶液反应放热为114.6kJ ,则1mol硫酸与足量氢氧化钡溶液反应放热为114.6kJ |
C. 的燃烧热是 的燃烧热是 ,则 ,则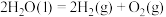 反应的 反应的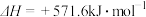 |
D.一定条件下,将0.5mol 和1.5mol 和1.5mol 置于密闭的容器中充分反应生成 置于密闭的容器中充分反应生成 ,放热19.3kJ,其热化学方程式为: ,放热19.3kJ,其热化学方程式为: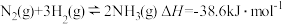 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】标准状态下,下列物质气态时的相对能量如表;可根据HO(g)+HO(g)=H2O2(g)计算出H2O2中氧氧单键的键能为214kJ mol-1。下列说法
mol-1。下列说法不正确 的是
 mol-1。下列说法
mol-1。下列说法| 物质(g) | O | H | HO | HOO | H2 | O2 | H2O2 | H2O |
能量/ | 249 | 218 | 39 | 10 | 0 | 0 | -136 | -242 |
A.H2的键能为436kJ mol-1 mol-1 |
| B.O2的键能大于H2O2中氧氧单键的键能的两倍 |
| C.解离氧氧单键所需能量:HOO<H2O2 |
D.H2O(g)+O(g)=H2O2(g)  -143kJ -143kJ mol-1 mol-1 |
您最近一年使用:0次


 2SO3(g)△H=-196kJ/mol(反应热)
2SO3(g)△H=-196kJ/mol(反应热) 2NH3(g)
2NH3(g)

