有一包白色粉末,可能含有 Na2SO4、CaCO3、KCl、BaCl2、CuSO4 中的一种或几种,按以下步骤进行实验:
①将此粉末溶于水,得到无色溶液和白色沉淀;
②将足量稀盐酸加入白色沉淀中,沉淀部分溶解,并有气泡产生。
(1)根据上述实验现象,判断此粉末中一定含有的物质是______ 、________ _________ ,一定没有的物质是__________ ,可能含有的物质是____________ (均填写化学式)。
(2)上述实验中反应的离子方程式是__________________________________________ 。
①将此粉末溶于水,得到无色溶液和白色沉淀;
②将足量稀盐酸加入白色沉淀中,沉淀部分溶解,并有气泡产生。
(1)根据上述实验现象,判断此粉末中一定含有的物质是
(2)上述实验中反应的离子方程式是
15-16高一上·福建厦门·期中 查看更多[10]
河北省石家庄市河北师范大学附属中学2022-2023学年高一上学期十月月考化学试题湖南省怀化市第五中学2021-2022学年高一上学期期中考试化学试题黑龙江省绥化市明水县第一中学2020-2021学年高一上学期第一次月考化学试题安徽省安庆市怀宁县第二中学2019-2020学年高一上学期期中考试化学试题四川省阆中中学2020-2021学年高一上学期开学考试化学试题辽宁省营口市第二高级中学2019-2020学年高一上学期第一次月考化学试题江苏省南通市启东中学2020年人教版高中化学必修一期末复习第二章 化学物质及其变化(一)辽宁省朝阳市凌源三中2019-2020学年高一上学期第二次月考化学试题【全国百强校】江苏省南京市南京师范大学附属中学2017-2018学年高一上学期期中考试化学试题2015-2016学年福建厦门双十中学高一上期中考试化学试卷
更新时间:2020-10-31 12:09:26
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某校化学小组学生利用下图所列装置进行“铁与水反应”的实验,并利用产物进一步制取FeCl3·6H2O晶体。(图中夹持及尾气处理装置均已略去)

(1)装置B中发生反应的化学方程式是________________________________ ;
(2)装置E中的现象是______________________________________________ 。
(3)装置C中右侧导管为什么既不插入试管底部,又不只进入试管一点点,其主要原因是___________ .
(4)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤.该小组学生利用上述滤液制取FeCl3·6H2O晶体,设计流程如下:
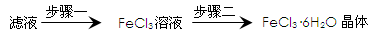
①步骤一中通入足量Cl2发生反应的离子方程式为_______________________________________ 。
②步骤二,从FeCl3稀溶液中得到FeCl3・6H2O晶体的主要操作包括______________ .

(1)装置B中发生反应的化学方程式是
(2)装置E中的现象是
(3)装置C中右侧导管为什么既不插入试管底部,又不只进入试管一点点,其主要原因是
(4)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤.该小组学生利用上述滤液制取FeCl3·6H2O晶体,设计流程如下:
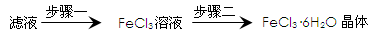
①步骤一中通入足量Cl2发生反应的离子方程式为
②步骤二,从FeCl3稀溶液中得到FeCl3・6H2O晶体的主要操作包括
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】电子工业上使用的印刷电路板,是在敷有铜膜的塑料板上以涂层保护所要的线路,然后用三氯化铁浓溶液作用掉(腐蚀)未受保护的铜膜后形成的。某工程师为了从使用过的腐蚀废液(含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费)中回收铜,并将铁的化合物全部转化为FeCl3溶液作为腐蚀液原料循环使用,准备采用下列步骤:
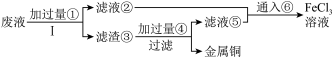
(1)写出FeCl3溶液与铜箔发生反应的离子方程式:____________ 。
(2)检验废腐蚀液中是否含有Fe3+所需试剂名称:________ ,实验现象:______________ 。
(3)向②中加入NaOH溶液并长时间暴露在空气中,此过程的现象:___________ ,此转化的化学方程式为:______________ 。
(4)写出③中所含物质:________ ,⑥发生反应的离子方程式:_______ 。

(1)写出FeCl3溶液与铜箔发生反应的离子方程式:
(2)检验废腐蚀液中是否含有Fe3+所需试剂名称:
(3)向②中加入NaOH溶液并长时间暴露在空气中,此过程的现象:
(4)写出③中所含物质:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】亚氯酸钠(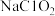 )主要用于棉纺、造纸业的漂白,也用于食品消毒、水处理等。以氯酸钠等为原料制备亚氯酸钠的工艺流程如下:
)主要用于棉纺、造纸业的漂白,也用于食品消毒、水处理等。以氯酸钠等为原料制备亚氯酸钠的工艺流程如下:

已知:①亚氯酸钠( )受热易分解;
)受热易分解;
②高浓度的 易爆炸;
易爆炸;
③“反应1”涉及的反应符号表达为 (未配平)。
(未配平)。
回答下列问题:
(1)写出“反应1”涉及的反应离子方程式:_______ ;该反应每生成67.5g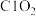 需要消耗
需要消耗_______ g 气体,“反应1”需要鼓入空气,空气的作用是
气体,“反应1”需要鼓入空气,空气的作用是_______ 。
(2)“反应2”生成 、
、 和
和 的化学方程式为
的化学方程式为_______ ,每生成1个 分子,转移电子的数目为
分子,转移电子的数目为_______ ;“反应2”需要控制反应温度不能过高,温度过高可能导致_______ 。
(3) 可以通过“冷却结晶”的方式提纯的原因是
可以通过“冷却结晶”的方式提纯的原因是_______ (从溶解度角度分析)。
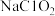 )主要用于棉纺、造纸业的漂白,也用于食品消毒、水处理等。以氯酸钠等为原料制备亚氯酸钠的工艺流程如下:
)主要用于棉纺、造纸业的漂白,也用于食品消毒、水处理等。以氯酸钠等为原料制备亚氯酸钠的工艺流程如下:
已知:①亚氯酸钠(
 )受热易分解;
)受热易分解;②高浓度的
 易爆炸;
易爆炸;③“反应1”涉及的反应符号表达为
 (未配平)。
(未配平)。回答下列问题:
(1)写出“反应1”涉及的反应离子方程式:
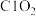 需要消耗
需要消耗 气体,“反应1”需要鼓入空气,空气的作用是
气体,“反应1”需要鼓入空气,空气的作用是(2)“反应2”生成
 、
、 和
和 的化学方程式为
的化学方程式为 分子,转移电子的数目为
分子,转移电子的数目为(3)
 可以通过“冷却结晶”的方式提纯的原因是
可以通过“冷却结晶”的方式提纯的原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】有一瓶溶液,其中可能含有H+、NH4+、K+、Na+、Mg2+、Ba2+、Fe3+、CO32-、SO42-、Cl-和I-。取该溶液进行了以下实验:
(1)用pH试纸检验,表明溶液呈强酸性;
(2)取部分溶液,加入数滴氯水及2 mL CCl4,经振荡后CCl4层呈紫红色;
(3)另取部分溶液,加入NaOH 溶液使其变为碱性,无沉淀生成;
(4)取部分上述碱性溶液,加Na2CO3溶液,有白色沉淀生成;
(5)将(3)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝;根据上述实验事实,可知原溶液中肯定含有的离子是___________ ;肯定没有的离子是_____________ ;还不能确定是否含有的离子是_____________ 。
(1)用pH试纸检验,表明溶液呈强酸性;
(2)取部分溶液,加入数滴氯水及2 mL CCl4,经振荡后CCl4层呈紫红色;
(3)另取部分溶液,加入NaOH 溶液使其变为碱性,无沉淀生成;
(4)取部分上述碱性溶液,加Na2CO3溶液,有白色沉淀生成;
(5)将(3)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝;根据上述实验事实,可知原溶液中肯定含有的离子是
您最近一年使用:0次
【推荐2】某混合物澄清透明的水溶液中,可能含有以下离子中的若干种:K+、Ca2+、Fe2+、Cu2+、Cl-、 、
、 ,现每次取100.00mL该溶液进行以下实验:
,现每次取100.00mL该溶液进行以下实验:
①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量BaCl2溶液后生成沉淀,洗涤后干燥沉淀6.27g,再将该沉淀加入足量盐酸溶解后再过滤洗涤干燥后得沉淀2.33g。
请回答下列问题:
(1)根据以上实验判断,原溶液中一定不存在的离子是_______ ,可能存在的离子是_______ 。要确定可能含有的离子,还需要进行的实验操作是_______ ,写出沉淀与盐酸反应的离子方程式为_______ 。
(2)原溶液中一定存在的阳离子为_______ ,其物质的量浓度至少为_______ mol∙L-1。
(3)原溶液中一定存在的阴离子是_______ ,其物质的量浓度为_______ mol∙L-1、_______ mol∙L-1。
 、
、 ,现每次取100.00mL该溶液进行以下实验:
,现每次取100.00mL该溶液进行以下实验:①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量BaCl2溶液后生成沉淀,洗涤后干燥沉淀6.27g,再将该沉淀加入足量盐酸溶解后再过滤洗涤干燥后得沉淀2.33g。
请回答下列问题:
(1)根据以上实验判断,原溶液中一定不存在的离子是
(2)原溶液中一定存在的阳离子为
(3)原溶液中一定存在的阴离子是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】Ⅰ.已知某KNO3溶液A中,混有少量的Ca2+和SO42-等杂质,某同学设计了如下实验方案以制得纯净的KNO3固体。
根据上述回答:
(1)沉淀D中所含有的物质是___ .
(2)按上述实验方案制得的KNO3晶体,经分析测定仍含有杂质,其原因是上述第____ 步(填①、②、③)可能存在问题,请加以完善:________________________________________ 。
Ⅱ.有A、B、C三种可溶性盐,阴、阳离子各不相同,其阴离子的摩尔质量按A、B、C的顺序依次减小。
将等物质的量的A、B、C溶于水,所得溶液中只含有Al3+、Na+、SO42-、NO3-、Cl-五种离子,同时生成一种白色沉淀。请回答下列问题:
(1)经检验,三种正盐中还含有下列选项中的一种离子,该离子是_______ 。
A.NH4+ B.Ba2+ C.Mg2+ D.Cu2+
(2)写出A的化学式:_________ 。
(3)若将A、B、C三种盐按一定比例溶于水,所得溶液中只含有Al3+、Cl-、NO3-、Na+四种离子且物质的量之比依次为1:1:3:1(不考虑水电离的影响)。则A、B、C三种盐的物质的量之比为____________ 。

根据上述回答:
(1)沉淀D中所含有的物质是
(2)按上述实验方案制得的KNO3晶体,经分析测定仍含有杂质,其原因是上述第
Ⅱ.有A、B、C三种可溶性盐,阴、阳离子各不相同,其阴离子的摩尔质量按A、B、C的顺序依次减小。
将等物质的量的A、B、C溶于水,所得溶液中只含有Al3+、Na+、SO42-、NO3-、Cl-五种离子,同时生成一种白色沉淀。请回答下列问题:
(1)经检验,三种正盐中还含有下列选项中的一种离子,该离子是
A.NH4+ B.Ba2+ C.Mg2+ D.Cu2+
(2)写出A的化学式:
(3)若将A、B、C三种盐按一定比例溶于水,所得溶液中只含有Al3+、Cl-、NO3-、Na+四种离子且物质的量之比依次为1:1:3:1(不考虑水电离的影响)。则A、B、C三种盐的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D四种可溶性盐,其阳离子分别是Na+、Ba2+、Cu2+、Ag+中的某一种,阴离子分别是Cl-、 、
、 、
、 中的某一种。(离子在物质中不重复出现)现做以下实验:
中的某一种。(离子在物质中不重复出现)现做以下实验:
①将四种盐各取少量,分别溶于盛有5 mL蒸馏水的4支试管中,只有B盐溶液呈蓝色。
②分别向4支试管中加入2 mL稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
(1)根据上述实验事实,推断这四种盐的化学式分别为A___________ ;B___________ ;C___________ ;D___________ 。
(2)写出下列反应的离子方程式:
①A+D:___________ ;
②B+D:___________ ;
③C溶液中滴加少量稀盐酸(无气体产生):___________ 。
 、
、 、
、 中的某一种。(离子在物质中不重复出现)现做以下实验:
中的某一种。(离子在物质中不重复出现)现做以下实验:①将四种盐各取少量,分别溶于盛有5 mL蒸馏水的4支试管中,只有B盐溶液呈蓝色。
②分别向4支试管中加入2 mL稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
(1)根据上述实验事实,推断这四种盐的化学式分别为A
(2)写出下列反应的离子方程式:
①A+D:
②B+D:
③C溶液中滴加少量稀盐酸(无气体产生):
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】有A、B、C、D四种化合物,分别由K+、Ba2+、SO 、CO
、CO 、OH-中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水但溶于盐酸并放出无色无味的气体E;③C的水溶液呈碱性,与稀硫酸反应生成A;④D可溶于水,与稀硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
、OH-中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水但溶于盐酸并放出无色无味的气体E;③C的水溶液呈碱性,与稀硫酸反应生成A;④D可溶于水,与稀硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
(1)推断A、B、D的化学式:A:__ ;B:___ ;C:__ ;D:__ ;E:__ 。
(2)写出下列反应的离子方程式。
①D与氯化钙溶液反应:__ ;
②C与硫酸铜溶液反应:__ ;
③B与稀盐酸溶液反应:__ 。
 、CO
、CO 、OH-中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水但溶于盐酸并放出无色无味的气体E;③C的水溶液呈碱性,与稀硫酸反应生成A;④D可溶于水,与稀硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
、OH-中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水但溶于盐酸并放出无色无味的气体E;③C的水溶液呈碱性,与稀硫酸反应生成A;④D可溶于水,与稀硫酸作用时放出气体E,E可使澄清石灰水变浑浊。(1)推断A、B、D的化学式:A:
(2)写出下列反应的离子方程式。
①D与氯化钙溶液反应:
②C与硫酸铜溶液反应:
③B与稀盐酸溶液反应:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】某强酸性溶液X中含有Ba2+、Al3+、NH 、Fe2+、Fe3+、CO
、Fe2+、Fe3+、CO 、SO
、SO 、SO
、SO 、Cl-、NO
、Cl-、NO 中的一种或几种,取该溶液进行连续实验,实验过程如下:
中的一种或几种,取该溶液进行连续实验,实验过程如下:

已知:气体D在常温常压下呈现红棕色。
(1)上述离子中,溶液X中除H+外还肯定含有的离子是___________ ,不能确定是否含有的离子(Q)是____________
(2)写出生成A的离子方程式:_______________
(3)写出气体D与足量氧气反应生成E的化学方程式:_____________
 、Fe2+、Fe3+、CO
、Fe2+、Fe3+、CO 、SO
、SO 、SO
、SO 、Cl-、NO
、Cl-、NO 中的一种或几种,取该溶液进行连续实验,实验过程如下:
中的一种或几种,取该溶液进行连续实验,实验过程如下:
已知:气体D在常温常压下呈现红棕色。
(1)上述离子中,溶液X中除H+外还肯定含有的离子是
(2)写出生成A的离子方程式:
(3)写出气体D与足量氧气反应生成E的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】有一瓶澄清的溶液,其中可能含有NH4+、K+、Na+、Mg2+、Ba2+、Fe3+、SO42―、CO32―、Cl―和I―。取该溶液进行了以下实验:(1)用pH试纸检验,表明溶液呈强酸性;(2)取部分溶液,加入CCl4及数滴氯水,经振荡后CCl4层呈紫红色;(3)另取部分溶液,加入稀NaOH 溶液使其变为碱性,溶液中无沉淀生成;(4)取部分上述碱性溶液,加Na2CO3溶液有白色沉淀生成;(5)将(3)得到的碱性溶液加热,有气体放出,该气体能使润湿的红色石蕊试纸变蓝。根据上述实验事实填空:
①该溶液中肯定含有的离子是____________________________ ;
②还不能确定是否存在的离子是_________________________ ;
③请写出检验Cl―的方法_____________________ 。
①该溶液中肯定含有的离子是
②还不能确定是否存在的离子是
③请写出检验Cl―的方法
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】有一包白色固体粉末,其中可能含有KMnO4、NaNO3、BaCl2、Na2SO4、Na2CO3中的一种或几种,现做以下实验:
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤后溶液呈无色;
②向①的沉淀物中加入足量稀硝酸,固体部分溶解,并有气泡产生;
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生;
④另取①中过滤后的溶液于试管中,向该试管中加入足量硝酸银溶液产生白色沉淀。
试根据上述实验事实,回答下列问题:
(1)原白色粉末中一定不含有的物质是__________ (填化学式,下同),一定含有的物质是_____________ ,可能含有的物质是______________ 。
(2)写出下列步骤中发生的离子方程式:
①________
②________
④_______
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤后溶液呈无色;
②向①的沉淀物中加入足量稀硝酸,固体部分溶解,并有气泡产生;
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生;
④另取①中过滤后的溶液于试管中,向该试管中加入足量硝酸银溶液产生白色沉淀。
试根据上述实验事实,回答下列问题:
(1)原白色粉末中一定不含有的物质是
(2)写出下列步骤中发生的离子方程式:
①
②
④
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某溶液可能含Cl-、SO42-、CO32-、Cu2+、Ba2+和Na+。探究小组为了确定该溶液中离子的组成,取该溶液 100mL 进行以下实验:(填写下表空格)
若 100mL 溶液中含有 0.3mol Na+,则向步骤三的滤液中加入足量 AgNO3 溶液, 过滤、洗涤、干燥,可得到______________ g 白色沉淀[保留小数点后一位]。
| 实验操作与现象 | 实验结论 | 判断理由 | |
| 步骤一 | 加入过量NaOH溶液,得到蓝色沉淀; | 肯定有 Cu2+、肯定无 | 肯定无该离子的理由 |
| 步骤二 | 将蓝色沉淀过滤、洗涤、灼烧得到24.0g 固体; | Cu2+物质的量浓度为 | Cu 元素守恒。过滤所用玻璃仪器有烧杯、 |
| 步骤三 | 向上述滤液中加足量Ba(NO3)2溶液,得到46.6g不溶于稀硝酸的沉淀。 | 肯定有Cl-、 | 相应的离子方程式: |
您最近一年使用:0次



