(1)在标准状况下,有物质①44. 8 LH2,②24 gCH4,③l molH2O,④3. 01×1023个O2,含分子数最多的是_____ (填序号,下同),含电子数最多的是________ ,质量最大的是________ ,体积最小的是________ ;
(2)选择下列实验方法分离物质,将分离方法的序号填在横线上。
a、萃取分液法;b、 加热分解; c、结晶法;d、 分液法;e、蒸馏法;f、 过滤法
①________ 从硝酸钾 和氯化钠的混合溶液中获得硝酸钾
②________ 分离水和苯的混合物
③________ 分离碘和四氯化碳
④________ 分离食盐水和沙子的混合物
(3)以下6种为中学化学中常见的物质:①Cu;②NaHSO4;③SO3;④H2SO4;⑤CaCO3;⑥Cu(OH)2。请按下列分类标准回答问题:
属于电解质的是_________ ;在水中能电离出H+的是_________ ;属于酸的是_________ ;属于碱的是________ 。
(2)选择下列实验方法分离物质,将分离方法的序号填在横线上。
a、萃取分液法;b、 加热分解; c、结晶法;d、 分液法;e、蒸馏法;f、 过滤法
①
②
③
④
(3)以下6种为中学化学中常见的物质:①Cu;②NaHSO4;③SO3;④H2SO4;⑤CaCO3;⑥Cu(OH)2。请按下列分类标准回答问题:
属于电解质的是
更新时间:2020-11-03 15:40:05
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】“宏观辨识与微观探析”是化学核心素养之一。
二氧化碳转化为甲醇(CH3OH)的反应微观示意图如下:
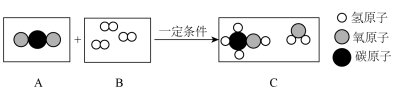
(1)B框中的物质属于_______ (选填“混合物”、“化合物”、“氧化物”或“单质”)。
(2)参加反应的A、B分子个数比为_________ 。
(3)该反应的化学方程式为____________________________________________ 。
二氧化碳转化为甲醇(CH3OH)的反应微观示意图如下:

(1)B框中的物质属于
(2)参加反应的A、B分子个数比为
(3)该反应的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】以下9种物质为中学化学中常见的物质:①Cu②NaHSO4③SO3④H2SO4⑤C2H5OH⑥BaSO4⑦Cu(OH)2⑧NaOH⑨CH3COOH,请按下列分类标准回答问题。
(1)属于电解质的是___ ,属于非电解质的是___ 。(填序号,下同)
(2)能电离出H+的是___ ,属于酸的是___ 。
(3)属于碱的是___ ,其中属于难溶性盐的是___ 。
(4)请写出NaHSO4溶解于水的电离方程式___ 。请写出CH3COOH溶解于水的电离方程式___ 。
(1)属于电解质的是
(2)能电离出H+的是
(3)属于碱的是
(4)请写出NaHSO4溶解于水的电离方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】科学家在研究化学物质时,常常对物质进行分类,以便对同类物质的组成和性能进行深入的研究。物质分类及转化思想贯穿整个化学科学习的始终。
(1)SiO2是普通玻璃的主要成分,与CO2一样是酸性氧化物,写出SiO2溶于NaOH溶液的化学方程式:_______ 。
(2)现有:①KCl晶体②稀盐酸③氨气④熔融NaCl⑤蔗糖⑥铜⑦CO2;其中能导电的是_______ (填序号,下同);属于电解质的是_______ ;属于非电解质的是_______ 。
(3)有下列六个反应:
A.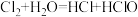
B.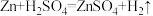
C.
D.
E.
F.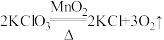
其中属于置换反应的是_______ ,既属于分解反应又属于氧化还原反应的是_______ (填字母)。
(1)SiO2是普通玻璃的主要成分,与CO2一样是酸性氧化物,写出SiO2溶于NaOH溶液的化学方程式:
(2)现有:①KCl晶体②稀盐酸③氨气④熔融NaCl⑤蔗糖⑥铜⑦CO2;其中能导电的是
(3)有下列六个反应:
A.
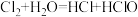
B.
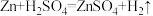
C.

D.

E.

F.
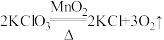
其中属于置换反应的是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】按要求回答下列问题:
(1)反应 在化学上被称为“铝热反应”,人们可利用该反应来焊接铁轨。该反应中,
在化学上被称为“铝热反应”,人们可利用该反应来焊接铁轨。该反应中,___________ (填化学式,下同)是氧化剂,___________ 是还原剂。
(2)写出氢氧化钡在水溶液中的电离方程式:___________ 。
(3)写出金属钠与水反应的离子方程式:___________ 。
(4) 可在呼吸面具和潜水艇中作为氧气的来源,请写出
可在呼吸面具和潜水艇中作为氧气的来源,请写出 与
与 反应的化学方程式
反应的化学方程式__________ 。
(5) 个
个 的物质的量是
的物质的量是___________ ,在标准状况下的体积为___________ 。
(6) 个
个 分子中共含有
分子中共含有___________ 个质子。
(1)反应
 在化学上被称为“铝热反应”,人们可利用该反应来焊接铁轨。该反应中,
在化学上被称为“铝热反应”,人们可利用该反应来焊接铁轨。该反应中,(2)写出氢氧化钡在水溶液中的电离方程式:
(3)写出金属钠与水反应的离子方程式:
(4)
 可在呼吸面具和潜水艇中作为氧气的来源,请写出
可在呼吸面具和潜水艇中作为氧气的来源,请写出 与
与 反应的化学方程式
反应的化学方程式(5)
 个
个 的物质的量是
的物质的量是(6)
 个
个 分子中共含有
分子中共含有
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】新型冠状病毒肺炎疫情在全球爆发,研究表明“84”消毒液可以有效地消灭病毒。已知某“84”消毒液部分标签如下图所示:
回答下列问题:
(1)计算该“84”消毒液主要成分的物质的量浓度为_______ mol·L (保留1位小数)。
(保留1位小数)。
(2)某同学参阅该“84”消毒液的配方,欲用NaClO固体配制230 mL 4.0 mol·L 的NaClO消毒液,需要用
的NaClO消毒液,需要用_______ (填仪器名称)称量NaClO固体的质量_______ g。
(3)在配制该“84”消毒液的过程中,除烧杯、胶头滴管等仪器外,还必需的玻璃仪器有玻璃棒、_______ 。
(4)加蒸馏水定容时不慎超过了刻度线,正确的处理方法是_______ 。
(5)下列操作可能使配制的溶液浓度偏高的是_______ (填字母)。
A.移液时,未洗涤烧杯内壁和玻璃棒
B.溶解后未经冷却就移液
C.移液时,有少量液体溅出
D.定容时,俯视刻度线
E.容量瓶用蒸馏水洗净后,没烘干就直接使用
净含量:500 mL 密度:1.19 g/cm 主要成分:25% NaClO(质量分数) NaClO摩尔质量:74.5 g/mol 注意事项:密封保存,易吸收空气中的  变质 变质 |
(1)计算该“84”消毒液主要成分的物质的量浓度为
 (保留1位小数)。
(保留1位小数)。(2)某同学参阅该“84”消毒液的配方,欲用NaClO固体配制230 mL 4.0 mol·L
 的NaClO消毒液,需要用
的NaClO消毒液,需要用(3)在配制该“84”消毒液的过程中,除烧杯、胶头滴管等仪器外,还必需的玻璃仪器有玻璃棒、
(4)加蒸馏水定容时不慎超过了刻度线,正确的处理方法是
(5)下列操作可能使配制的溶液浓度偏高的是
A.移液时,未洗涤烧杯内壁和玻璃棒
B.溶解后未经冷却就移液
C.移液时,有少量液体溅出
D.定容时,俯视刻度线
E.容量瓶用蒸馏水洗净后,没烘干就直接使用
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】I.有下列物质:①Fe ②NH4Cl溶液③Na2O ④Cu(OH)2 ⑤熔融的MgCl2 ⑥H2SO4 ⑦CO2 ⑧C2H5OH(酒精)(用序号作答 )。其中属于电解质的有_____________ ,属于非电解质的有________________ 。
Ⅱ、某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+中的几种,请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是________ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子所发生的离子方程式为______________________________________ 。
(3)取(2)中的滤液,加入过量的NaOH出现白色沉淀,说明原溶液中肯定有的该离子所发生的离子方程式为___________________________ 。
(4)通过以上实验确定原溶液中一定含有的阳离子是_________ ,不能确定的阳离子是_________ 。
(5)原溶液可能大量存在的阴离子是下列的________ 。
A.Cl- B.NO C.CO
C.CO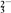 D.OH-
D.OH-
Ⅲ.现有M、N两种气态化合物,其摩尔质量之比为2:1,试回答下列问题:
(1)同温同压下,M、N气体的密度之比为____________ 。
(2)相同温度下,在两个相同体积的密闭容器中分别充入M、N,若两个容器中气体的密度相等,则两个容器中的压强之比为____________ 。
Ⅱ、某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+中的几种,请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子所发生的离子方程式为
(3)取(2)中的滤液,加入过量的NaOH出现白色沉淀,说明原溶液中肯定有的该离子所发生的离子方程式为
(4)通过以上实验确定原溶液中一定含有的阳离子是
(5)原溶液可能大量存在的阴离子是下列的
A.Cl- B.NO
 C.CO
C.CO D.OH-
D.OH-Ⅲ.现有M、N两种气态化合物,其摩尔质量之比为2:1,试回答下列问题:
(1)同温同压下,M、N气体的密度之比为
(2)相同温度下,在两个相同体积的密闭容器中分别充入M、N,若两个容器中气体的密度相等,则两个容器中的压强之比为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】教材中有两个关于混合物分离的实验,请回答下列有关问题
实验一:通过蒸馏的方法除去自来水中含有的氯离子等杂质制取纯净水,如图所示
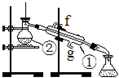
(1)写出下列仪器的名称:①___________ ②_____________
(2)若利用以上装置分离酒精和四氯化碳两种溶液的混合物,还缺少的仪器是______________ ,将仪器补充完整后进行的实验操作的名称是______________ ;①的进水口是__________ (填“f”或“g”)
(3)仪器②中常加入碎瓷片,这样做的目的是___________________
实验二:用CCl4从碘水中萃取I2并分液漏斗分离两种溶液.
其实验操作中有如下两步:
①将漏斗上口玻璃塞打开或使塞上的凹槽或小孔准漏斗的小孔.
②静置分层后,旋开活塞,用烧杯接收下层液体
(4)下层流出的是_____________ 溶液,上层液体从_________________ 得到(填“上口”或“下口”)
(5)萃取碘水中的I2单质时要用到萃取剂,下列关于所加萃取剂的说法正确的是( )
A.不与碘反应
B.碘在其中的溶解度大于在水中的溶解度
C.该萃取剂与水不互溶且密度不同
D.可以选用CCl4、 酒精做萃取剂.
实验一:通过蒸馏的方法除去自来水中含有的氯离子等杂质制取纯净水,如图所示

(1)写出下列仪器的名称:①
(2)若利用以上装置分离酒精和四氯化碳两种溶液的混合物,还缺少的仪器是
(3)仪器②中常加入碎瓷片,这样做的目的是
实验二:用CCl4从碘水中萃取I2并分液漏斗分离两种溶液.
其实验操作中有如下两步:
①将漏斗上口玻璃塞打开或使塞上的凹槽或小孔准漏斗的小孔.
②静置分层后,旋开活塞,用烧杯接收下层液体
(4)下层流出的是
(5)萃取碘水中的I2单质时要用到萃取剂,下列关于所加萃取剂的说法正确的是
A.不与碘反应
B.碘在其中的溶解度大于在水中的溶解度
C.该萃取剂与水不互溶且密度不同
D.可以选用CCl4、 酒精做萃取剂.
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】下列有关实验的叙述,正确的是(填序号)__________________
A.浓硫酸不小心沾到皮肤上,立即用稀NaOH溶液洗涤
B.用重结晶法提纯含少量NaCl的KNO3晶体
C.用分液漏斗将甘油和水的混合液体分离
D.为了测定某溶液的pH,将未经湿润的pH试纸浸入到待测溶液,过一会取出,与标准比色卡进行对比
E.配制银氨溶液时,将稀氨水慢慢滴加到硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止
A.浓硫酸不小心沾到皮肤上,立即用稀NaOH溶液洗涤
B.用重结晶法提纯含少量NaCl的KNO3晶体
C.用分液漏斗将甘油和水的混合液体分离
D.为了测定某溶液的pH,将未经湿润的pH试纸浸入到待测溶液,过一会取出,与标准比色卡进行对比
E.配制银氨溶液时,将稀氨水慢慢滴加到硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止
您最近半年使用:0次

 、
、 、
、 等杂质离子,可按如下步骤进行精制,完成各步内容:
等杂质离子,可按如下步骤进行精制,完成各步内容: ;⑤
;⑤ 、
、

