1840年盖斯根据一系列实验事实得出规律,他指出:“若是一个反应可以分步进行,则各步反应的反应热总和与这个反应一次发生时的反应热相同。”这是在各反应于相同条件下完成时的有关反应热的重要规律,称为盖斯定律。已知金刚石和石墨分别在氧气中完全燃烧的热化学方程式为:C(金刚石、s)+O2(g)=CO2(g);△H=-395.41kJ/mol,C(石墨、s)+O2(g)=CO2(g);△H=-393.51kJ/mol,则金刚石转化石墨时的热化学方程式为:_____________ 。由此看来更稳定的碳的同素异形体为:____________ 。
更新时间:2020-11-06 08:38:12
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】当反应物的总能量高于生成物时,该反应为______________ 反应;当反应物的总能量低于生成物时,该反应为______________ 反应(填“吸热或放热”),能量越高的物质越______________ (填“稳定或不稳定”)。
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】按要求完成下列问题。
(1)奥运会火炬常用的燃料为丙烷、丁烷等。已知:丙烷的燃烧热ΔH1=-2220kJ/mol,正丁烷的燃烧热△H2=-2878kJ/mol;异丁烷的燃烧热ΔH3=-2869.6kJ/mol。
①下列有关说法不正确的是___________ (填标号)。
A.奥运火炬燃烧时的能量转化形式主要是由化学能转化为热能、光能
B.异丁烷分子中的碳氢键比正丁烷的多
C.正丁烷比异丁烷稳定
②已知1molH2燃烧生成液态水放出的热量是285.8kJ,现有6mol由氢气和丙烷组成的混合气体,完全燃烧时放出的热量是3649kJ,则该混合气体中氢气和丙烷的物质的量比为___________ 。
(2)利用氢气可以制取工业原料乙酸。已知:
Ⅰ.CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH=-870.3kJ·mol-1
Ⅱ.C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
Ⅲ.H2(g)+ O2(g)=H2O(l) ΔH=-285.8kJ·mol-1
O2(g)=H2O(l) ΔH=-285.8kJ·mol-1
①相同质量的CH3COOH、C、H2完全燃烧时,放出热量最多的是___________ 。
②利用上述信息计算反应:2C(s)+2H2(g)+O2(g)=CH3COOH(l) ΔH=___________ 。
(1)奥运会火炬常用的燃料为丙烷、丁烷等。已知:丙烷的燃烧热ΔH1=-2220kJ/mol,正丁烷的燃烧热△H2=-2878kJ/mol;异丁烷的燃烧热ΔH3=-2869.6kJ/mol。
①下列有关说法不正确的是
A.奥运火炬燃烧时的能量转化形式主要是由化学能转化为热能、光能
B.异丁烷分子中的碳氢键比正丁烷的多
C.正丁烷比异丁烷稳定
②已知1molH2燃烧生成液态水放出的热量是285.8kJ,现有6mol由氢气和丙烷组成的混合气体,完全燃烧时放出的热量是3649kJ,则该混合气体中氢气和丙烷的物质的量比为
(2)利用氢气可以制取工业原料乙酸。已知:
Ⅰ.CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH=-870.3kJ·mol-1
Ⅱ.C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
Ⅲ.H2(g)+
 O2(g)=H2O(l) ΔH=-285.8kJ·mol-1
O2(g)=H2O(l) ΔH=-285.8kJ·mol-1①相同质量的CH3COOH、C、H2完全燃烧时,放出热量最多的是
②利用上述信息计算反应:2C(s)+2H2(g)+O2(g)=CH3COOH(l) ΔH=
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】回答问题:
(1)已知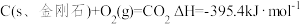 ,
,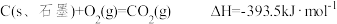 。
。
①石墨中 键键能
键键能___________ (填“大于”“小于”或“等于”)金刚石中 键键能。
键键能。
②由石墨转化为金刚石的热化学方程式为___________ 。
(2)将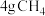 完全燃烧生成气态
完全燃烧生成气态 和液态水,放出热量
和液态水,放出热量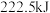 ,其热化学反应方程式为:
,其热化学反应方程式为:___________ 。
(3) 的气态高能燃料乙硼烷
的气态高能燃料乙硼烷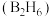 在氧气中燃烧,生成固态三氧化二硼和液态水,放出
在氧气中燃烧,生成固态三氧化二硼和液态水,放出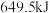 热量,其热化学反应方程式为:
热量,其热化学反应方程式为:___________ 。
(4)已知下列反应的反应热:
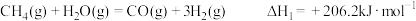
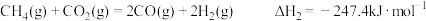
则 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为___________ 。
(1)已知
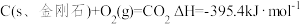 ,
,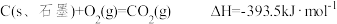 。
。①石墨中
 键键能
键键能 键键能。
键键能。②由石墨转化为金刚石的热化学方程式为
(2)将
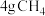 完全燃烧生成气态
完全燃烧生成气态 和液态水,放出热量
和液态水,放出热量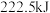 ,其热化学反应方程式为:
,其热化学反应方程式为:(3)
 的气态高能燃料乙硼烷
的气态高能燃料乙硼烷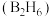 在氧气中燃烧,生成固态三氧化二硼和液态水,放出
在氧气中燃烧,生成固态三氧化二硼和液态水,放出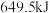 热量,其热化学反应方程式为:
热量,其热化学反应方程式为:(4)已知下列反应的反应热:
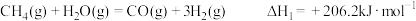
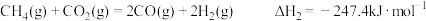
则
 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】红磷和Cl2发生反应生成PCl3或PCl5。反应过程和能量关系如右图所示(图中的 表示生成1mol产物的数据)。
表示生成1mol产物的数据)。

回答下列问题:
(1)1molPCl3所具有的总能量比1molP和1.5molCl2所具有的总能量___________ (填“高”或“低”)___________ kJ。
(2)PCl3和Cl2化合成PCl5的热化学方程式是___________ 。
(3)P和Cl2反应生成1molPCl5的 =
=___________ 。
(4)PCl5与足量水充分反应,最终生成两种酸,其化学方程式是___________ 。
(5)红磷的同素异形体白磷在氧气中燃烧有如下转化关系。
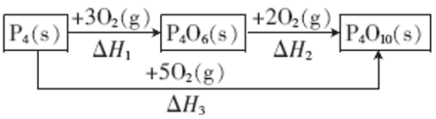
其中 =
=___________ (用含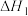 和
和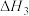 的代数式表示)。
的代数式表示)。
 表示生成1mol产物的数据)。
表示生成1mol产物的数据)。
回答下列问题:
(1)1molPCl3所具有的总能量比1molP和1.5molCl2所具有的总能量
(2)PCl3和Cl2化合成PCl5的热化学方程式是
(3)P和Cl2反应生成1molPCl5的
 =
=(4)PCl5与足量水充分反应,最终生成两种酸,其化学方程式是
(5)红磷的同素异形体白磷在氧气中燃烧有如下转化关系。

其中
 =
=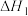 和
和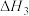 的代数式表示)。
的代数式表示)。
您最近半年使用:0次
【推荐2】2023年5月17日,西昌卫星发射中心成功发射第五十六颗北斗导航卫星,以后的中国将会在航天航空领域取得更优异成果!一种太空生命保障系统利用电解水供氧,生成的氢气与宇航员呼出的二氧化碳在催化剂作用下生成水和甲烷,水可循环使用。
(1)已知:
①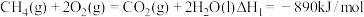
②
③
请写出 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为_____ 。
(2)科学家研发出一种新系统,将甲烷直接应用于燃料电池,以触发电化学反应,有效减少太空舱碳的排放,该电池采用 溶液为电解质,其工作原理如图所示:
溶液为电解质,其工作原理如图所示:
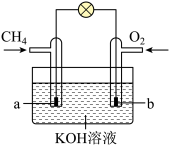
①外电路电子移动方向:_____ (填“a→b”或“b→a”)。
②a电极为_____ 极(填“正”“负”),a电极的电极方程式为_____ 。
(1)已知:
①
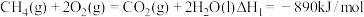
②

③

请写出
 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为(2)科学家研发出一种新系统,将甲烷直接应用于燃料电池,以触发电化学反应,有效减少太空舱碳的排放,该电池采用
 溶液为电解质,其工作原理如图所示:
溶液为电解质,其工作原理如图所示:
①外电路电子移动方向:
②a电极为
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐3】以太阳能为热源,热化学硫碘循环分解水是一种高效、环保的制氢方法,其流程图如图所示。

相关反应的热化学方程式为
反应Ⅰ:SO2(g)+I2(g)+2H2O(l)=2HI(aq)+H2SO4(aq)△H1=﹣213kJ•mol﹣1
反应Ⅱ:H2SO4(aq)=SO2(g)+H2O(l)+ O2(g)△H2=+327kJ•mol﹣1
O2(g)△H2=+327kJ•mol﹣1
反应Ⅲ:2HI(aq)=H2(g)+I2(g)△H3=+172kJ•mol﹣1
则反应2H2O(l)=2H2(g)+O2(g)△H=___________ 。

相关反应的热化学方程式为
反应Ⅰ:SO2(g)+I2(g)+2H2O(l)=2HI(aq)+H2SO4(aq)△H1=﹣213kJ•mol﹣1
反应Ⅱ:H2SO4(aq)=SO2(g)+H2O(l)+
 O2(g)△H2=+327kJ•mol﹣1
O2(g)△H2=+327kJ•mol﹣1反应Ⅲ:2HI(aq)=H2(g)+I2(g)△H3=+172kJ•mol﹣1
则反应2H2O(l)=2H2(g)+O2(g)△H=
您最近半年使用:0次



