汽车尾气中通常含有NO和CO等大气污染物,某课题组依据反应2CO(g)+2NO(g) N2(g)+2CO2(g) △H=-749 kJ·mol-1探究减少汽车尾气对大气的污染的方法,重点探究如何提高汽车尾气的转化速率。
N2(g)+2CO2(g) △H=-749 kJ·mol-1探究减少汽车尾气对大气的污染的方法,重点探究如何提高汽车尾气的转化速率。
(1)实验设计的部分数据如下表,按序号填写表格空白
(2)该课题组探究的是___________ 对反应速率的影响。
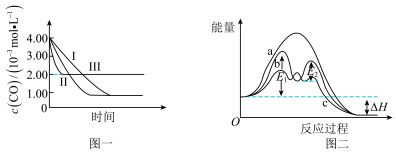
(3)三组实验c(CO)随时间变化如图一所示。通过图中___________ 两条曲线可知,催化效率较高的催化剂是___________ (填成分);第III组实验中,达平衡时c(NO)为___________ 。
(4)相同温度下,催化剂对反应过程中能量变化的影响对比如图二所示,其中与图一曲线II对应的曲线是___________ (填“a”、“b”或“c”)。
 N2(g)+2CO2(g) △H=-749 kJ·mol-1探究减少汽车尾气对大气的污染的方法,重点探究如何提高汽车尾气的转化速率。
N2(g)+2CO2(g) △H=-749 kJ·mol-1探究减少汽车尾气对大气的污染的方法,重点探究如何提高汽车尾气的转化速率。(1)实验设计的部分数据如下表,按序号填写表格空白
| 编号 | t/℃ | c(NO)/mol·L-1 | c(CO)/mol·L-1 | 催化剂 |
| Ⅰ | 280 | 5.50×10-3 | 4.00×10-3 | Cu—Co—Ce |
| Ⅱ | ① | ② | 4.00×10-3 | Pd—Pt—Rh |
| Ⅲ | 360 | 5.50×10-3 | ③ | Pd—Pt—Rh |
(3)三组实验c(CO)随时间变化如图一所示。通过图中
(4)相同温度下,催化剂对反应过程中能量变化的影响对比如图二所示,其中与图一曲线II对应的曲线是

更新时间:2020-11-11 15:29:32
|
相似题推荐
填空题
|
适中
(0.64)
【推荐1】在相同条件下进行Mg与HCl、H2SO4反应的对照实验,相关数据如下:
(1)试比较有关量的大小:v1____ v2,n1____ n2(填“>”、“=”或“<”)
(2)现欲改变条件,使实验Ⅱ中v2降低,但不改变n2的值,试写出两种可行的方法。
方法Ⅰ_____________________________________________ 。
方法Ⅱ_____________________________________________ 。
| Mg的质量 | 酸 量 | 开始时反应速率 | 产生H2总量 | |
| Ⅰ | 0.24 g | HCl 0.2 mol/L 100 mL | v1 | n1 |
| Ⅱ | 0.24 g | H2SO40.2 mol/L 100 mL | v2 | n2 |
(2)现欲改变条件,使实验Ⅱ中v2降低,但不改变n2的值,试写出两种可行的方法。
方法Ⅰ
方法Ⅱ
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】能源与材料、信息一起被称为现代社会发展的三大支柱。面对能源枯竭的危机,提高能源利用率和开辟新能源是解决这一问题的两个主要方向。
(1)化学反应速率和限度与生产、生活密切相关,这是化学学科关注的方面之一。某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水法收集反应放出的氢气,实验记录如下(累计值):
①哪一段时间内反应速率最大:__________ min(填“0~1”“1~2”“2~3”“3~4”或“4~5”)。
②另一学生为控制反应速率防止反应过快难以测量氢气体积。他事先在盐酸中加入等体积的下列溶液以减慢反应速率但不影响生成氢气的量。你认为不可行的是____________ (填字母序号)。
A 浓盐酸 B KCl溶液 C 蒸馏水 D CuSO4溶液
(2)寻找替代能源,是化学学科一直关注的另一方面。电能是一种二次能源,电能的应用大大丰富和方便了我们的生活、学习和工作。某化学兴趣小组探究铝电极在原电池中的作用,设计了一个Mg、Al、NaOH溶液电池,请写出
①原电池的负极电极反应:_________________________________ ;
②原电池的正极电极反应:___________________________________ ;
③原电池的总反应的离子方程式:___________________________________ 。
(1)化学反应速率和限度与生产、生活密切相关,这是化学学科关注的方面之一。某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水法收集反应放出的氢气,实验记录如下(累计值):
| 时间 | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL(标况) | 100 | 240 | 464 | 576 | 620 |
①哪一段时间内反应速率最大:
②另一学生为控制反应速率防止反应过快难以测量氢气体积。他事先在盐酸中加入等体积的下列溶液以减慢反应速率但不影响生成氢气的量。你认为不可行的是
A 浓盐酸 B KCl溶液 C 蒸馏水 D CuSO4溶液
(2)寻找替代能源,是化学学科一直关注的另一方面。电能是一种二次能源,电能的应用大大丰富和方便了我们的生活、学习和工作。某化学兴趣小组探究铝电极在原电池中的作用,设计了一个Mg、Al、NaOH溶液电池,请写出
①原电池的负极电极反应:
②原电池的正极电极反应:
③原电池的总反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.向体积为2 L的固定密闭容器中通入3 mol X气体,在一定温度下发生如下反应:2X(g) Y(g)+3Z(g)。经5 min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y表示的化学反应速率为
Y(g)+3Z(g)。经5 min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y表示的化学反应速率为____________ ,X的转化率为__________ ,Z的平衡浓度为_______________ 。
Ⅱ.一定温度下,反应N2(g)+O2(g) 2NO(g)在密闭容器中进行,回答下列措施对化学反应速率的影响(填“增大”“减小”或“不变”)。
2NO(g)在密闭容器中进行,回答下列措施对化学反应速率的影响(填“增大”“减小”或“不变”)。
(1)缩小体积使压强增大:__________ ;
(2)恒容充入N2:__________ ;
(3)恒容充入He:__________ ;
(4)恒压充入He:__________ 。
 Y(g)+3Z(g)。经5 min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y表示的化学反应速率为
Y(g)+3Z(g)。经5 min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y表示的化学反应速率为Ⅱ.一定温度下,反应N2(g)+O2(g)
 2NO(g)在密闭容器中进行,回答下列措施对化学反应速率的影响(填“增大”“减小”或“不变”)。
2NO(g)在密闭容器中进行,回答下列措施对化学反应速率的影响(填“增大”“减小”或“不变”)。(1)缩小体积使压强增大:
(2)恒容充入N2:
(3)恒容充入He:
(4)恒压充入He:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某温度时,在VL密闭容器中,A、B、C三种物质的物质的量随时间变化的曲线如图所示,由图中数据分析:

(1)反应的化学方程式为__________________ 。
(2)从开始到t1 min末时,用物质C表示的反应速率为____________________ 。

(1)反应的化学方程式为
(2)从开始到t1 min末时,用物质C表示的反应速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在容积不变的密闭容器中进行如下反应:A(g)+2B(g) 3C(g)+nD(g),开始时A的物质的量浓度为3mol/L,B的物质的量浓度为5mol/L;5min末测得C的物质的量浓度为3mol/L,用D表示的化学反应速率v(D)为0.2mol/L/min。
3C(g)+nD(g),开始时A的物质的量浓度为3mol/L,B的物质的量浓度为5mol/L;5min末测得C的物质的量浓度为3mol/L,用D表示的化学反应速率v(D)为0.2mol/L/min。
计算:(1)5min末A的物质的量浓度为___________ ,B的物质的量浓度为___________ 。
(2)前5min内用B表示的化学反应速率v(B)为___________ 。
(3)化学方程式中n的值为___________ 。
(4)此反应在四种不同情况下的反应速率最快的是___________ (填编号)
①v(A)=5mol·L-1·min-1②v(B)=6mol·L-1·min-1
③v(C)=7.5mol·L-1·min-1④v(D)=8mol·L-1·min-1
 3C(g)+nD(g),开始时A的物质的量浓度为3mol/L,B的物质的量浓度为5mol/L;5min末测得C的物质的量浓度为3mol/L,用D表示的化学反应速率v(D)为0.2mol/L/min。
3C(g)+nD(g),开始时A的物质的量浓度为3mol/L,B的物质的量浓度为5mol/L;5min末测得C的物质的量浓度为3mol/L,用D表示的化学反应速率v(D)为0.2mol/L/min。计算:(1)5min末A的物质的量浓度为
(2)前5min内用B表示的化学反应速率v(B)为
(3)化学方程式中n的值为
(4)此反应在四种不同情况下的反应速率最快的是
①v(A)=5mol·L-1·min-1②v(B)=6mol·L-1·min-1
③v(C)=7.5mol·L-1·min-1④v(D)=8mol·L-1·min-1
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】T ℃时,在容积为0.5 L的密闭容器中发生如下反应:mA(g)+nB(g)  pC(g)+qD(s) ΔH<0(m、n、p、q为最简整数比)。A、B、C、D的物质的量变化如图所示。
pC(g)+qD(s) ΔH<0(m、n、p、q为最简整数比)。A、B、C、D的物质的量变化如图所示。
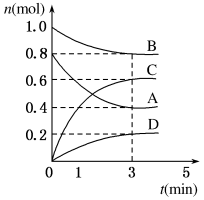
(1)前3 min,v(C)=______________ 。
(2)在该温度下K=___________ (填数值)
(3)反应达到平衡后,下列措施对A的转化率无影响的是________ (填选项字母)。
A.保持体积不变,再通入2 mol A和1 mol B B.移走一部分D C.把容器的体积缩小一倍 D.升高温度
(4)T ℃时,容积为1 L的密闭容器中,起始时充入0.2molA、0.4molB、0.3molC、0.5molD,此时v(正)_____ v(逆) (填“>”“<”或“=”) 。判断的依据是________ 。
 pC(g)+qD(s) ΔH<0(m、n、p、q为最简整数比)。A、B、C、D的物质的量变化如图所示。
pC(g)+qD(s) ΔH<0(m、n、p、q为最简整数比)。A、B、C、D的物质的量变化如图所示。
(1)前3 min,v(C)=
(2)在该温度下K=
(3)反应达到平衡后,下列措施对A的转化率无影响的是
A.保持体积不变,再通入2 mol A和1 mol B B.移走一部分D C.把容器的体积缩小一倍 D.升高温度
(4)T ℃时,容积为1 L的密闭容器中,起始时充入0.2molA、0.4molB、0.3molC、0.5molD,此时v(正)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】甲醇是最基本的有机化工原料之一。工业上可用二氧化碳和氢气反应来生产甲醇。
(1)已知气态甲醇的燃烧热为a kJ/mol,2H2(g)+O2(g) = 2H2O(g) ΔH= -b kJ/mol;H2O(g)=H2O(l) ΔH= -c kJ/mol。 则CO2(g)+3H2(g) CH3OH(g)+H2O(g)的ΔH=
CH3OH(g)+H2O(g)的ΔH=_________ 。
(2)某温度下,在2 L密闭容器中,充入2.4 mol CO2和4.4 mol H2,发生合成甲醇的反应,测得甲醇的物质的量随时间的变化图象如图中的曲线I,则前4分钟ν(CO2)=__________ ;若在1 min时,改变某一反应条件,曲线I变为曲线II,则改变的条件为___________ ;该温度下反应的化学平衡常数为___________ 。

(3)在另一温度下发生合成甲醇的反应,如图关闭K,向A容器中充入1 mol CO2和4 mol H2,向B容器中充入1.2 mol CO2和4.8 mol H2,两容器分别发生上述反应。已知起始时容器A和B的体积均为a L,反应达到平衡时容器B的体积为0.9a L,维持其他条件不变,若打开K一段时间后重新达到平衡,容器B的体积为______ L(不考虑温度的变化,P为可自由滑动活塞,不考虑活塞的摩擦力)。

(4)一定条件下甲醇可进一步氧化转化为甲酸。室温下,将a mol/L的甲酸与b mol/L的NaOH溶液等体积混合,体系中存在c(Na+)=c(HCOO-),试用含a和b的代数式表示甲酸的电离常数为_____________________ 。
(1)已知气态甲醇的燃烧热为a kJ/mol,2H2(g)+O2(g) = 2H2O(g) ΔH= -b kJ/mol;H2O(g)=H2O(l) ΔH= -c kJ/mol。 则CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)的ΔH=
CH3OH(g)+H2O(g)的ΔH=(2)某温度下,在2 L密闭容器中,充入2.4 mol CO2和4.4 mol H2,发生合成甲醇的反应,测得甲醇的物质的量随时间的变化图象如图中的曲线I,则前4分钟ν(CO2)=

(3)在另一温度下发生合成甲醇的反应,如图关闭K,向A容器中充入1 mol CO2和4 mol H2,向B容器中充入1.2 mol CO2和4.8 mol H2,两容器分别发生上述反应。已知起始时容器A和B的体积均为a L,反应达到平衡时容器B的体积为0.9a L,维持其他条件不变,若打开K一段时间后重新达到平衡,容器B的体积为

(4)一定条件下甲醇可进一步氧化转化为甲酸。室温下,将a mol/L的甲酸与b mol/L的NaOH溶液等体积混合,体系中存在c(Na+)=c(HCOO-),试用含a和b的代数式表示甲酸的电离常数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据表中所给数据分析催化剂对氨的合成反应速率的影响_____ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】我国提出争取在2030年前实现碳达峰、2060年前实现碳中和,这对于改善环境、实现绿色发展至关重要。其中二氧化碳技术是当前研究热点,下图就是利用催化剂 实现其转化的途径之一、
实现其转化的途径之一、

(1)催化剂 容易产生积碳而失活,实验显示,如果在一定温度下,向催化剂
容易产生积碳而失活,实验显示,如果在一定温度下,向催化剂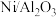 通入
通入 ,催化剂则会失活;失活后通入氢气,催化剂又会复活。请用化学方程式表示原因
,催化剂则会失活;失活后通入氢气,催化剂又会复活。请用化学方程式表示原因___________ 、___________ 。
(2) 的存在会使催化剂
的存在会使催化剂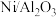 中毒,主要原因是
中毒,主要原因是 与金属结合,阻止了
与金属结合,阻止了___________ 与金属的结合,使主反应停止。
(3)上图总反应方程式为___________ ;转化时,还伴随着副反应,请依据上图判断副反应的有机产物之一是___________ 。为了实现总反应, 与载体结合,由此推断总反应温度
与载体结合,由此推断总反应温度___________ (填“较高”或“常温”)。
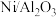 实现其转化的途径之一、
实现其转化的途径之一、
(1)催化剂
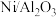 容易产生积碳而失活,实验显示,如果在一定温度下,向催化剂
容易产生积碳而失活,实验显示,如果在一定温度下,向催化剂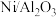 通入
通入 ,催化剂则会失活;失活后通入氢气,催化剂又会复活。请用化学方程式表示原因
,催化剂则会失活;失活后通入氢气,催化剂又会复活。请用化学方程式表示原因(2)
 的存在会使催化剂
的存在会使催化剂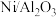 中毒,主要原因是
中毒,主要原因是 与金属结合,阻止了
与金属结合,阻止了(3)上图总反应方程式为
 与载体结合,由此推断总反应温度
与载体结合,由此推断总反应温度
您最近一年使用:0次



