有一包固体粉末,其中可能含有NaCl、Ba(NO3)2、K2SO4、Na2CO3、KNO3中的一种或几种,现做以下实验:
①取部分固体粉末加入水中,振荡,有白色沉淀生成;
②取①的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生;
试根据上述实验事实,回答下列问题:
(1)原固体粉末中一定含有的物质是_________ ,可能含有的物质是________ 。(写化学式)
(2)写出上述步骤中发生反应的离子方程式:①________ 。②________ 。
(3)若要判断可能含有的物质是否存在,则可取少量①中的上层清液分成两份,一份_____ ,另一份____ (补充实验步骤)
①取部分固体粉末加入水中,振荡,有白色沉淀生成;
②取①的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生;
试根据上述实验事实,回答下列问题:
(1)原固体粉末中一定含有的物质是
(2)写出上述步骤中发生反应的离子方程式:①
(3)若要判断可能含有的物质是否存在,则可取少量①中的上层清液分成两份,一份
更新时间:2020-11-11 09:46:11
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】由A和B两种可溶性盐组成的混合物,进行了下列实验:
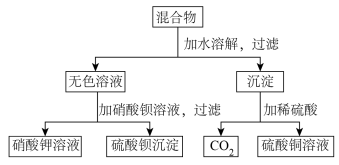
(1)若A溶液有颜色,试判断,A、B分别是_____________ 、_____________ 。(写化学式)
(2)写出实验过程中发生反应的离子方程式_____________ 、_____________ 、_____________ 。(顺序不限)

(1)若A溶液有颜色,试判断,A、B分别是
(2)写出实验过程中发生反应的离子方程式
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】实验室中某次产生的实验废液中可能含有大量Na+、Cu2+、 、
、 、Cl-、H+等。设计实验进行鉴别,步骤如下:
、Cl-、H+等。设计实验进行鉴别,步骤如下:
①加入足量NaOH溶液产生蓝色沉淀;
②向①反应后滤液中滴加足量Ba(OH)2溶液,有白色沉淀生成;
③过滤,然后向所得白色沉淀中加入过量稀硝酸,沉淀无变化。由此判断:
(1)该废液中确定存在的离子有___________ ,可能存在的离子为___________ 。。
(2)某兴趣小组要定性的鉴别可能存在的阴阳离子,对操作③后的溶液需要进行两步实验:
①鉴别阳离子的方法为___________ 。(写出操作、现象和结论,下同)
②鉴别阴离子的方法2为___________ 。
 、
、 、Cl-、H+等。设计实验进行鉴别,步骤如下:
、Cl-、H+等。设计实验进行鉴别,步骤如下:①加入足量NaOH溶液产生蓝色沉淀;
②向①反应后滤液中滴加足量Ba(OH)2溶液,有白色沉淀生成;
③过滤,然后向所得白色沉淀中加入过量稀硝酸,沉淀无变化。由此判断:
(1)该废液中确定存在的离子有
(2)某兴趣小组要定性的鉴别可能存在的阴阳离子,对操作③后的溶液需要进行两步实验:
①鉴别阳离子的方法为
②鉴别阴离子的方法2为
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】某实验小组探究酸和碱反应的本质(是什么微粒反应),设计了如下实验:
验I操作:Ba(OH)2:溶液 红色溶液
红色溶液 红色变浅到无色
红色变浅到无色 白色沉淀。
白色沉淀。
(1)实验I结论:___________ 。
实验II操作:盐酸溶液 [现象1]
[现象1] [现象2]
[现象2] [现象3]
[现象3] [现象4]。
[现象4]。
实验II结论:在盐酸中滴加Ba(OH)2溶液,盐酸中的H+参加了反应,而Cl-未参加反应。
(2)实验II分析:加入硝酸稀溶液的目的是___________ ,乙试剂为___________ 溶液。
(3)[现象3]对应的实验现象___________ 。
验I操作:Ba(OH)2:溶液
 红色溶液
红色溶液 红色变浅到无色
红色变浅到无色 白色沉淀。
白色沉淀。(1)实验I结论:
实验II操作:盐酸溶液
 [现象1]
[现象1] [现象2]
[现象2] [现象3]
[现象3]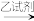 [现象4]。
[现象4]。实验II结论:在盐酸中滴加Ba(OH)2溶液,盐酸中的H+参加了反应,而Cl-未参加反应。
(2)实验II分析:加入硝酸稀溶液的目的是
(3)[现象3]对应的实验现象
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】草酸(乙二酸)存在于自然界的植物中,草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水。草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解。甲组同学按照如图所示的装置检验草酸晶体的分解产物。实验过程中,装置C、G中均出现浑浊。

回答下列问题:
(1)装置A试管口向上而不向下倾斜的原因是_______ 。
(2)装置B的主要作用是_______ 。若无装置B,则不能证明草酸晶体的分解产物中含有CO2,其原因是_______ 。
(3)装置D的主要作用是_______ 。为证明装置D的作用,可以在装置D和装置E之间,增加一个盛放_______ (填试剂名称)的洗气瓶。
(4)能证明草酸晶体分解产物中有CO的现象是_______ 。
(5)根据草酸晶体的性质和实验可知,草酸晶体分解的化学方程式为_______ 。

回答下列问题:
(1)装置A试管口向上而不向下倾斜的原因是
(2)装置B的主要作用是
(3)装置D的主要作用是
(4)能证明草酸晶体分解产物中有CO的现象是
(5)根据草酸晶体的性质和实验可知,草酸晶体分解的化学方程式为
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】请用化学方法鉴别苯、乙醇、乙酸、甲酸溶液和苯酚溶液。
(1)写出鉴别方法和使用化学试剂的先后顺序_______ 。
(2)写出有关反应的化学方程式_______ 。
(1)写出鉴别方法和使用化学试剂的先后顺序
(2)写出有关反应的化学方程式
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】在编号为A、B、C、D的四支试管中分别盛有NaHSO4、NaHCO3、BaCl2、BaCO3固体,在只有蒸馏水和若干试管的条件下,将它们一一鉴别出来,在你设计的实验方案中:
(1)已知NaHSO4溶于水发生电离:NaHSO4=Na++H++SO ,根据物质的溶解性不同,最先检验出来的固体是
,根据物质的溶解性不同,最先检验出来的固体是_______ ,随后枪验出的第二种物质是_______ ;
(2)后两种固体被检验出来时发生反应的离子方程式分别是___________ 、__________ 。
(1)已知NaHSO4溶于水发生电离:NaHSO4=Na++H++SO
 ,根据物质的溶解性不同,最先检验出来的固体是
,根据物质的溶解性不同,最先检验出来的固体是(2)后两种固体被检验出来时发生反应的离子方程式分别是
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】有一瓶溶液只含Cl-、CO32—、SO42—、Na+、NH4+、K+、Mg2+七种离子中的某几种。经实验:
①原溶液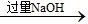 白色沉淀;
白色沉淀;
②将①所得溶液 放出使湿润的红色石蕊试纸变蓝的气体;
放出使湿润的红色石蕊试纸变蓝的气体;
③原溶液中加BaCl2溶液不产生沉淀。
④原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
回答下列问题:
(1)试分析原溶液中一定含有的离子是________________ ,一定不含有的离子是____________ ,可能含有的离子是________________ 。
(2)有同学认为实验④可以省略,你认为呢?(填“可以”或“不可以”)_________ ,并说明理由___________________________________________________________ 。
①原溶液
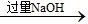 白色沉淀;
白色沉淀;②将①所得溶液
 放出使湿润的红色石蕊试纸变蓝的气体;
放出使湿润的红色石蕊试纸变蓝的气体;③原溶液中加BaCl2溶液不产生沉淀。
④原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
回答下列问题:
(1)试分析原溶液中一定含有的离子是
(2)有同学认为实验④可以省略,你认为呢?(填“可以”或“不可以”)
您最近半年使用:0次
【推荐2】I.某校化学兴趣小组同学猜想自来水中可能含有Cu2+、Ca2+、Mg2+和某些阴离子,进行了三组实验:
①取适量自来水于试管中,滴加足量的NaOH溶液,产生白色沉淀;
②过滤后取滤液于试管中,滴加足量的Na2CO3溶液,又有白色沉淀生成;
③另取适量自来水于试管中,滴加足量稀硝酸后再滴加AgNO3溶液,也产生白色沉淀。
(1)不用做实验就可排除的离子是___________ 。
(2)可初步确定自来水中___________ (填“含有”或“不含有”)Ca2+、Mg2+。
(3)自来水中所含阴离子可以确定有___________ (填离子符号),理由是(用离子方程式表示)___________ 。
II.二氧化氯(ClO2)泡腾片由NaClO2、固体酸及辅助剂混合制得,是一种用来消毒的家庭用品。使用时只需将泡腾片放入水中,5~10分钟即可完全溶解,释放出ClO2,其反应为: 5 +4H+=4ClO2+Cl-+2H2O 。(注:ClO2是一种易溶于水的气体。)
+4H+=4ClO2+Cl-+2H2O 。(注:ClO2是一种易溶于水的气体。)
(4)ClO2中Cl元素的化合价为___________ 。
(5)释放出ClO2的反应中实际上作为氧化剂与作为还原剂的个数比为______ 。
(6)用双线桥法表示释放出ClO2的反应(标出电子转移情况及数目、化合价变化、被氧化、被还原情况)______ 。
(7)二氧化氯泡腾片使用时需要加水,水的作用是___________ 。
①取适量自来水于试管中,滴加足量的NaOH溶液,产生白色沉淀;
②过滤后取滤液于试管中,滴加足量的Na2CO3溶液,又有白色沉淀生成;
③另取适量自来水于试管中,滴加足量稀硝酸后再滴加AgNO3溶液,也产生白色沉淀。
(1)不用做实验就可排除的离子是
(2)可初步确定自来水中
(3)自来水中所含阴离子可以确定有
II.二氧化氯(ClO2)泡腾片由NaClO2、固体酸及辅助剂混合制得,是一种用来消毒的家庭用品。使用时只需将泡腾片放入水中,5~10分钟即可完全溶解,释放出ClO2,其反应为: 5
 +4H+=4ClO2+Cl-+2H2O 。(注:ClO2是一种易溶于水的气体。)
+4H+=4ClO2+Cl-+2H2O 。(注:ClO2是一种易溶于水的气体。)(4)ClO2中Cl元素的化合价为
(5)释放出ClO2的反应中实际上作为氧化剂与作为还原剂的个数比为
(6)用双线桥法表示释放出ClO2的反应(标出电子转移情况及数目、化合价变化、被氧化、被还原情况)
(7)二氧化氯泡腾片使用时需要加水,水的作用是
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】某白色粉末A在农业上用作杀菌剂,进行下列实验:
(1)白色粉末溶解在水中,得到蓝色溶液,分成等量的两份
(2)在其中一份蓝色溶液中加入适量的盐溶液B,恰好沉淀完全,过滤,得到白色沉淀和蓝色溶液;
(3)在另一份蓝色溶液中加入适量C溶液,恰好沉淀完全,过滤,得到蓝色沉淀和纯净的硝酸钾溶液。
根据实验现象推断:
A___________________ B___________________ C___________________
(4)NaCl溶液中含有少量的CaCl2,某学生用过量的Na2CO3使Ca2+离子转化为沉淀而除去,确认Na2CO3已过量的实验方法是:________________________________ 。
(1)白色粉末溶解在水中,得到蓝色溶液,分成等量的两份
(2)在其中一份蓝色溶液中加入适量的盐溶液B,恰好沉淀完全,过滤,得到白色沉淀和蓝色溶液;
(3)在另一份蓝色溶液中加入适量C溶液,恰好沉淀完全,过滤,得到蓝色沉淀和纯净的硝酸钾溶液。
根据实验现象推断:
A
(4)NaCl溶液中含有少量的CaCl2,某学生用过量的Na2CO3使Ca2+离子转化为沉淀而除去,确认Na2CO3已过量的实验方法是:
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】某溶液,只含以下离子中的若干种:K+、Cu2+、Ba2+、Cl-、NO 、SO
、SO ,现取三份100mL溶液分别进行如下实验:
,现取三份100mL溶液分别进行如下实验:
①第一份加入硝酸钡溶液无明显现象,再加入AgNO3溶液有沉淀产生
②第二份加足量NaOH溶液后,有蓝色沉淀产生
③第三份加足量Na2SO4溶液后,有白色沉淀产生,加盐酸,沉淀质量不变
根据以上实验,回答下列问题:
(1)溶液中不能确定是否存在的离子是___ ,一定存在的离子是___ 。
(2)溶液中不存在的离子是___ ,实验②发生反应的离子方程式为___ 。
(3)写出第三份溶液中生成白色沉淀的离子方程式:___ 。
 、SO
、SO ,现取三份100mL溶液分别进行如下实验:
,现取三份100mL溶液分别进行如下实验:①第一份加入硝酸钡溶液无明显现象,再加入AgNO3溶液有沉淀产生
②第二份加足量NaOH溶液后,有蓝色沉淀产生
③第三份加足量Na2SO4溶液后,有白色沉淀产生,加盐酸,沉淀质量不变
根据以上实验,回答下列问题:
(1)溶液中不能确定是否存在的离子是
(2)溶液中不存在的离子是
(3)写出第三份溶液中生成白色沉淀的离子方程式:
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】为了将混有硫酸钠、碳酸氢铵的氯化钠提纯,某同学设计实验流程如图:
NaCl、Na2SO4、NH4HCO3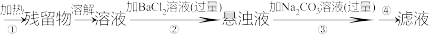

回答下列问题:
(1)操作①的目的是_______ 。操作②能否用硝酸钡溶液_______ 。(填“能”或“不能”)。
(2)进行操作②后,如何判断SO 已除尽,方法是
已除尽,方法是_______ 。
(3)操作③中发生反应的化学方程式为_______ 。操作④的名称是_______ 。
(4)此设计方案是否严密_______ (填“严密”或“不严密”),理由是_______ 。
(5)原固体样品中含NaClm1g,最后得到的NaCl固体m2g,则m1_______ m2(填“>”“<”或“=”)。
NaCl、Na2SO4、NH4HCO3
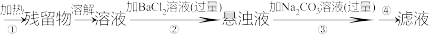

回答下列问题:
(1)操作①的目的是
(2)进行操作②后,如何判断SO
 已除尽,方法是
已除尽,方法是(3)操作③中发生反应的化学方程式为
(4)此设计方案是否严密
(5)原固体样品中含NaClm1g,最后得到的NaCl固体m2g,则m1
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】有一包白色固体粉末,其中可能含有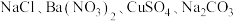 中的一种或几种,现做以下实验:
中的一种或几种,现做以下实验:
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤后溶液呈无色;
②向①的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生;
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生;
④另取①中过滤后的溶液,加入足量稀盐酸,有气泡产生;继续滴加足量 溶液产生白色沉淀。
溶液产生白色沉淀。
试根据上述实验事实,回答下列问题:
(1)原白色粉末中一定含有的物质是_______ ,一定不含的物质是_______ ,可能含有的物质是_______ 。(以上各种物质均写化学式)
(2)写出下列步骤中②发生反应的离子方程式:_______ 。
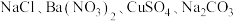 中的一种或几种,现做以下实验:
中的一种或几种,现做以下实验:①将部分粉末加入水中,振荡,有白色沉淀生成,过滤后溶液呈无色;
②向①的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生;
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生;
④另取①中过滤后的溶液,加入足量稀盐酸,有气泡产生;继续滴加足量
 溶液产生白色沉淀。
溶液产生白色沉淀。试根据上述实验事实,回答下列问题:
(1)原白色粉末中一定含有的物质是
(2)写出下列步骤中②发生反应的离子方程式:
您最近半年使用:0次



