某课外活动小组进行Fe(OH)3胶体的制备实验并检验其相关性质。
(1)若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是__ 。
A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液
(2)写出制备Fe(OH)3胶体的化学反应方程式:___ 。
(3)将制得的胶体放入半透膜制成的袋内,如图所示,放置2min后,取少量半透膜外的液体于试管中,置于暗处,用一束强光从侧面照射,观察__  填“有”或“无”
填“有”或“无”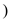 丁达尔现象,再向试管中加入用稀硝酸酸化的硝酸银溶液,可观察到的现象为
丁达尔现象,再向试管中加入用稀硝酸酸化的硝酸银溶液,可观察到的现象为___ 。
(1)若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是
A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液
(2)写出制备Fe(OH)3胶体的化学反应方程式:
(3)将制得的胶体放入半透膜制成的袋内,如图所示,放置2min后,取少量半透膜外的液体于试管中,置于暗处,用一束强光从侧面照射,观察
 填“有”或“无”
填“有”或“无” 丁达尔现象,再向试管中加入用稀硝酸酸化的硝酸银溶液,可观察到的现象为
丁达尔现象,再向试管中加入用稀硝酸酸化的硝酸银溶液,可观察到的现象为
更新时间:2020-11-13 08:32:22
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】某课外活动小组进行 胶体的制备实验并检验其相关性质。
胶体的制备实验并检验其相关性质。
(1)若将饱和 溶液分别滴入下列物质中,能形成胶体的是
溶液分别滴入下列物质中,能形成胶体的是___________ 。
A.冷水
B.沸水
C.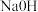 浓溶液D.
浓溶液D. 浓溶液
浓溶液
(2)写出制备 胶体的化学反应方程式
胶体的化学反应方程式___________ 。
(3)取少量制得的胶体加入试管中,再加入少量 溶液,观察到的现象是
溶液,观察到的现象是___________
(4) 胶体区别于
胶体区别于 溶液最本质的特征是___________。
溶液最本质的特征是___________。
(5)将制得的胶体放入半透膜制成的袋内,如图所示,放置 后,取少量半透膜外的液体于试管中,向试管中加入硝酸银溶液,再滴加稀硝酸,可观察到的现象为
后,取少量半透膜外的液体于试管中,向试管中加入硝酸银溶液,再滴加稀硝酸,可观察到的现象为___________ 。
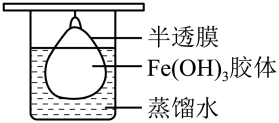
 胶体的制备实验并检验其相关性质。
胶体的制备实验并检验其相关性质。(1)若将饱和
 溶液分别滴入下列物质中,能形成胶体的是
溶液分别滴入下列物质中,能形成胶体的是A.冷水
B.沸水
C.
 浓溶液D.
浓溶液D. 浓溶液
浓溶液(2)写出制备
 胶体的化学反应方程式
胶体的化学反应方程式(3)取少量制得的胶体加入试管中,再加入少量
 溶液,观察到的现象是
溶液,观察到的现象是(4)
 胶体区别于
胶体区别于 溶液最本质的特征是___________。
溶液最本质的特征是___________。A. 胶体粒子的直径在 胶体粒子的直径在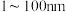 之间 之间 |
B. 胶体具有丁达尔效应 胶体具有丁达尔效应 |
C. 胶体是均一的分散系 胶体是均一的分散系 |
D. 胶体的分散质粒子能透过滤纸 胶体的分散质粒子能透过滤纸 |
 后,取少量半透膜外的液体于试管中,向试管中加入硝酸银溶液,再滴加稀硝酸,可观察到的现象为
后,取少量半透膜外的液体于试管中,向试管中加入硝酸银溶液,再滴加稀硝酸,可观察到的现象为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】某实验兴趣小组同学进行胶体的制备及性质实验,回答下列问题。
I、氢氧化铁胶体的制备和性质
(1)图中仪器a的名称为___________ 。
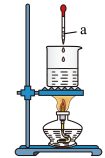
(2)①设计实验证明获得了氢氧化铁胶体___________ 。
②烧杯中发生反应的化学方程式为___________ 。
II、AgI是难溶于水的黄色沉淀,在一定条件下也可以形成胶体。兴趣小组设计如下实验探究某种条件对AgI胶体粒子所带电性的影响:
实验①:将稀AgNO3溶液逐滴加入过量的稀KI溶液中,得到AgI胶体I;
实验②:将稀KI溶液逐滴加入过量的稀AgNO3溶液中,得到AgI胶体II;
实验③:将提纯后的AgI胶体I与AgI胶体II进行混合,出现了黄色沉淀。
完成下列填空:
(3)写出制备AgI胶体I的离子方程式___________ 。
(4)提纯AI胶体的方法如图所示。
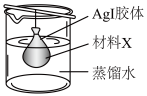
材料X为___________ 。用该法提纯AgI胶体II,进入蒸馏水中而被除去的离子有___________ (写离子符号,写三种)。
(5)本实验的探究结论是制备AgI胶体时反应物的用量对胶体粒子所带电性___________ (选填“有”或“无”)影响。简述作出此判断的理由___________ 。
I、氢氧化铁胶体的制备和性质
(1)图中仪器a的名称为

(2)①设计实验证明获得了氢氧化铁胶体
②烧杯中发生反应的化学方程式为
II、AgI是难溶于水的黄色沉淀,在一定条件下也可以形成胶体。兴趣小组设计如下实验探究某种条件对AgI胶体粒子所带电性的影响:
实验①:将稀AgNO3溶液逐滴加入过量的稀KI溶液中,得到AgI胶体I;
实验②:将稀KI溶液逐滴加入过量的稀AgNO3溶液中,得到AgI胶体II;
实验③:将提纯后的AgI胶体I与AgI胶体II进行混合,出现了黄色沉淀。
完成下列填空:
(3)写出制备AgI胶体I的离子方程式
(4)提纯AI胶体的方法如图所示。

材料X为
(5)本实验的探究结论是制备AgI胶体时反应物的用量对胶体粒子所带电性
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】完成下列填空:
(1)下列物质中:①稀硫酸②SO2③熔融NaOH④CH4⑤NH4Cl固体⑥Al。属于电解质的是___________ 。(填序号,下同)。属于非电解质的是___________ 。
(2)9.5g某二价金属氯化物(ACl2)中含有0.2molCl-,则A的摩尔质量是___________ 。
(3)在烧杯中加入20mL蒸馏水,加热至沸腾,向烧杯中逐滴加入几滴饱和FeCl3溶液,继续加热至呈红褐色后停止加热。证明有胶体生成的实验操作及现象是___________ 。
(4)湿法制备高铁酸钾( )是在碱性环境中进行,反应体系中有六种反应微粒:
)是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:___________ 。
(5)二氧化氯(ClO2)被联合国世界卫生组织列为A1级高效安全灭菌消毒剂。工业上可以利用硫铁矿【主要成分为二硫化亚铁(FeS2)】还原氯酸钠(NaClO3)制取二氧化氯。制备的离子方程式为: +FeS2+H+
+FeS2+H+ ClO2+Fe3++
ClO2+Fe3++ +H2O(未配平)。请配平以上反应方程式
+H2O(未配平)。请配平以上反应方程式___________ 。
(6)如图是某学校实验室从化学试剂商店采购的浓硫酸试剂标签上的部分内容。现用该浓硫酸配制240mL1.84mol/L的稀硫酸。可供选用的仪器有:胶头滴管;烧瓶;烧杯;药匙;量筒;托盘天平。
请回答下列问题:
①配制稀硫酸时,还缺少的仪器是___________ (填写名称)。
②经计算,配制240mL1.84mol·L-1的稀硫酸需要量取上述浓硫酸的体积为___________ mL。
③对所配制的稀硫酸进行测定,发现其浓度大于1.84mol·L-1,配制过程中下列各项操作可能引起该误差的有___________ (填写字母)。
A.用量筒量取浓硫酸时,俯视刻度线取浓硫酸
B.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水
C.将硫酸稀释后立即转入容量瓶后,紧接着就进行以后的实验操作
D.用量筒量取浓硫酸后,洗涤量筒并将洗涤液也转移入烧杯中
E.定容时,仰视容量瓶刻度线
F.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处
(1)下列物质中:①稀硫酸②SO2③熔融NaOH④CH4⑤NH4Cl固体⑥Al。属于电解质的是
(2)9.5g某二价金属氯化物(ACl2)中含有0.2molCl-,则A的摩尔质量是
(3)在烧杯中加入20mL蒸馏水,加热至沸腾,向烧杯中逐滴加入几滴饱和FeCl3溶液,继续加热至呈红褐色后停止加热。证明有胶体生成的实验操作及现象是
(4)湿法制备高铁酸钾(
 )是在碱性环境中进行,反应体系中有六种反应微粒:
)是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:(5)二氧化氯(ClO2)被联合国世界卫生组织列为A1级高效安全灭菌消毒剂。工业上可以利用硫铁矿【主要成分为二硫化亚铁(FeS2)】还原氯酸钠(NaClO3)制取二氧化氯。制备的离子方程式为:
 +FeS2+H+
+FeS2+H+ ClO2+Fe3++
ClO2+Fe3++ +H2O(未配平)。请配平以上反应方程式
+H2O(未配平)。请配平以上反应方程式(6)如图是某学校实验室从化学试剂商店采购的浓硫酸试剂标签上的部分内容。现用该浓硫酸配制240mL1.84mol/L的稀硫酸。可供选用的仪器有:胶头滴管;烧瓶;烧杯;药匙;量筒;托盘天平。
| 硫酸化学纯(CP)(500mL) 品名:硫酸 化学式:H2SO4 相对分子质量:98 密度:1.84g/cm3 质量分数:98% |
①配制稀硫酸时,还缺少的仪器是
②经计算,配制240mL1.84mol·L-1的稀硫酸需要量取上述浓硫酸的体积为
③对所配制的稀硫酸进行测定,发现其浓度大于1.84mol·L-1,配制过程中下列各项操作可能引起该误差的有
A.用量筒量取浓硫酸时,俯视刻度线取浓硫酸
B.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水
C.将硫酸稀释后立即转入容量瓶后,紧接着就进行以后的实验操作
D.用量筒量取浓硫酸后,洗涤量筒并将洗涤液也转移入烧杯中
E.定容时,仰视容量瓶刻度线
F.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】现有甲、乙、丙三名同学分别进行 胶体的制备实验。
胶体的制备实验。
①甲同学向 氯化铁溶液中加入少量的
氯化铁溶液中加入少量的 溶液;
溶液;
②乙同学直接加热饱和 溶液;
溶液;
③丙同学向 沸水中逐滴加入几滴
沸水中逐滴加入几滴 饱和溶液,继续煮沸至液体呈透明的红褐色,停止加热。
饱和溶液,继续煮沸至液体呈透明的红褐色,停止加热。
(1)其中操作正确的同学是_______ 。
(2)证明有 胶体生成的最简单的实验操作是
胶体生成的最简单的实验操作是_______ 。
(3)丁同学利用所制得的 胶体进行下列实验:
胶体进行下列实验:
①将其装入U形管内,用石墨作为电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明 胶粒带
胶粒带_______ 电荷。
②向其中加入饱和 溶液,产生的现象是
溶液,产生的现象是_______ 。
③向所得 胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为
胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为_______ ;继续滴加,沉淀最终消失且得棕黄色溶液,写出反应的化学方程式:_______ 。
④欲除去 胶体中混有的
胶体中混有的 ,该操作名称是
,该操作名称是_______ 。
 胶体的制备实验。
胶体的制备实验。①甲同学向
 氯化铁溶液中加入少量的
氯化铁溶液中加入少量的 溶液;
溶液;②乙同学直接加热饱和
 溶液;
溶液;③丙同学向
 沸水中逐滴加入几滴
沸水中逐滴加入几滴 饱和溶液,继续煮沸至液体呈透明的红褐色,停止加热。
饱和溶液,继续煮沸至液体呈透明的红褐色,停止加热。(1)其中操作正确的同学是
(2)证明有
 胶体生成的最简单的实验操作是
胶体生成的最简单的实验操作是(3)丁同学利用所制得的
 胶体进行下列实验:
胶体进行下列实验:①将其装入U形管内,用石墨作为电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明
 胶粒带
胶粒带②向其中加入饱和
 溶液,产生的现象是
溶液,产生的现象是③向所得
 胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为
胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为④欲除去
 胶体中混有的
胶体中混有的 ,该操作名称是
,该操作名称是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】将少量饱和 溶液分别滴加到下列物质中,得到三种分散系:
溶液分别滴加到下列物质中,得到三种分散系:

回答下列问题:
(1)将丙中溶液继续加热至液体呈透明的红褐色,发生反应的化学方程式为_______ 。
(2)判断丙中成功制备胶体的方法(写出相关的操作、现象和结论)是_______ 。
(3)向经过检验后的丙中逐滴加入稀盐酸,会出现一系列变化:
①先出现和乙中相同的现象,该过程称为_______ 。
②随后得到和甲相同的溶液,此反应的离子方程式为_______ 。
(4)向丙中插入电极通电,胶体粒子移向与电源_______ (填“正”或“负”,下同)极相连的一极,说明该胶体粒子带_______ 电荷。
(5)用如图所示的装置来提纯丙中制得的胶体,实验过程中需不断更换烧杯中的蒸馏水证明胶体中杂质离子已经完全除去的方法是_______ 。
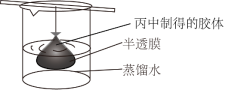
 溶液分别滴加到下列物质中,得到三种分散系:
溶液分别滴加到下列物质中,得到三种分散系:
回答下列问题:
(1)将丙中溶液继续加热至液体呈透明的红褐色,发生反应的化学方程式为
(2)判断丙中成功制备胶体的方法(写出相关的操作、现象和结论)是
(3)向经过检验后的丙中逐滴加入稀盐酸,会出现一系列变化:
①先出现和乙中相同的现象,该过程称为
②随后得到和甲相同的溶液,此反应的离子方程式为
(4)向丙中插入电极通电,胶体粒子移向与电源
(5)用如图所示的装置来提纯丙中制得的胶体,实验过程中需不断更换烧杯中的蒸馏水证明胶体中杂质离子已经完全除去的方法是

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
I、甲同学向1mol•L﹣1氯化铁溶液中加入少量的NaOH溶液;
II、乙同学直接加热饱和FeCl3溶液;
III、丙同学向25ml沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至溶液呈红褐色,停止加热。试回答下列问题:
(1)其中操作正确的同学是___ 。写出此过程中的化学方程式:___ ;
(2)证明有Fe(OH)3胶体生成的最简单实验操作是___ ;
(3)丁同学利用所制得的Fe(OH)3胶体进行下列实验:
①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明Fe(OH)3胶粒带__ 电荷。
②向其中加入饱和Na2SO4溶液,产生的现象是____ ;
③向所得Fe(OH)3胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为___ ;继续滴加,沉淀最终消失且得棕黄色溶液,写出化学方程式___ ;
I、甲同学向1mol•L﹣1氯化铁溶液中加入少量的NaOH溶液;
II、乙同学直接加热饱和FeCl3溶液;
III、丙同学向25ml沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至溶液呈红褐色,停止加热。试回答下列问题:
(1)其中操作正确的同学是
(2)证明有Fe(OH)3胶体生成的最简单实验操作是
(3)丁同学利用所制得的Fe(OH)3胶体进行下列实验:
①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明Fe(OH)3胶粒带
②向其中加入饱和Na2SO4溶液,产生的现象是
③向所得Fe(OH)3胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为
您最近一年使用:0次



