四只试剂瓶中分别装有NaNO3溶液、Na2CO3溶液、Na2SO4溶液和NaCl溶液,就如何检验这四种溶液分别解答下列各题。在四支试管中分别取四种溶液各1 mL,做下列实验。
(1)在四支试管中分别滴入________ ,出现气泡现象的是________ ,离子方程式是_________________ 。
(2)在剩余三支试管中分别滴入________ ,出现白色沉淀现象的是________ ,离子方程式是____________________________ 。
(3)在剩余两支试管中分别滴入________ ,出现白色沉淀现象的是________ ,离子方程式是_____________ 。三次实验中都没有明显现象的是______________ 。
(1)在四支试管中分别滴入
(2)在剩余三支试管中分别滴入
(3)在剩余两支试管中分别滴入
更新时间:2020-11-15 11:10:09
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】有一无色透明溶液,只可能含有以下离子中的若干种:K+、H+、Mg2+、Fe3+、Ba2+、SO 、CO
、CO 、NO
、NO ,现取两份各100mL溶液进行如下实验:
,现取两份各100mL溶液进行如下实验:
①第一份加足量NaHCO3溶液加热后,收集到气体0.05mol。
②第二份加足量Ba(NO3)2溶液充分反应后过滤干燥,得沉淀4.66g。
根据上述实验回答:
(1)溶液中一定不存在的离子是___ 。
(2)溶液中不能确定是否存在的离子是___ 。
(3)写出①发生反应的离子方程式___ 。
(4)写出②发生反应的离子方程式___ 。
 、CO
、CO 、NO
、NO ,现取两份各100mL溶液进行如下实验:
,现取两份各100mL溶液进行如下实验:①第一份加足量NaHCO3溶液加热后,收集到气体0.05mol。
②第二份加足量Ba(NO3)2溶液充分反应后过滤干燥,得沉淀4.66g。
根据上述实验回答:
(1)溶液中一定不存在的离子是
(2)溶液中不能确定是否存在的离子是
(3)写出①发生反应的离子方程式
(4)写出②发生反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】有一固体混合物A,已知其中可能含有MgCl2、CuSO4、CaCO3、FeCl3四种物质中的两种或多种。按如图所示进行实验,出现的现象如图中所述(假设过程中所有发生的反应都恰好完全进行)。
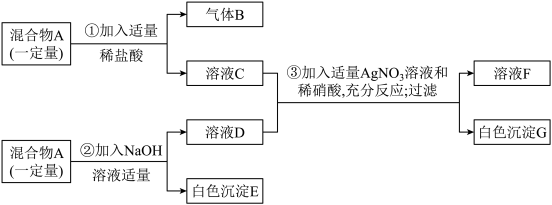
试根据实验过程和发生的现象做出判断,填写以下空白:
(1)气体B的化学式为______ 。
(2)在混合物A里,上述四物质中肯定不存在的物质是_____ (写化学式)。
(3)在溶液F中,主要含有___ 种溶质,其中大量含有的酸根离子符号是____ 。
(4)写出1个生成白色沉淀G的化学方程式:_____ 。

试根据实验过程和发生的现象做出判断,填写以下空白:
(1)气体B的化学式为
(2)在混合物A里,上述四物质中肯定不存在的物质是
(3)在溶液F中,主要含有
(4)写出1个生成白色沉淀G的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某白色粉末,可能含有硫酸钠、硫酸铜、氯化钠、硝酸钡、碳酸钙中的一种或几种。某科学兴趣小组为探究其成分,设计了如下实验流程(所加试剂均足量)。
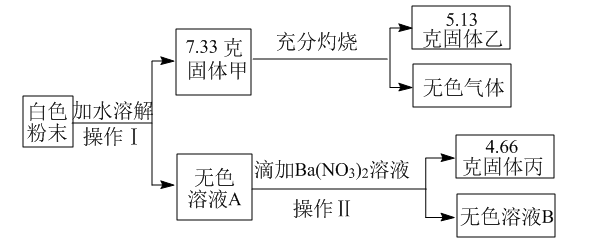
(1)操作I的名称是_____ 。
(2)生成无色气体的质量是___________ 克,所涉及的化学反应方程式_____
(3)固体甲的成分是___________ ,所涉及的离子反应方程式_____
(4)这种白色粉末中一定不含有___________ 。
(5)求白色粉末中肯定含有的物质总质量___________ 。

(1)操作I的名称是
(2)生成无色气体的质量是
(3)固体甲的成分是
(4)这种白色粉末中一定不含有
(5)求白色粉末中肯定含有的物质总质量
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】莫尔盐在500℃时隔绝空气加热完全分解,固体产物可能有FeO和Fe2O3,气体产物可能有NH3、SO3、H2O、N2和SO2,为检验分解产物的成分,设计如下实验装置进行实验。___________ 。
(2)为验证A中残留的铁的氧化物中是否含有FeO,需要选用的试剂有___________。
(3)装置B是为了检验分解产物是否有___________ 气体;装置C是为了检验分解产物是否有___________ 气体。
(4)若A中分解产物有N2,固体残留物只有Fe2O3,Fe2O3的物质的量为bmol,C中沉淀物质的量为amol,则b___________ a。
A.大于 B.小于 C.等于
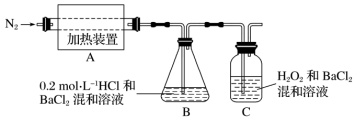
(2)为验证A中残留的铁的氧化物中是否含有FeO,需要选用的试剂有___________。
| A.KSCN溶液 | B.稀硫酸 | C.浓盐酸 | D.KMnO4溶液 |
(4)若A中分解产物有N2,固体残留物只有Fe2O3,Fe2O3的物质的量为bmol,C中沉淀物质的量为amol,则b
A.大于 B.小于 C.等于
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某学习小组设计实验探究CuSO4分解产物
Ⅰ.甲同学选择下列装置设计实验探究硫酸铜分解的气态产物SO3、SO2和O2,并验证SO2的还原性。
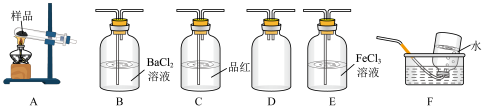
回答下列有关问题
(1)上述装置按气流从左至右排序为A、D、___________ E、F(填代号)。
(2)装置D的作用是______________________ ;能证明有SO3生成的实验现象是______________________ 。
(3)在实验过程中C装置中红色溶液逐渐变为无色溶液,说明A中分解产物有___________ ;待C中有明显现象后,F开始收集气体,F装置中集气瓶收集到了少量气体,该气体是___________ (填化学式)。
(4)为了验证SO2的还原性,取E装置中反应后的溶液于试管中,设计如下实验:
a.滴加少量的NH4SCN溶液 b.滴加少量的K3[Fe(CN)6]溶液
c.滴加酸性KMnO4溶液 d.滴加盐酸酸化的BaCl2溶液
其中,方案合理的有___________ (填代号),写出E装置中可能发生反应的离子方程式:________________ 。
Ⅱ.乙同学利用A中残留固体验证固体产物(假设硫酸铜已完全分解)查阅资料知,铜有+2、+1价,且分解产物中不含0价的铜。Cu2O在酸性条件下不稳定,发生反应:Cu2O+2H+=Cu+Cu2++H2O。
(5)为了验证固体产物中是否有Cu2O,设计了下列4种方案,其中能达到实验目的的是___________ 。
甲:取少量残留固体于试管,滴加足量的稀硝酸,观察溶液颜色是否变为蓝色
乙:取少量残留固体于试管,滴加足量的稀硫酸,观察溶液颜色是否变为蓝色
丙:取少量残留固体于试管,滴加足量的稀盐酸,观察是否有红色固体生成
丁:取少量残留固体于试管,通入氢气,加热,观察是否生成红色固体
(6)经检验CuSO4分解生成CuO、Cu2O、SO3、SO2和O2,且CuO、Cu2O的质量之比为5:9,SO2、O2、SO3的体积之比(同温同压下测定)为4:3:2。写出CuSO4分解的化学方程式:______________ 。
Ⅰ.甲同学选择下列装置设计实验探究硫酸铜分解的气态产物SO3、SO2和O2,并验证SO2的还原性。

回答下列有关问题
(1)上述装置按气流从左至右排序为A、D、
(2)装置D的作用是
(3)在实验过程中C装置中红色溶液逐渐变为无色溶液,说明A中分解产物有
(4)为了验证SO2的还原性,取E装置中反应后的溶液于试管中,设计如下实验:
a.滴加少量的NH4SCN溶液 b.滴加少量的K3[Fe(CN)6]溶液
c.滴加酸性KMnO4溶液 d.滴加盐酸酸化的BaCl2溶液
其中,方案合理的有
Ⅱ.乙同学利用A中残留固体验证固体产物(假设硫酸铜已完全分解)查阅资料知,铜有+2、+1价,且分解产物中不含0价的铜。Cu2O在酸性条件下不稳定,发生反应:Cu2O+2H+=Cu+Cu2++H2O。
(5)为了验证固体产物中是否有Cu2O,设计了下列4种方案,其中能达到实验目的的是
甲:取少量残留固体于试管,滴加足量的稀硝酸,观察溶液颜色是否变为蓝色
乙:取少量残留固体于试管,滴加足量的稀硫酸,观察溶液颜色是否变为蓝色
丙:取少量残留固体于试管,滴加足量的稀盐酸,观察是否有红色固体生成
丁:取少量残留固体于试管,通入氢气,加热,观察是否生成红色固体
(6)经检验CuSO4分解生成CuO、Cu2O、SO3、SO2和O2,且CuO、Cu2O的质量之比为5:9,SO2、O2、SO3的体积之比(同温同压下测定)为4:3:2。写出CuSO4分解的化学方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】硫化氢(H2S)是一种有毒的可燃性气体,用H2S、空气和KOH溶液可以组成燃料电池,其总反应式为2H2S+3O2+4KOH==2K2SO3+4H2O。
(1)该电池工作时正极应通入___________ 。
(2)该电池的负极电极反应式为:_________________ 。
(3)该电池工作时负极区溶液的pH________ (填“升高”“不变”“降低”)
(4)有人提出K2SO3可被氧化为K2SO4,因此上述电极反应式中的K2SO3应为K2SO4,某学习小组欲将电池工作一段时间后的电解质溶液取出检验,以确定电池工作时反应的产物。实验室有下列试剂供选用,请帮助该小组完成实验方案设计。
0.01mol·L-1KMnO4酸性溶液,1mol·L-1HNO3,1mol·L-1H2SO4,1mol·L-1HCl,0.1mol·L-1Ba(OH)2,0.1 mol·L-1BaCl2。
(5)若电池开始工作时每100mL电解质溶液含KOH 56g,取电池工作一段时间后的电解质溶液20.00mL,加入BaCl2溶液至沉淀完全,过滤洗涤沉淀,将沉沉在空气中充分加热至恒重,测得固体质量为11.65g,计算电池工作一段时间后溶液中KOH的物质的量浓度( ) 。
(结果保留四位有效数字,假设溶液体积保持不变,已知:M(KOH)=56,M(BaSO4)=233,M(BaSO3)=217)
(1)该电池工作时正极应通入
(2)该电池的负极电极反应式为:
(3)该电池工作时负极区溶液的pH
(4)有人提出K2SO3可被氧化为K2SO4,因此上述电极反应式中的K2SO3应为K2SO4,某学习小组欲将电池工作一段时间后的电解质溶液取出检验,以确定电池工作时反应的产物。实验室有下列试剂供选用,请帮助该小组完成实验方案设计。
0.01mol·L-1KMnO4酸性溶液,1mol·L-1HNO3,1mol·L-1H2SO4,1mol·L-1HCl,0.1mol·L-1Ba(OH)2,0.1 mol·L-1BaCl2。
| 实验步骤 | 实验现象及相关结论 |
| ①取少量电解质溶液于试管中,用pH试纸测其pH。 | 试纸呈深蓝色,经比对溶液的pH约为14,说明溶液中有残余的KOH。 |
| ②继续加入 | 若有白色沉淀产生,则溶液中含有K2SO4。 若无白色沉淀产生,则溶液中没有K2SO4 |
| ③另取少量电解质溶液于试管中,先加1 mol·L-1的H2SO4酸化,再滴入2~3滴0.01 mol·L-1KMnO4酸性溶液,振荡 |
(5)若电池开始工作时每100mL电解质溶液含KOH 56g,取电池工作一段时间后的电解质溶液20.00mL,加入BaCl2溶液至沉淀完全,过滤洗涤沉淀,将沉沉在空气中充分加热至恒重,测得固体质量为11.65g,计算电池工作一段时间后溶液中KOH的物质的量浓度
(结果保留四位有效数字,假设溶液体积保持不变,已知:M(KOH)=56,M(BaSO4)=233,M(BaSO3)=217)
您最近一年使用:0次



