为了探究 Fe2+、Cu2+、Ag+的氧化性强弱,设计实验如图所示,充分反应后:
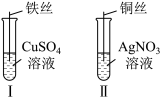
(1)Ⅰ中发生反应的离子方程式为_____ ;
(2)Ⅱ中铜丝上观察到的现象是_____ ;
(3)结合Ⅰ、Ⅱ实验现象可知 Fe2+ 、Cu2+ 、Ag+的氧化性由强到弱的顺序为_______ 。
(4)实验Ⅱ中的 AgNO3完全反应后,抽出铜丝,洗净后干燥,称重,发现铜丝比反应前增重 0.304g,则反应生成的Ag 的质量为_____ g。

(1)Ⅰ中发生反应的离子方程式为
(2)Ⅱ中铜丝上观察到的现象是
(3)结合Ⅰ、Ⅱ实验现象可知 Fe2+ 、Cu2+ 、Ag+的氧化性由强到弱的顺序为
(4)实验Ⅱ中的 AgNO3完全反应后,抽出铜丝,洗净后干燥,称重,发现铜丝比反应前增重 0.304g,则反应生成的Ag 的质量为
更新时间:2020-11-23 11:23:53
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】根据下图所示实验,回答问题:

(1)实验①观察到的现象是________________________ 。
(2)实验②观察到的现象是________________________ 。

(3)实验③观察到的现象是________________________ 。实验④观察到的现象是________________________ 。
(4)由上述实验,你能得出的结论是________________________ 。

(1)实验①观察到的现象是
(2)实验②观察到的现象是

(3)实验③观察到的现象是
(4)由上述实验,你能得出的结论是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】钛(Ti)是一种性能非常优越的金属,被称为继铝、铁之后的第三金属。某化学兴趣小组设计如下实验探究Mg、Ti、Cu的金属活动性顺序:同温下,取大小相同的这三种金属薄片,分别投入等体积、等物质的量浓度的足量稀盐酸中,实验现象如下表所示。
回答下列问题:
(1)三种金属加入盐酸前都先用砂纸将表面擦光亮,其目的是___________ (填序号)。
①除去氧化膜,利于直接反应
②使反应的金属温度相同
③使表面光亮,易观察现象
(2)写出镁与盐酸反应的离子方程式:___________ 。
(3)根据表中的实验现象可得出三种金属的活动性由强到弱的顺序为___________ ,判断的依据是___________ 。
(4)若将金属钛置于硫酸铜溶液中,可能的现象是___________ 。
| 金属 | Ti | Mg | Cu |
| 实验现象 | 产生气泡速度缓慢 | 产生气泡速度快 | 无明显现象 |
(1)三种金属加入盐酸前都先用砂纸将表面擦光亮,其目的是
①除去氧化膜,利于直接反应
②使反应的金属温度相同
③使表面光亮,易观察现象
(2)写出镁与盐酸反应的离子方程式:
(3)根据表中的实验现象可得出三种金属的活动性由强到弱的顺序为
(4)若将金属钛置于硫酸铜溶液中,可能的现象是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】Ⅰ: 元素的金属活动性递变规律是元素周期表学习的重要内容之一。某校研究性学习小组查阅课外资料,看到第IVA族的三种金属锗、锡、铅的性质:“锗、锡在空气中不反应,铅在空气中表面生成一层氧化铅,请解释发生上述变化的原因是___________________________________________________________ 。
Ⅱ: 另一研究性学习小组欲通过实验探究Zn、Fe、Cu的金属活动性顺序,根据不同的实验条件设计了如下的几种实验方案:
(1)该小组同学根据提供的Zn片、Fe片和稀硫酸,设计成了一个原电池比较锌与铁的活动性顺序,请在下侧方框内画出原电池装置图。并写出正极的反应现象及电极反应式。
现象_______________________________ ;电极反应式___________________________ ;装置图:________________________

(2)现只有Fe片、CuO和稀硫酸这几种药品,请你帮忙设计方案比较铁与铜的活动性顺序。你的设计方法是___________________________________________________________________________
Ⅱ: 另一研究性学习小组欲通过实验探究Zn、Fe、Cu的金属活动性顺序,根据不同的实验条件设计了如下的几种实验方案:
(1)该小组同学根据提供的Zn片、Fe片和稀硫酸,设计成了一个原电池比较锌与铁的活动性顺序,请在下侧方框内画出原电池装置图。并写出正极的反应现象及电极反应式。
现象

(2)现只有Fe片、CuO和稀硫酸这几种药品,请你帮忙设计方案比较铁与铜的活动性顺序。你的设计方法是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】Fe是应用最广泛的金属,被誉为“金属之王”。某兴趣小组对Fe、Fe2+及Fe3+的某些性质进行实验探究。
(一)A小组按如图所示操作进行实验,探究氧化剂的氧化性强弱。
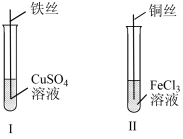
(1)Ⅰ中发生反应的离子方程式为___ 。
(2)Ⅱ中发生反应的化学方程式为___ 。
(3)结合实验Ⅰ、Ⅱ可知Fe2+,Cu2+,Fe3+的氧化性由强到弱的顺序为___ 。
(二)B小组研究Fe与水蒸气的反应,分别进行了如图实验。
请回答:
(4)实验Ⅰ中湿棉花的作用是____ 。
(5)实验Ⅰ中反应的化学方程式是___ 。
(6)若观察到实验Ⅰ中肥皂液持续产生肥皂泡,实验Ⅱ中溶液B呈现红色。说明溶液A中含有___ 。
(7)若观察到实验Ⅰ中肥皂液持续产生肥皂泡,但实验Ⅱ中溶液B未呈现红色。溶液B未呈现红色的原因是___ 。
(一)A小组按如图所示操作进行实验,探究氧化剂的氧化性强弱。

(1)Ⅰ中发生反应的离子方程式为
(2)Ⅱ中发生反应的化学方程式为
(3)结合实验Ⅰ、Ⅱ可知Fe2+,Cu2+,Fe3+的氧化性由强到弱的顺序为
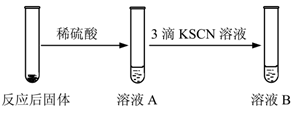
(二)B小组研究Fe与水蒸气的反应,分别进行了如图实验。
| 实验Ⅰ | 实验Ⅱ |
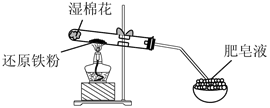 |  |
(4)实验Ⅰ中湿棉花的作用是
(5)实验Ⅰ中反应的化学方程式是
(6)若观察到实验Ⅰ中肥皂液持续产生肥皂泡,实验Ⅱ中溶液B呈现红色。说明溶液A中含有
(7)若观察到实验Ⅰ中肥皂液持续产生肥皂泡,但实验Ⅱ中溶液B未呈现红色。溶液B未呈现红色的原因是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空(a、b、c、d中重合部分代表物质间反应,且氯水足量)。

(1)能证明氯水具有漂白性的是________ (填“a”、“b”、“c”或“d”);
(2)c过程中的现象是_________________ ;d过程中的现象是__________________ ;e过程中的现象是___________________ ;b过程中的化学方程式为______________________ ;e过程的反应方程式____________________ ;
(3)久置的氯水变为______ ,用化学反应方程式表示为_______________ ;
(4)实验室保存饱和氯水的方法是_____________________ 。

(1)能证明氯水具有漂白性的是
(2)c过程中的现象是
(3)久置的氯水变为
(4)实验室保存饱和氯水的方法是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】小明同学想通过比较两种最高价氧化物水化物的酸性强弱来验证S与C的非金属性的强弱,他查阅了资料:可以利用强酸制备弱酸的原理来判断酸性强弱。于是小明采用了下图所示的装置进行实验。请回答:

(1)仪器A的名称是________ ,应盛放下列药品中的__________ 。
a.稀硫酸 b.亚硫酸 c.氢硫酸 d.盐酸
(2)仪器B的名称是________ ,应盛放下列药品中的__________ 。
a.碳酸钙 b.硫酸钠 c.氯化钠 d.碳酸钠
(3)仪器C中盛放的药品是澄清石灰水,如果看到的现象是澄清石灰水变浑浊,证明B中发生反应生成了_____________ ,即可说明___________ 比________ 酸性强,非金属性________ 比______ 强,B中发生反应的离子方程式为______________________________ 。

(1)仪器A的名称是
a.稀硫酸 b.亚硫酸 c.氢硫酸 d.盐酸
(2)仪器B的名称是
a.碳酸钙 b.硫酸钠 c.氯化钠 d.碳酸钠
(3)仪器C中盛放的药品是澄清石灰水,如果看到的现象是澄清石灰水变浑浊,证明B中发生反应生成了
您最近一年使用:0次



