现有甲、乙、丙三名同学分别进行 Fe(OH)3胶体的制备实验。甲同学:向 1mol·L-1的 FeCl3溶液中加少量NaOH 溶液。乙同学:直接加热饱和FeCl3溶液。丙同学:向 25 mL 沸水中逐滴加入 5~6 滴FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热。试回答下列问题:
(1)其中操作正确的同学是_____ 。
(2)证明有 Fe(OH)3胶体生成的实验操作是_____ ,利用的胶体性质是_____ 。
(3)已知在胶体中加入电解质溶液能使胶体粒子沉淀出来,丁同学向所制得的 Fe(OH)3胶体中加入稀硫酸,产生的现象是_____ 。
(1)其中操作正确的同学是
(2)证明有 Fe(OH)3胶体生成的实验操作是
(3)已知在胶体中加入电解质溶液能使胶体粒子沉淀出来,丁同学向所制得的 Fe(OH)3胶体中加入稀硫酸,产生的现象是
更新时间:2020-11-23 11:23:53
|
相似题推荐
解答题-工业流程题
|
容易
(0.94)
【推荐1】铝铁及其化合物是中学化学常见的物质。由制铝工业废渣(主要含Fe、Ca、Al等的氧化物)制取聚合硫酸铁铝净水剂的流程如下:
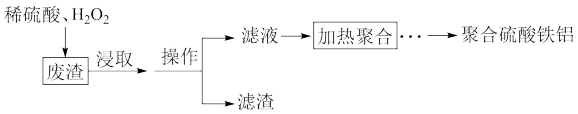
(1)写出“滤渣”的主要成分___________ (写化学式)。
(2)为了提高浸取率,可行的操作是_______ (写出其中一条),“操作”的名称是_______ 。
(3)写出铝的氧化物在“浸取”中发生的离子方程式_______ ,从氧化还原角度看, 在该操作中表现出
在该操作中表现出___________ 性。
(4)聚合硫酸铁铝溶于水形成 、
、 胶体具有
胶体具有______ 作用,达到净水的效果。

(1)写出“滤渣”的主要成分
(2)为了提高浸取率,可行的操作是
(3)写出铝的氧化物在“浸取”中发生的离子方程式
 在该操作中表现出
在该操作中表现出(4)聚合硫酸铁铝溶于水形成
 、
、 胶体具有
胶体具有
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
解题方法
【推荐2】分类是认识和研究物质及其变化的一种常用的科学方法。依据物质类别和元素价态可以对物质的性质进行解释和预测。以下为含氯物质的价类二维图,请回答下列问题:

(1)a物质的化学式为___________ ,b属于___________ (填“酸性”或“碱性”)氧化物。
(2)用Cl2O消毒水时,Cl2O还可将水中的Fe2+转化为Fe3+,Fe3+再水解生成Fe(OH)3胶体,说明Cl2O具有___________ 性。在此水处理过程中生成的Fe(OH)3胶体有___________ 作用。Fe(OH)3胶体与Fe(OH)3沉淀的本质区别是___________ 。
(3)工业上可以用反应2NaClO3+H2SO4+SO2=2ClO2+2NaHSO4制备Cl2O,用单线桥法标出电子转移的数目和方向___________ 。
(4)实验室制取氯气时,下列装置能达到相应实验目的是___________ 。
写出实验室用二氧化锰与浓盐酸反应制取氯气的化学方程式:___________ 。

(1)a物质的化学式为
(2)用Cl2O消毒水时,Cl2O还可将水中的Fe2+转化为Fe3+,Fe3+再水解生成Fe(OH)3胶体,说明Cl2O具有
(3)工业上可以用反应2NaClO3+H2SO4+SO2=2ClO2+2NaHSO4制备Cl2O,用单线桥法标出电子转移的数目和方向
(4)实验室制取氯气时,下列装置能达到相应实验目的是
 |  |  |  |
| A.制备Cl2 | B.除去Cl2中的HCl | C.收集Cl2 | D.尾气处理 |
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
【推荐3】某校学生在学习完胶体的知识后,利用化学兴趣社团活动时间,在实验室中用饱和FeCl3溶液制备Fe(OH)3胶体。具体操作是:取一支烧杯,加入适量的蒸馏水,加热至沸腾。将少量饱和FeCl3溶液分多次缓慢加入,继续加热至刚好变成红褐色,停止加热。
(1)该反应的化学方程式为_______ 。证明有氢氧化铁胶体生成的实验操作和现象是_______ 。
(2)甲同学在做实验时,由于使用了自来水,结果试管中形成了悬浊液,他制得的是_______ 。
(3)乙同学想Fe(OH)3胶体中可能含有FeCl3溶液,为了提纯Fe(OH)3胶体,他可以采用的方法是_______ 。
(4)丙同学将制好的Fe(OH)3胶体装入U型玻璃管中,插入电极,连通直流电,进行电泳实验。一段时间后,观察到阴极附近液体颜色加深,原因是Fe(OH)3胶体粒子带_______ (选填“正电荷”或“负电荷”)。
(5)丁同学取适量的Fe(OH)3胶体注入试管,然后用胶头滴管逐滴向试管中加入过量稀硫酸,看到的现象是_______ ,涉及的反应化学方程式_______ 。
(1)该反应的化学方程式为
(2)甲同学在做实验时,由于使用了自来水,结果试管中形成了悬浊液,他制得的是
(3)乙同学想Fe(OH)3胶体中可能含有FeCl3溶液,为了提纯Fe(OH)3胶体,他可以采用的方法是
(4)丙同学将制好的Fe(OH)3胶体装入U型玻璃管中,插入电极,连通直流电,进行电泳实验。一段时间后,观察到阴极附近液体颜色加深,原因是Fe(OH)3胶体粒子带
(5)丁同学取适量的Fe(OH)3胶体注入试管,然后用胶头滴管逐滴向试管中加入过量稀硫酸,看到的现象是
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
【推荐1】现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
Ⅰ、甲同学向氯化铁溶液中加入少量的NaOH溶液;
Ⅱ、乙同学向沸水中滴加饱和氯化铁溶液后,长时间加热;
Ⅲ、丙同学向25mL沸水中逐滴加入5~6滴FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热。
(1)其中操作正确的同学是_______ ;他的操作中涉及到的制备胶体的化学方程式为_______
(2)判断胶体制备是否成功,可利用胶体的_______ 。
(3)丁同学将所制得的Fe(OH) 3胶体进行下列实验:
向Fe(OH) 3胶体中逐滴加入了稀H2SO4溶液,结果出现了一系列变化。
a.先出现红褐色沉淀,原因是_______ 。
b.随后沉淀溶解,此反应的离子方程式是_______ 。
Ⅰ、甲同学向氯化铁溶液中加入少量的NaOH溶液;
Ⅱ、乙同学向沸水中滴加饱和氯化铁溶液后,长时间加热;
Ⅲ、丙同学向25mL沸水中逐滴加入5~6滴FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热。
(1)其中操作正确的同学是
(2)判断胶体制备是否成功,可利用胶体的
(3)丁同学将所制得的Fe(OH) 3胶体进行下列实验:
向Fe(OH) 3胶体中逐滴加入了稀H2SO4溶液,结果出现了一系列变化。
a.先出现红褐色沉淀,原因是
b.随后沉淀溶解,此反应的离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
【推荐2】将少量饱和 溶液分别滴加到下列物质中,得到三种分散系,完成相关问题:
溶液分别滴加到下列物质中,得到三种分散系,完成相关问题:
甲:饱和 溶液滴加到冷水中;
溶液滴加到冷水中;
乙:饱和 溶液滴加到NaOH溶液中;
溶液滴加到NaOH溶液中;
丙:饱和 溶液滴加到沸水中。
溶液滴加到沸水中。
(1)将丙继续加热煮沸得到红褐色透明液体,反应的化学方程式为___________ 。
(2)用最简单的方法判断丙中是否成功制备胶体,请写出相关的操作、现象和结论___________ 。
(3)向经过检验后的丙中逐滴加入稀盐酸,会出现一系列变化,但最终得到和甲相同的溶液,写出该过程发生反应的离子方程式:___________ 。
(4)在氯化铁溶液、氢氧化铁胶体、氢氧化铁悬浊液三种分散系中,分散质粒子直径最小的是___________ ,最大的是___________ ,氢氧化铁胶体分散质粒子直径大小介于___________ 之间。
 溶液分别滴加到下列物质中,得到三种分散系,完成相关问题:
溶液分别滴加到下列物质中,得到三种分散系,完成相关问题:甲:饱和
 溶液滴加到冷水中;
溶液滴加到冷水中;乙:饱和
 溶液滴加到NaOH溶液中;
溶液滴加到NaOH溶液中;丙:饱和
 溶液滴加到沸水中。
溶液滴加到沸水中。(1)将丙继续加热煮沸得到红褐色透明液体,反应的化学方程式为
(2)用最简单的方法判断丙中是否成功制备胶体,请写出相关的操作、现象和结论
(3)向经过检验后的丙中逐滴加入稀盐酸,会出现一系列变化,但最终得到和甲相同的溶液,写出该过程发生反应的离子方程式:
(4)在氯化铁溶液、氢氧化铁胶体、氢氧化铁悬浊液三种分散系中,分散质粒子直径最小的是
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
解题方法
【推荐3】某实验兴趣小组同学用如图所示装置制备氢氧化铁胶体(部分夹持装置已略去)。根据所学知识回答下列问题:
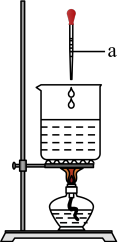
(1)仪器a的名称为_______ 。
(2)氢氧化铁胶体的制备方法:向沸水中逐滴加入5-6滴_______ ,继续煮沸至_______ 。
(3)Fe(OH)3中铁、氢、氧三种元素的质量比是:_______
(4)鉴别Fe(OH)3胶体和FeCl3溶液的具体操作是_______
(5)写出制备胶体的反应方程式:_______ 。

(1)仪器a的名称为
(2)氢氧化铁胶体的制备方法:向沸水中逐滴加入5-6滴
(3)Fe(OH)3中铁、氢、氧三种元素的质量比是:
(4)鉴别Fe(OH)3胶体和FeCl3溶液的具体操作是
(5)写出制备胶体的反应方程式:
您最近一年使用:0次
解答题-工业流程题
|
容易
(0.94)
名校
【推荐1】硫酸铁铵[aFe2(SO4)3·b(NH4)2SO4·cH2O]广泛用于城镇生活饮用水、工业循环水的净化等。某化工厂以硫酸亚铁(含少量硝酸钙)和硫酸铵为原料,设计如图工艺流程制取硫酸铁铵。
请回答下列问题:
(1)硫酸亚铁溶液加硫酸酸化的主要目的是________ 。
(2)下列物质中最适合的氧化剂B是________ 。
a.NaClO b.H2O2 c.KMnO4 d.K2Cr2O7
(3)操作甲的名称是_____ 。
(4)上述流程中,氧化之后和加热蒸发之前,需加入少量______ (填化学式),检验Fe2+是否已全部被氧化的方法为_______________ 。
(5)称取14.00 g所得产品,将其溶于水配制成100 mL溶液,分成两等份,向其中一份溶液中加入足量NaOH溶液,过滤、洗涤得到2.14 g沉淀;向另一份溶液中加入含0.05 mol Ba(NO3)2的溶液,恰好完全反应,则该硫酸铁铵的化学式为____ 。
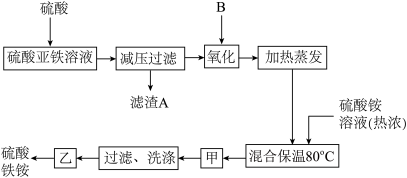
请回答下列问题:
(1)硫酸亚铁溶液加硫酸酸化的主要目的是
(2)下列物质中最适合的氧化剂B是
a.NaClO b.H2O2 c.KMnO4 d.K2Cr2O7
(3)操作甲的名称是
(4)上述流程中,氧化之后和加热蒸发之前,需加入少量
(5)称取14.00 g所得产品,将其溶于水配制成100 mL溶液,分成两等份,向其中一份溶液中加入足量NaOH溶液,过滤、洗涤得到2.14 g沉淀;向另一份溶液中加入含0.05 mol Ba(NO3)2的溶液,恰好完全反应,则该硫酸铁铵的化学式为
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
解题方法
【推荐2】用如图所示装置(夹持仪器省略)制备氢氧化亚铁。
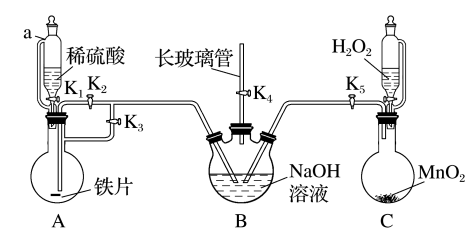
实验步骤如下:
Ⅰ.检查装置气密性后,关闭K2、K5,打开K1、K3、K4,使装置A中产生的气体进入装置B中,排尽B中空气。
Ⅱ.待B中空气排尽后,关闭K3,打开K2,将A中溶液压入B中并观察现象。
Ⅲ.关闭K1、K2,打开K5,使C中气体通入B中并观察现象。
回答下列问题:
(1)仪器a的名称是_______ ,B中长玻璃管的作用是_______ 。
(2)装置A中金属离子的检验方法是_______ 。
(3)步骤 Ⅲ 装置B中的现象是_______ ,其发生反应的化学方程式为_______ 。

实验步骤如下:
Ⅰ.检查装置气密性后,关闭K2、K5,打开K1、K3、K4,使装置A中产生的气体进入装置B中,排尽B中空气。
Ⅱ.待B中空气排尽后,关闭K3,打开K2,将A中溶液压入B中并观察现象。
Ⅲ.关闭K1、K2,打开K5,使C中气体通入B中并观察现象。
回答下列问题:
(1)仪器a的名称是
(2)装置A中金属离子的检验方法是
(3)步骤 Ⅲ 装置B中的现象是
您最近一年使用:0次




