已知某浓硫酸的标签如图:
现欲用该硫酸配制100ml1.0mo·L-1的硫酸溶液,具体操作如下:
①用量筒量取浓硫酸
②洗涤仪器2-3次,将洗涤液转入容量瓶中,摇匀
③将稀释、冷却后的硫酸转入100mL容量瓶中
④将浓硫酸倒入盛有水的烧杯中稀释、冷却
⑤加水至液面接近刻度线1~2cm处:定容,摇匀
完成下列填空:
(1)正确的操作顺序是___ (用序号填写)。
(2)本实验用到的基本仪器已有烧杯、量筒、玻璃棒,还缺少的仪器是___ 。
(3)第①步操作中应用量筒量取___ mL浓硫酸;应选择___ mL量筒(填5、10或50)。
(4)下列操作,会导致溶液浓度偏大的是___ 。
A.容量瓶洗涤过之后未干燥
B.洗涤量筒、烧杯和玻璃棒2~3次
C.定容时俯视容量瓶的刻度线
D.定容摇匀后发现凹液面低于刻度线,又补加蒸馏水至刻度线
| 浓硫酸(分析纯) 化学式:H2SO4相对分子适量:98 密度:1.84 g·cm-3质量分数:98% |
①用量筒量取浓硫酸
②洗涤仪器2-3次,将洗涤液转入容量瓶中,摇匀
③将稀释、冷却后的硫酸转入100mL容量瓶中
④将浓硫酸倒入盛有水的烧杯中稀释、冷却
⑤加水至液面接近刻度线1~2cm处:定容,摇匀
完成下列填空:
(1)正确的操作顺序是
(2)本实验用到的基本仪器已有烧杯、量筒、玻璃棒,还缺少的仪器是
(3)第①步操作中应用量筒量取
(4)下列操作,会导致溶液浓度偏大的是
A.容量瓶洗涤过之后未干燥
B.洗涤量筒、烧杯和玻璃棒2~3次
C.定容时俯视容量瓶的刻度线
D.定容摇匀后发现凹液面低于刻度线,又补加蒸馏水至刻度线
19-20高一·浙江·阶段练习 查看更多[1]
(已下线)【浙江新东方】在线化学 (8)
更新时间:2020-11-23 16:45:09
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】I.用固体烧碱配制480 mL 0.1 mol·L-1 NaOH溶液,请回答以下问题:
(1)需称量__________ g烧碱固体,它应盛在_________ 中进行称量。
(2)配制过程中,不需要使用的仪器是______________ (填字母)。
A 托盘天平 B 药匙 C 烧杯 D 胶头滴管 E 玻璃棒 F 1000 mL容量瓶 G 500 mL容量瓶
(3)若配制0.1 mol·L-1 NaOH溶液的其他操作均正确,但出现下列错误操作,其中将使配制的NaOH溶液浓度偏高的是__________ (填字母)。
A 将NaOH溶液转移至容量瓶后,未洗涤烧杯和玻璃棒
B 将烧杯内的NaOH溶液向容量瓶中转移时,因操作不当使部分溶液溅出瓶外
C 定容摇匀后,发现液面低于刻度线,又加水至液面与刻度线相切
D 定容时俯视容量瓶的刻度线
II.欲用98%的浓硫酸(ρ=1.84 g·mL-1 )配制成浓度为0.5 mol·L-1 的稀硫酸480 mL。
(4)所需浓硫酸的体积为_________ mL。
(5)下列操作正确的排列顺序为________ (填字母)。
A 用量筒量取浓硫酸 B 反复颠倒摇匀 C.用胶头滴管加水至刻度 D 将配制好的溶液转入试剂瓶中贴上标签 E 稀释浓硫酸 F 将溶液转入容量瓶 G 洗涤稀释装置
(1)需称量
(2)配制过程中,不需要使用的仪器是
A 托盘天平 B 药匙 C 烧杯 D 胶头滴管 E 玻璃棒 F 1000 mL容量瓶 G 500 mL容量瓶
(3)若配制0.1 mol·L-1 NaOH溶液的其他操作均正确,但出现下列错误操作,其中将使配制的NaOH溶液浓度偏高的是
A 将NaOH溶液转移至容量瓶后,未洗涤烧杯和玻璃棒
B 将烧杯内的NaOH溶液向容量瓶中转移时,因操作不当使部分溶液溅出瓶外
C 定容摇匀后,发现液面低于刻度线,又加水至液面与刻度线相切
D 定容时俯视容量瓶的刻度线
II.欲用98%的浓硫酸(ρ=1.84 g·mL-1 )配制成浓度为0.5 mol·L-1 的稀硫酸480 mL。
(4)所需浓硫酸的体积为
(5)下列操作正确的排列顺序为
A 用量筒量取浓硫酸 B 反复颠倒摇匀 C.用胶头滴管加水至刻度 D 将配制好的溶液转入试剂瓶中贴上标签 E 稀释浓硫酸 F 将溶液转入容量瓶 G 洗涤稀释装置
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】用胆矾(CuSO4•5H2O)配制480mL0.1mol•L-1的CuSO4溶液,需要用到下列仪器:烧杯、量筒、药匙、玻璃棒、托盘天平、胶头滴管等。
(1)配制时,还缺少的玻璃仪器是____ (填名称)。该实验中两次用到玻璃棒,其作用分别是____ 和____ 。
(2)下列操作对所配溶液的浓度大小有何影响(填“偏大”、“偏小”或“无影响”)。
①容量瓶未干燥,浓度会_____ 。
②定容后摇匀,发现液面低于刻度线,又加少量的水至到刻度线,浓度会____ 。
(3)配制该溶液时,可以选择用托盘天平称取固体CuSO4•5H2O的质量为____ g。
(1)配制时,还缺少的玻璃仪器是
(2)下列操作对所配溶液的浓度大小有何影响(填“偏大”、“偏小”或“无影响”)。
①容量瓶未干燥,浓度会
②定容后摇匀,发现液面低于刻度线,又加少量的水至到刻度线,浓度会
(3)配制该溶液时,可以选择用托盘天平称取固体CuSO4•5H2O的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】实验室现需用500mL、0.2mol/L的Na2SO4溶液,请填写下列空白:
A.在天平上称出硫酸钠固体,把它放在___ 里,用适量的蒸馏水使它完全溶解。
B.把A所得溶液小心地注入容量瓶中。
C.用少量蒸馏水洗涤烧杯和玻璃棒___ 次,每次洗涤的液体都小心注入容量瓶,并轻轻摇匀。
D.继续向容量瓶中加蒸馏水至液面距刻度___ cm处,改用___ ,小心滴加蒸馏水至溶液凹面底部与刻度线相切。
E.将容量瓶塞塞紧,充分摇匀。
①本实验用到的基本仪器已有烧杯、天平(砝码、镊子)、药匙、量筒,还缺少的仪器是:___ 、___ 、___ 。
②下列情况会使所配溶液浓度偏高或偏低或不影响
a.某同学定容时俯视液面( ) ;
b.洗涤液未转入容量瓶( ) ;
c.容量瓶用前内壁沾有水珠,未烘干( ) 。
A.在天平上称出硫酸钠固体,把它放在
B.把A所得溶液小心地注入容量瓶中。
C.用少量蒸馏水洗涤烧杯和玻璃棒
D.继续向容量瓶中加蒸馏水至液面距刻度
E.将容量瓶塞塞紧,充分摇匀。
①本实验用到的基本仪器已有烧杯、天平(砝码、镊子)、药匙、量筒,还缺少的仪器是:
②下列情况会使所配溶液浓度偏高或偏低或不影响
a.某同学定容时俯视液面
b.洗涤液未转入容量瓶
c.容量瓶用前内壁沾有水珠,未烘干
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验室用NaOH固体配制245 mL 1.2 mol/L的NaOH溶液,填空并请回答下列问题:
(1)配制245 mL 1.2 mol/L的NaOH溶液,需用托盘天平称取NaOH______ g,所需的玻璃仪器有量筒、烧杯、______________________________________ 。
(2)容量瓶上需标有以下五项中的_____________________ 。(填序号)
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(3)在定容操作时,应将蒸馏水注入容量瓶,液面离容量瓶颈刻度线______________ 处,改用____________ 滴加蒸馏水至与刻度线相平。盖好瓶塞,反复颠倒摇匀。
(4)本实验中,下列配制的溶液浓度偏低的是_____________ 。 (填字母代号)
A.称量NaOH时,使用游码,砝码错放在左盘
B.向容量瓶中转移溶液时,不慎有液滴洒在容量瓶外面
C.定容时仰视观察液面
D.溶解后未冷却到室温就将溶液转移到容量瓶中
E.配制前,容量瓶中有少量蒸馏水
(5)下列关于容量瓶的使用方法和操作的描述,正确的是___________ 。(填字母代号)
A.使用容量瓶前检查它是否漏水
B.引流时,玻璃棒的下端应在容量瓶刻度线以上
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,定容至刻度线
D.配制溶液时,若试样是液体,用量筒取试样后直接倒入容量瓶中,缓慢加水定容至刻度线
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀
(1)配制245 mL 1.2 mol/L的NaOH溶液,需用托盘天平称取NaOH
(2)容量瓶上需标有以下五项中的
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(3)在定容操作时,应将蒸馏水注入容量瓶,液面离容量瓶颈刻度线
(4)本实验中,下列配制的溶液浓度偏低的是
A.称量NaOH时,使用游码,砝码错放在左盘
B.向容量瓶中转移溶液时,不慎有液滴洒在容量瓶外面
C.定容时仰视观察液面
D.溶解后未冷却到室温就将溶液转移到容量瓶中
E.配制前,容量瓶中有少量蒸馏水
(5)下列关于容量瓶的使用方法和操作的描述,正确的是
A.使用容量瓶前检查它是否漏水
B.引流时,玻璃棒的下端应在容量瓶刻度线以上
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,定容至刻度线
D.配制溶液时,若试样是液体,用量筒取试样后直接倒入容量瓶中,缓慢加水定容至刻度线
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】在花瓶中加入“鲜花保鲜剂”可延长鲜花的寿命。下表是1 L“鲜花保鲜剂”的成分,阅读后回答下列问题:
(1)“鲜花保鲜剂”中物质的量浓度最大的成分是________ (填写名称)。
(2)“鲜花保鲜剂”中K+的物质的量浓度为(阿司匹林中不含K+)______ (只要求写表达式,不需计算)mol·L-1。
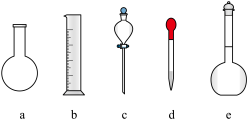
(3)下图所示的仪器中,在配制“鲜花保鲜剂”溶液时肯定不需要的是____________ (填字母),还缺少的玻璃仪器有____________ (填仪器名称)。
(4)配制过程中,下列操作使所配溶液浓度偏低的是____________ 。
A 容量瓶在使用前未干燥,里面有少量蒸馏水
B 溶解后没有冷却便进行定容
C 定容时仰视液面
D 容量瓶在使用前刚刚配制完一定物质的量浓度的鲜花保鲜剂而未洗净
E 加水定容时越过刻度线,又用胶头滴管吸出
F 定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(5)欲确定“鲜花保鲜剂”中硝酸银的浓度,则加入的试剂中应含有_________ (填化学符号)。
| 成分 | 质量/g | 摩尔质量/(g·mol-1) |
| 蔗糖 | 50.00 | 342 |
| 硫酸钾 | 0.50 | 174 |
| 阿司匹林 | 0.35 | 180 |
| 高锰酸钾 | 0.50 | 158 |
| 硝酸银 | 0.04 | 170 |
(2)“鲜花保鲜剂”中K+的物质的量浓度为(阿司匹林中不含K+)
(3)下图所示的仪器中,在配制“鲜花保鲜剂”溶液时肯定不需要的是

(4)配制过程中,下列操作使所配溶液浓度偏低的是
A 容量瓶在使用前未干燥,里面有少量蒸馏水
B 溶解后没有冷却便进行定容
C 定容时仰视液面
D 容量瓶在使用前刚刚配制完一定物质的量浓度的鲜花保鲜剂而未洗净
E 加水定容时越过刻度线,又用胶头滴管吸出
F 定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(5)欲确定“鲜花保鲜剂”中硝酸银的浓度,则加入的试剂中应含有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
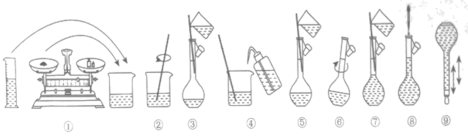
【推荐3】实验室中需0.5 mol/L  溶液950mL,下图为配制该溶液的示意图,请回答下列问题:
溶液950mL,下图为配制该溶液的示意图,请回答下列问题:
(1)下列关于容量瓶的使用中,错误的是___________ 。
A.使用容量瓶之前,检查其是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中定容
D.定容时,将蒸馏水小心倒入容量瓶中直至与刻度线齐平
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复上下颠倒,摇匀
(2)配制时用托盘天平称取 固体的质量是
固体的质量是___________ g。
(3)配制该溶液所需容量瓶规格为___________ 。
(4)上图②和③中玻璃棒的作用分别是___________ 、___________ 。
(5)若出现如下情况,对所配溶液浓度有何影响?(填“偏高”“偏低”或“无影响”)
A.步骤①称量的 失去部分结晶水:
失去部分结晶水:___________ ;
B.在步骤③中不慎有少量液体流到容量瓶外:___________ ;
C.没有进行步骤④和⑤:___________ ;
D.某同学在步骤⑧观察液面时仰视:___________ ;
E.溶解后溶液未冷却,立即进行移液:___________ 。
 溶液950mL,下图为配制该溶液的示意图,请回答下列问题:
溶液950mL,下图为配制该溶液的示意图,请回答下列问题:
(1)下列关于容量瓶的使用中,错误的是
A.使用容量瓶之前,检查其是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中定容
D.定容时,将蒸馏水小心倒入容量瓶中直至与刻度线齐平
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复上下颠倒,摇匀
(2)配制时用托盘天平称取
 固体的质量是
固体的质量是(3)配制该溶液所需容量瓶规格为
(4)上图②和③中玻璃棒的作用分别是
(5)若出现如下情况,对所配溶液浓度有何影响?(填“偏高”“偏低”或“无影响”)
A.步骤①称量的
 失去部分结晶水:
失去部分结晶水:B.在步骤③中不慎有少量液体流到容量瓶外:
C.没有进行步骤④和⑤:
D.某同学在步骤⑧观察液面时仰视:
E.溶解后溶液未冷却,立即进行移液:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验室需要0.1 mol·L−1NaOH溶液500 mL。
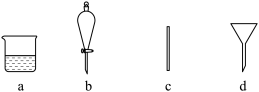
(1)在下图所示仪器中,配制上述溶液肯定不需要的是_________ (填序号),除图中已有仪器外,还需要的玻璃仪器是________ 。
(2)根据计算用托盘天平称取的NaOH固体质量为__________ g。
(3)关于容量瓶的四种叙述:
①是配制准确浓度溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水。这些叙述中正确的是______ (填字母)。
A.①②③④ B.②③ C.①②④ D.②③④
(4)容量瓶上需标有以下五项中的_________________ (填序号)。
(5)配制时,其正确的操作顺序是_________ (用字母表示,每个操作只用一次)。
A.用少量水洗涤烧杯2次~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1 cm~2 cm处
(6)下列配制的溶液浓度偏低的是____________ (填序号)。
A.称量NaOH时,砝码错放在左盘
B.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
C.加蒸馏水时不慎超过了刻度线
D.定容时俯视刻度线
E.配制前,容量瓶中有少量蒸馏水
(1)在下图所示仪器中,配制上述溶液肯定不需要的是

(2)根据计算用托盘天平称取的NaOH固体质量为
(3)关于容量瓶的四种叙述:
①是配制准确浓度溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水。这些叙述中正确的是
A.①②③④ B.②③ C.①②④ D.②③④
(4)容量瓶上需标有以下五项中的
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(5)配制时,其正确的操作顺序是
A.用少量水洗涤烧杯2次~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1 cm~2 cm处
(6)下列配制的溶液浓度偏低的是
A.称量NaOH时,砝码错放在左盘
B.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
C.加蒸馏水时不慎超过了刻度线
D.定容时俯视刻度线
E.配制前,容量瓶中有少量蒸馏水
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某实验需用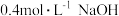 溶液
溶液 40mL。配制方法如下:
40mL。配制方法如下:
(1)配制该溶液应选用的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还必须的有___________ 。
(2)用托盘天平准确称量___________  固体
固体 。
。
(3)将称量好的 固体放在
固体放在 50mL大烧杯中,倒入约
50mL大烧杯中,倒入约 00mL蒸馏水,用玻璃棒搅拌,使固体全部溶解冷却后将烧杯中的溶液注入容量瓶中。用少量蒸馏水洗涤玻璃棒和烧杯内壁
00mL蒸馏水,用玻璃棒搅拌,使固体全部溶解冷却后将烧杯中的溶液注入容量瓶中。用少量蒸馏水洗涤玻璃棒和烧杯内壁 次,洗涤后的溶液
次,洗涤后的溶液___________ ,轻轻晃动容量瓶,使溶液混合均匀。
(4)向容量瓶中加入蒸馏水,到液面时 ,改用
,改用___________ 加蒸馏水至凹液面与刻度线相切。
(5)若在配制过程中出现下列情况,将使所配制的 溶液的浓度偏高的是
溶液的浓度偏高的是___________ ,偏低的是___________ ,对实验结果没有影响的是___________ (填各选项的序号)。
 定容摇匀后静止,发现液面低于刻度线,再加蒸馏水至刻度线
定容摇匀后静止,发现液面低于刻度线,再加蒸馏水至刻度线
 固体因长期保存部分潮解
固体因长期保存部分潮解
 配制溶液所用的容量瓶洗净后没有烘干
配制溶液所用的容量瓶洗净后没有烘干
 固体
固体 在烧杯中溶解后,立即将溶液转移到容量瓶内并接着进行后续操作
在烧杯中溶解后,立即将溶液转移到容量瓶内并接着进行后续操作
 转移溶液后,未洗涤烧杯和玻璃棒就直接定容
转移溶液后,未洗涤烧杯和玻璃棒就直接定容
 定容时,俯视观察液面
定容时,俯视观察液面
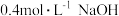 溶液
溶液 40mL。配制方法如下:
40mL。配制方法如下:(1)配制该溶液应选用的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还必须的有
(2)用托盘天平准确称量
 固体
固体 。
。(3)将称量好的
 固体放在
固体放在 50mL大烧杯中,倒入约
50mL大烧杯中,倒入约 00mL蒸馏水,用玻璃棒搅拌,使固体全部溶解冷却后将烧杯中的溶液注入容量瓶中。用少量蒸馏水洗涤玻璃棒和烧杯内壁
00mL蒸馏水,用玻璃棒搅拌,使固体全部溶解冷却后将烧杯中的溶液注入容量瓶中。用少量蒸馏水洗涤玻璃棒和烧杯内壁 次,洗涤后的溶液
次,洗涤后的溶液(4)向容量瓶中加入蒸馏水,到液面时
 ,改用
,改用(5)若在配制过程中出现下列情况,将使所配制的
 溶液的浓度偏高的是
溶液的浓度偏高的是 定容摇匀后静止,发现液面低于刻度线,再加蒸馏水至刻度线
定容摇匀后静止,发现液面低于刻度线,再加蒸馏水至刻度线 固体因长期保存部分潮解
固体因长期保存部分潮解 配制溶液所用的容量瓶洗净后没有烘干
配制溶液所用的容量瓶洗净后没有烘干 固体
固体 在烧杯中溶解后,立即将溶液转移到容量瓶内并接着进行后续操作
在烧杯中溶解后,立即将溶液转移到容量瓶内并接着进行后续操作 转移溶液后,未洗涤烧杯和玻璃棒就直接定容
转移溶液后,未洗涤烧杯和玻璃棒就直接定容 定容时,俯视观察液面
定容时,俯视观察液面
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】人体血液里Ca2+的浓度一般采用mg∙cm-3来表示。抽取一定体积的血样,将其中的Ca2+转化为草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸(如盐酸)可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中的浓度。
步骤1:配制KMnO4标准溶液。下图是配制100mL KMnO4标准溶液的过程。

(1)需用的仪器有天平、药匙、烧杯、玻璃棒、量筒、胶头滴管、___________ ,该仪器使用前必须进行的操作为___________ 。请你观察图示判断,其中不正确的操作有___________ (填序号)。
步骤2:测定血液样品中Ca2+的浓度。抽取血样20.00mL,经过上述处理后得到草酸,再用0.020mol∙L-1KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00mL KMnO4溶液。
已知:CaC2O4+2HCl=CaCl2+H2C2O4、2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。
(2)经过计算,血液样品中Ca2+的浓度为___________ mg∙cm-3。(写出计算过程)
(3)如果用图示的操作所配制的溶液进行实验,在其他操作正确的情况下,会导致血液样品中Ca2+的浓度___________ (填“偏大”“偏小”“无影响”)。
步骤1:配制KMnO4标准溶液。下图是配制100mL KMnO4标准溶液的过程。

(1)需用的仪器有天平、药匙、烧杯、玻璃棒、量筒、胶头滴管、
步骤2:测定血液样品中Ca2+的浓度。抽取血样20.00mL,经过上述处理后得到草酸,再用0.020mol∙L-1KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00mL KMnO4溶液。
已知:CaC2O4+2HCl=CaCl2+H2C2O4、2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。
(2)经过计算,血液样品中Ca2+的浓度为
(3)如果用图示的操作所配制的溶液进行实验,在其他操作正确的情况下,会导致血液样品中Ca2+的浓度
您最近一年使用:0次



