(I)现有下列八种物质:A.碳酸 B.铝 C.酒精 D.CO2 E.NH3·H2O F.BaSO4 G.氢氧化铁胶体 H.HNO3
上述物质中属于电解质的有_________ ;属于强电解质的有_________ ;既不是电解质又不是非电解质的有_________ 。(均填序号)
(II)向50ml沸水中加入5~6滴饱和FeCl3溶液,加热至产生红褐色液体,停止加热,得到氢氧化铁胶体。写出反应的化学方程式:___________ 。利用______________ 来鉴别溶液和胶体。
(III)写出下列反应的离子方程式
(1)在一定量的Ba(OH)2溶液中加入少量的NaHSO4溶液:____________________ 。
(2)在一定量的NaHCO3溶液中加入过量的稀H2SO4溶液:___________________ 。
上述物质中属于电解质的有
(II)向50ml沸水中加入5~6滴饱和FeCl3溶液,加热至产生红褐色液体,停止加热,得到氢氧化铁胶体。写出反应的化学方程式:
(III)写出下列反应的离子方程式
(1)在一定量的Ba(OH)2溶液中加入少量的NaHSO4溶液:
(2)在一定量的NaHCO3溶液中加入过量的稀H2SO4溶液:
更新时间:2020-12-09 14:16:52
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】铁及其化合物是中学实验室常用的试剂。
(1)利用氯化铁溶液制备氢氧化铁胶体。
①下列制备氢氧化铁胶体的操作方法正确的是___________ (填字母)。
A.向饱和氯化铁溶液中滴加适量的氢氧化钠溶液
B.在氨水中滴加氯化铁浓溶液
C.在沸水中滴加饱和氯化铁溶液,煮沸至溶液呈红褐色
②生成氢氧化铁胶体的离子方程式可表示为___________ 。
③区别氯化铁溶液和氢氧化铁胶体的方法是___________ 。
(2)绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的主要成分,也是中学化学一种常见的化学试剂。亚铁盐在空气中容易被氧化而变质。
①检验绿矾是否变质的实验操作是___________ 。
②甲同学取2mL稀硫酸酸化的FeSO4溶液,加入几滴H2O2溶液后,再加入1滴KSCN溶液,溶液变红,说明H2O2可将Fe2+氧化。FeSO4溶液与H2O2溶液反应的离子方程式为___________ 。
③乙同学认为甲同学的实验不够严谨,该同学在2mL用稀H2SO4酸化的FeSO4溶液中先加入0.5mL煤油,再于液面下依次加入几滴H2O2溶液和1滴KSCN溶液,溶液变红,煤油的作用是_______ 。
(1)利用氯化铁溶液制备氢氧化铁胶体。
①下列制备氢氧化铁胶体的操作方法正确的是
A.向饱和氯化铁溶液中滴加适量的氢氧化钠溶液
B.在氨水中滴加氯化铁浓溶液
C.在沸水中滴加饱和氯化铁溶液,煮沸至溶液呈红褐色
②生成氢氧化铁胶体的离子方程式可表示为
③区别氯化铁溶液和氢氧化铁胶体的方法是
(2)绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的主要成分,也是中学化学一种常见的化学试剂。亚铁盐在空气中容易被氧化而变质。
①检验绿矾是否变质的实验操作是
②甲同学取2mL稀硫酸酸化的FeSO4溶液,加入几滴H2O2溶液后,再加入1滴KSCN溶液,溶液变红,说明H2O2可将Fe2+氧化。FeSO4溶液与H2O2溶液反应的离子方程式为
③乙同学认为甲同学的实验不够严谨,该同学在2mL用稀H2SO4酸化的FeSO4溶液中先加入0.5mL煤油,再于液面下依次加入几滴H2O2溶液和1滴KSCN溶液,溶液变红,煤油的作用是
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】I.由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害,明胶是水溶性蛋白质混合物。
(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是________ 价,CrO 是一种酸根离子,则Fe(CrO2)2属于
是一种酸根离子,则Fe(CrO2)2属于_________ (填酸、碱、盐或氧化物)。
(2)明胶的水溶液和K2SO4溶液共同具备的性质是________ 。
A.都不稳定,密封放置会产生沉淀 B.二者均有丁达尔效应 C.分散质粒子可通过滤纸
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的_________ 。
A.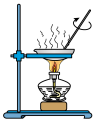 B.
B.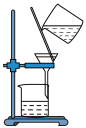 C.
C.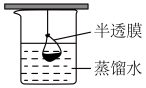
II.在实验室中用饱和FeCl3溶液制备Fe(OH)3胶体,具体操作是:取一支烧杯,加入适量的蒸馏水,加热至沸腾,将少量饱和FeCl3溶液分多次缓慢滴入,继续加热至刚好变成红褐色,停止加热。
(4)该反应的化学方程式为_________ 。
(5)某同学取适量Fe(OH)3胶体于试管,然后用胶头滴管逐滴向试管中加入稀硫酸,看到的现象是先产生红褐色沉淀,原因是:________ ,随着稀硫酸的不断滴加,沉淀又溶解,原因是:________ 。(用离子方程式表示)
(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是
 是一种酸根离子,则Fe(CrO2)2属于
是一种酸根离子,则Fe(CrO2)2属于(2)明胶的水溶液和K2SO4溶液共同具备的性质是
A.都不稳定,密封放置会产生沉淀 B.二者均有丁达尔效应 C.分散质粒子可通过滤纸
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的
A.
 B.
B. C.
C.
II.在实验室中用饱和FeCl3溶液制备Fe(OH)3胶体,具体操作是:取一支烧杯,加入适量的蒸馏水,加热至沸腾,将少量饱和FeCl3溶液分多次缓慢滴入,继续加热至刚好变成红褐色,停止加热。
(4)该反应的化学方程式为
(5)某同学取适量Fe(OH)3胶体于试管,然后用胶头滴管逐滴向试管中加入稀硫酸,看到的现象是先产生红褐色沉淀,原因是:
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】现有下列物质:①硫酸镁溶液② ③
③ ④乙醇⑤
④乙醇⑤ ⑥
⑥ ⑦稀醋酸⑧氧气
⑦稀醋酸⑧氧气
回答下列问题:
(1)上述物质中属于电解质的是______ (填标号),能导电的是______ (填标号)。
(2)与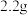 ③含有相同分子数的(8)标准状况下的体积为
③含有相同分子数的(8)标准状况下的体积为______ L。
(3)⑤在水溶液中的电离方程式为______ 。
(4)②加入①中发生反应的离子方程式为______ 。
 ③
③ ④乙醇⑤
④乙醇⑤ ⑥
⑥ ⑦稀醋酸⑧氧气
⑦稀醋酸⑧氧气回答下列问题:
(1)上述物质中属于电解质的是
(2)与
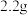 ③含有相同分子数的(8)标准状况下的体积为
③含有相同分子数的(8)标准状况下的体积为(3)⑤在水溶液中的电离方程式为
(4)②加入①中发生反应的离子方程式为
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】有以下物质:①铜②乙醇③氨水④二氧化硫⑤硫酸钡固体⑥氢氧化钠溶液⑦液氨⑧熔融氯化钠⑨稀硝酸⑩盐酸
(1)其中能导电的是___________ (填序号,下同);属于电解质的是___________ ;属于非电解质的是_____ 。
(2)写出⑥中NaOH的电离方程式:___________ 。
(3)选择上述物质写出二氧化硫是酸性氧化物的化学方程式___________ 。
(4)写出⑦与⑩发生反应的离子方程式___________ 。
(1)其中能导电的是
(2)写出⑥中NaOH的电离方程式:
(3)选择上述物质写出二氧化硫是酸性氧化物的化学方程式
(4)写出⑦与⑩发生反应的离子方程式
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】填空题
(1)现有以下物质:①Al2(SO4)3晶体,②稀盐酸 ,③冰醋酸(固态纯醋酸) ,④石墨, ⑤酒精(C2H5OH),⑥食盐水,⑦葡萄糖(C6H12O6),请回答下列问题:
Ⅰ.以上物质中属于电解质的是_______ (填序号,下同)。
Ⅱ.以上物质中属于非电解质的是_______ 。
Ⅲ.请写出①在水溶液中的电离方程式_______ 。
(2)配平化学方程式:_______ 。_______Cu + _______HNO3(稀)  _______Cu(NO3)2 + _______NO↑+_______H2O
_______Cu(NO3)2 + _______NO↑+_______H2O
(3)新生成的氢氧化亚铁在空气中会迅速变为灰绿色、最后变为红褐色,其过程中涉及到的化学方程式为:_______ 。
(1)现有以下物质:①Al2(SO4)3晶体,②稀盐酸 ,③冰醋酸(固态纯醋酸) ,④石墨, ⑤酒精(C2H5OH),⑥食盐水,⑦葡萄糖(C6H12O6),请回答下列问题:
Ⅰ.以上物质中属于电解质的是
Ⅱ.以上物质中属于非电解质的是
Ⅲ.请写出①在水溶液中的电离方程式
(2)配平化学方程式:
 _______Cu(NO3)2 + _______NO↑+_______H2O
_______Cu(NO3)2 + _______NO↑+_______H2O(3)新生成的氢氧化亚铁在空气中会迅速变为灰绿色、最后变为红褐色,其过程中涉及到的化学方程式为:
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】二氧化氯(ClO2)是国际上公认的高效消毒灭菌剂。一种制备ClO2的反应原理为5NaClO2+4HCl=4ClO2↑+5NaCl+2H2O。回答下列问题:
(1)按物质分类,上述反应中的各物质未涉及的类别是___________ (填序号)。
a.酸 b.碱 c.盐 d.氧化物
(2)将上述化学方程式改为离子方程式:___________ 。
(3)NaClO2的还原产物是___________ ;检验溶液中含有Cl-的常用试剂是___________ 。
(4)上述反应中,___________ (填“能”或“不能”)用稀硫酸代替盐酸,说明理由:___________ 。
(1)按物质分类,上述反应中的各物质未涉及的类别是
a.酸 b.碱 c.盐 d.氧化物
(2)将上述化学方程式改为离子方程式:
(3)NaClO2的还原产物是
(4)上述反应中,
您最近半年使用:0次
【推荐2】在Cu+HNO3 ———— Cu(NO3)2+NO↑+4H2O反应中,
(1)______ 元素被氧化, ______ 是氧化剂;
(2)______ 是氧化产物, ______ 发生氧化反应;
(3)被还原的HNO3与参加反应的HNO3物质的量之比是______ ;
(4)用双线桥标出该反应电子转移的方向和数目:
3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O_____________________________________ ;
(5)当有8mol HNO3被还原时,反应转移___________ 个电子;
(6)写出该反应的离子反应方程式___________________________ 。
(1)
(2)
(3)被还原的HNO3与参加反应的HNO3物质的量之比是
(4)用双线桥标出该反应电子转移的方向和数目:
3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
(5)当有8mol HNO3被还原时,反应转移
(6)写出该反应的离子反应方程式
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】生活离不开化学。家庭厨卫中有许多中学化学常见的物质,它们的主要成分如下表。
回答下列问题:
(1)以上主要成分中属于弱电解质的有___ (填序号)。NaCl中所含化学键类型为____________ 。
(2)当碱面不慎洒落在天然气火焰上,观察到的现象是_____________ 。
(3)KAl(SO4)2·12H2O的电离方程式为_______________ 。
(4)Na2CO3溶液中混有少量NaHCO3,可加适量的NaOH溶液除杂,离子反应方程式为________ ;
Na2CO3固体中若含有少量NaHCO3,可采取的除杂方法为___________ 。
(5)NaHCO3溶液与白醋反应的离子方程式为_________________ 。
(6)84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:_______________ 。
商品 | 食盐 | 碱面 | 84消毒液 | 发酵粉 |
主要成分 | ① NaCl | ② Na2CO3 | ③ NaClO | ④ NaHCO3 ⑤KAl(SO4)2·12H2O |
商品 | 料酒 | 白醋 | 洁厕灵 | \ |
主要成分 | ⑥C2H5OH | ⑦CH3COOH | ⑧HCl |
回答下列问题:
(1)以上主要成分中属于弱电解质的有
(2)当碱面不慎洒落在天然气火焰上,观察到的现象是
(3)KAl(SO4)2·12H2O的电离方程式为
(4)Na2CO3溶液中混有少量NaHCO3,可加适量的NaOH溶液除杂,离子反应方程式为
Na2CO3固体中若含有少量NaHCO3,可采取的除杂方法为
(5)NaHCO3溶液与白醋反应的离子方程式为
(6)84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:
您最近半年使用:0次



