氯元素是生产生活中常见的非金属元素。某同学探究Cl2及其化合物的性质。
(1)氯气能溶于水,氯气的水溶液称为氯水,写出Cl2与水反应的化学方程式___________ 。
(2)某同学把品红试纸(染有品红的纸)伸入氯水中,品红试纸褪色。
发现问题:氯水中的哪些成分使品红试纸褪色?
猜想:
猜想1:溶液中的H2O使品红试纸褪色;
猜想2:溶液中的___________ (填化学式)使品红褪色;
猜想3:盐酸使品红试纸褪色;
猜想4:溶液中的HClO使品红试纸褪色。
实验探究:
综合分析:氯水中的___________ (填化学式)使品红试纸褪色,具有漂白作用。
(3)向氯水中加入NaOH溶液,氯水浅黄绿色褪去。原因是(用相关化学方程式解释)___________ 。
(4)久置氯水最终变成了稀盐酸,原因是___________ 。
(1)氯气能溶于水,氯气的水溶液称为氯水,写出Cl2与水反应的化学方程式
(2)某同学把品红试纸(染有品红的纸)伸入氯水中,品红试纸褪色。
发现问题:氯水中的哪些成分使品红试纸褪色?
猜想:
猜想1:溶液中的H2O使品红试纸褪色;
猜想2:溶液中的
猜想3:盐酸使品红试纸褪色;
猜想4:溶液中的HClO使品红试纸褪色。
实验探究:
| 实验操作 | 实验现象 | 过程分析 |
| ①把品红试纸伸入水中 | 没有褪色 | 猜想1不成立 |
| ②把品红试纸伸入 | 没有褪色 | 猜想2不成立 |
| ③ | 没有褪色 | 猜想3不成立 |
(3)向氯水中加入NaOH溶液,氯水浅黄绿色褪去。原因是(用相关化学方程式解释)
(4)久置氯水最终变成了稀盐酸,原因是
更新时间:2020-12-09 15:47:07
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
【推荐1】氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空(a、b、c、d中重合部分代表物质间反应,且氯水足量)。

(1)能证明氯水具有漂白性的是________ (填“a”、“b”、“c”或“d”);
(2)c过程中的现象是_________________ ;d过程中的现象是__________________ ;e过程中的现象是___________________ ;b过程中的化学方程式为______________________ ;e过程的反应方程式____________________ ;
(3)久置的氯水变为______ ,用化学反应方程式表示为_______________ ;
(4)实验室保存饱和氯水的方法是_____________________ 。

(1)能证明氯水具有漂白性的是
(2)c过程中的现象是
(3)久置的氯水变为
(4)实验室保存饱和氯水的方法是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】为探究氯水中含有的部分粒子及某些粒子的性质,某化学兴趣小组做了如下实验:
(1)观察氯水颜色,发现氯水呈黄绿色,证明氯水中含有的粒子是________ 。
(2)向氯水中滴入碳酸钠溶液,有气体生成,说明氯水中含有的粒子是________ 。
(3)盛有氯水的试管中的有色布条褪色,说明氯水中含有的粒子是________ 。
(4)将紫色石蕊溶液滴入新制氯水中,溶液显红色。起作用的微粒是________ ,过一会儿,溶液的颜色褪去,起作用的微粒是________ 。
(5)向氯水中滴加硝酸银溶液有白色沉淀生成,证明氯水中含有的粒子是________ 。
(6)氯水经光照后,颜色逐渐消失,放出的气体是________ ,溶液的酸性________ (填“增强”“不变”或“减弱”)。
(7)将氯气通入水中,所得溶液中具有氧化性的含氯微粒是________ 。
(1)观察氯水颜色,发现氯水呈黄绿色,证明氯水中含有的粒子是
(2)向氯水中滴入碳酸钠溶液,有气体生成,说明氯水中含有的粒子是
(3)盛有氯水的试管中的有色布条褪色,说明氯水中含有的粒子是
(4)将紫色石蕊溶液滴入新制氯水中,溶液显红色。起作用的微粒是
(5)向氯水中滴加硝酸银溶液有白色沉淀生成,证明氯水中含有的粒子是
(6)氯水经光照后,颜色逐渐消失,放出的气体是
(7)将氯气通入水中,所得溶液中具有氧化性的含氯微粒是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】有X、Y、Z三种元素,他们的单质在常温常压下均为气体。
①X的单质可在Z的单质中燃烧生成XZ,其火焰为苍白色;
②化合物XZ的水溶液可使蓝色石蕊试纸变红;
③每2 mol X2可与1 mol Y2化合生成2 mol X2Y,X2Y在常温下为液体;
④Z的单质溶于化合物X2Y,所得溶液具有漂白作用。
回答下列问题:
(1)XZ:_______ ;X2Y:_______ 。(填化学式)
(2)写出Z单质与化合物X2Y反应的化学方程式:_______ 。
(3)写出Z单质与熟石灰反应的化学方程式:_______ 。
(4)氯水中含有多种粒子。将紫色石蕊溶液滴入氯水中,溶液显红色,起作用的粒子是_______ ;过一会儿,溶液的颜色逐渐褪去,起作用的粒子是_______ ;向氯水中滴入硝酸银溶液,产生白色沉淀,起作用的粒子是_______ 。
①X的单质可在Z的单质中燃烧生成XZ,其火焰为苍白色;
②化合物XZ的水溶液可使蓝色石蕊试纸变红;
③每2 mol X2可与1 mol Y2化合生成2 mol X2Y,X2Y在常温下为液体;
④Z的单质溶于化合物X2Y,所得溶液具有漂白作用。
回答下列问题:
(1)XZ:
(2)写出Z单质与化合物X2Y反应的化学方程式:
(3)写出Z单质与熟石灰反应的化学方程式:
(4)氯水中含有多种粒子。将紫色石蕊溶液滴入氯水中,溶液显红色,起作用的粒子是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】Ⅰ.为探究氯水中含有的部分粒子及某些粒子的性质,某化学兴趣小组做了如下实验:
(1)将紫色石蕊溶液滴入新制氯水中,溶液显红色,起作用的微粒是_______ ,过一会儿,溶液的颜色褪去,起作用的微粒是_______ 。
Ⅱ.某研究小组为了制备84消毒液(主要成分为 )设计了如图装置。并查阅到下列资料:“氯气与水的反应是放热反应,在加热条件下氯气与碱液发生如下反应:
)设计了如图装置。并查阅到下列资料:“氯气与水的反应是放热反应,在加热条件下氯气与碱液发生如下反应: ”。回答下列问题:
”。回答下列问题:
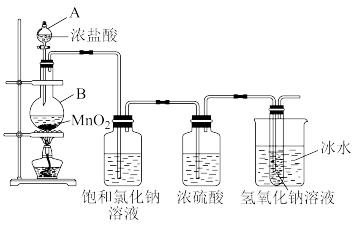
(2)上述加热条件下氯气与碱液发生的反应中氧化剂和还原剂的物质的量之比为_______ 。
(3)装置中仪器 的名称
的名称_______ ,装置中盛放饱和氯化钠溶液的作用_______ 。
(4)装置中能否省去盛冰水的烧杯?_______ ,理由是_______ 。
(5)写出仪器 中反应的离子方程式,并用单线桥法标出反应中电子转移的方向和数目
中反应的离子方程式,并用单线桥法标出反应中电子转移的方向和数目_______ 。
(1)将紫色石蕊溶液滴入新制氯水中,溶液显红色,起作用的微粒是
Ⅱ.某研究小组为了制备84消毒液(主要成分为
 )设计了如图装置。并查阅到下列资料:“氯气与水的反应是放热反应,在加热条件下氯气与碱液发生如下反应:
)设计了如图装置。并查阅到下列资料:“氯气与水的反应是放热反应,在加热条件下氯气与碱液发生如下反应: ”。回答下列问题:
”。回答下列问题:
(2)上述加热条件下氯气与碱液发生的反应中氧化剂和还原剂的物质的量之比为
(3)装置中仪器
 的名称
的名称(4)装置中能否省去盛冰水的烧杯?
(5)写出仪器
 中反应的离子方程式,并用单线桥法标出反应中电子转移的方向和数目
中反应的离子方程式,并用单线桥法标出反应中电子转移的方向和数目
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】在新制氯水中分别进行下列实验,写出相应的实验现象及反应的微粒。
(1)在氯水中加入镁条,现象为:________ ,反应微粒是:________ 。
(2)将氯水滴加到AgNO3溶液中,现象为:________ ,反应微粒是:________ 。
(3)将红布条放入氯水中,现象为:________ ,反应微粒是:________ 。
(4)氯水中滴加紫色石蕊试液,现象为:________ ,微粒是:________ 。
(5)将氯水滴加到FeCl2溶液中,现象为:________ ,微粒是:________ 。
(1)在氯水中加入镁条,现象为:
(2)将氯水滴加到AgNO3溶液中,现象为:
(3)将红布条放入氯水中,现象为:
(4)氯水中滴加紫色石蕊试液,现象为:
(5)将氯水滴加到FeCl2溶液中,现象为:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
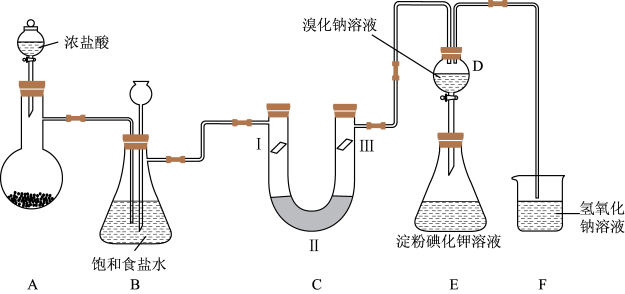
【推荐3】某校课外化学小组设计如下装置制备少量氯气并进行系列实验(夹持仪器已略)。
已知:卤素在水中的颜色如下表:
(1)若装置A中制备氯气,请写出装置A中的离反应方程式,_____________ ;
(2)装置B中的作用____________
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入____________
(4)设计装置D、B的目的是验证氧化性Cl2>Br2>I2。当向D中缓缓通入一定量氯气时,可以看到D中无色溶液逐渐变为_______ 色, 若打开D装置的活塞,使D中溶液滴入E装置, 可以观察到的现象是_________ ; 经认真考虑,有同学提出该实验方案仍有不足,你若同意该建议,请说明其中不足的原因是____ (若不同意, 则该空不用写)
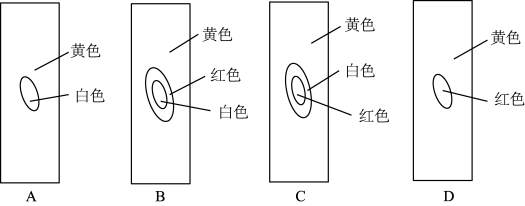
(5)实验后,用玻璃棒蘸取新制的氯水滴在pH试纸中部,观察到的现象是_____ (填选项)
(6)若0.lmolMnO2和25mL12 mol∙L−1盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为 .(不考虑盐酸的挥发)

已知:卤素在水中的颜色如下表:
Cl2 | Br2 | I2 | |
水溶液颜色 | 黄绿色 | 橙黄色 | 棕黄色 |
(2)装置B中的作用
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入
A | B | C | D | |
I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
II | 碱石灰 | 无水氯化钙 | 碱石灰 | 无水氯化钙 |
III | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(5)实验后,用玻璃棒蘸取新制的氯水滴在pH试纸中部,观察到的现象是

(6)若0.lmolMnO2和25mL12 mol∙L−1盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为 .(不考虑盐酸的挥发)
| A.等于0.15mol | B.小于0.15mol |
| C.大于0.15mol, 小于0.3mol | D.以上结论都不对 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】Ⅰ.如图所示装置可用于二氧化锰与浓盐酸在加热条件下制取氯气,并利用产物进行后续实验,请填写下列空白:

(1)写出二氧化锰与浓盐酸反应的化学方程式:____ 。
(2)在该反应中,HCl充当的是____ (填“氧化剂”或“还原剂”)。
(3)洗气瓶B中盛有饱和食盐水,洗气瓶C中盛有品红溶液,在洗气瓶D中盛有石灰乳,则洗气瓶C中观察到的现象是____ ;洗气瓶D中发生反应的化学方程式是____ 。
Ⅱ.氯水中含有多种成分,因而具有多重性质。根据氯水分别与如图四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量)。

(4)能证明氯水具有漂白性的是____ (填“a”“b”“c”或“d”)。
(5)c过程中的现象是____ 。
(6)b过程中的离子方程式为_____ 。

(1)写出二氧化锰与浓盐酸反应的化学方程式:
(2)在该反应中,HCl充当的是
(3)洗气瓶B中盛有饱和食盐水,洗气瓶C中盛有品红溶液,在洗气瓶D中盛有石灰乳,则洗气瓶C中观察到的现象是
Ⅱ.氯水中含有多种成分,因而具有多重性质。根据氯水分别与如图四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量)。

(4)能证明氯水具有漂白性的是
(5)c过程中的现象是
(6)b过程中的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】氯水中含有多种成分,因而具有多种性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量)。
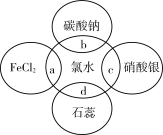
(1)c中证明氯水含有________ 粒子(用粒子符号表示)。
(2)d过程中的现象是____________________ ,
(3)b过程中反应的离子方程式___________________ 。
(4)a过程中反应的化学方程式为______________ 。

(1)c中证明氯水含有
(2)d过程中的现象是
(3)b过程中反应的离子方程式
(4)a过程中反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】某研究性学习小组欲探究氯气的化学性质,设计如图所示的实验装置。
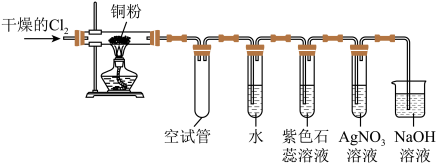
已知:该装置气密性良好;铜粉放在耐高温托盘内(防止硬质玻璃管炸裂)。
请回答下列问题:
(1)为防止铜与空气中的氧气反应,在加热之前应该进行的操作为____ 。
(2)当观察到AgNO3溶液中出现白色沉淀时,点燃酒精灯加热;写出AgNO3溶液中发生反应的化学方程式:____ 。
(3)硬质玻璃管中的反应现象为____ ,反应的化学方程式为____ 。
(4)装置中空试管的作用是____ 。
(5)实验中,观察到紫色石蕊溶液颜色的变化为____ 。
(6)烧杯中氢氧化钠溶液的作用是___ ,发生反应的化学方程式为_____ 。
(7)盛水的试管中,溶液最后的颜色为___ ,说明氯气____ (填“能”或“不能”)溶于水。

已知:该装置气密性良好;铜粉放在耐高温托盘内(防止硬质玻璃管炸裂)。
请回答下列问题:
(1)为防止铜与空气中的氧气反应,在加热之前应该进行的操作为
(2)当观察到AgNO3溶液中出现白色沉淀时,点燃酒精灯加热;写出AgNO3溶液中发生反应的化学方程式:
(3)硬质玻璃管中的反应现象为
(4)装置中空试管的作用是
(5)实验中,观察到紫色石蕊溶液颜色的变化为
(6)烧杯中氢氧化钠溶液的作用是
(7)盛水的试管中,溶液最后的颜色为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】回答下列问题:
(1)鉴别新制的氯水与久置的氯水_______________________________________________ 。
(2)次氯酸不稳定,见光易分解生成氯化氢和氧气。请设计实验证明有氧气生成________ 。
(1)鉴别新制的氯水与久置的氯水
(2)次氯酸不稳定,见光易分解生成氯化氢和氧气。请设计实验证明有氧气生成
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空(a、b、c、d中重合部分代表物质间反应,且氯水足量)。

(1)能证明氯水具有漂白性的是_______________ (填“a”、“b”、“c”或“d”);
(2)c过程中的现象是__________________________________________________________
(3)e过程中的现象是________________________________________________________ ;
(4)b过程中的化学方程式为__________________________________________________ ;
(5)久置的氯水变为________ ,用化学反应方程式表示为_____________________________ ;
(6)实验室保存饱和氯水的方法是_________________________________________ 。

(1)能证明氯水具有漂白性的是
(2)c过程中的现象是
(3)e过程中的现象是
(4)b过程中的化学方程式为
(5)久置的氯水变为
(6)实验室保存饱和氯水的方法是
您最近一年使用:0次



