焦亚硫酸钠(Na2S2O5)可用作食品加工的防腐剂,制备示意图如下。已知:2NaHSO3=Na2S2O5+H2O。下列说法不正确 的是
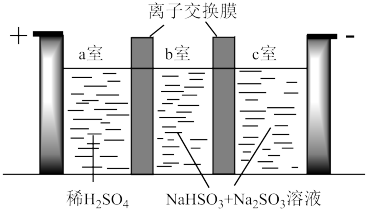

| A.采用的是阳离子交换膜 |
| B.阳极的电极反应式为2H2O-4e-= 4H+ + O2↑ |
| C.当阴极生成0.2 g气体时,a室溶液质量减少1.6 g |
| D.电解后将b室溶液进行结晶、脱水,可得到Na2S2O5 |
2020·浙江嘉兴·模拟预测 查看更多[6]
(已下线)选择题6-10(已下线)专题七 电化学中“离子交换膜”的应用(练习)四川省峨眉第二中学校2021-2022学年高二下学期5月月考化学试题(已下线)小题19 多池多室带膜电化学装置 ——备战2021年高考化学经典小题考前必刷(全国通用)广西梧州市2021届高三3月联考理科综合化学试题浙江省嘉兴市2021届高三12月教学测试化学试题
更新时间:2020-12-09 08:52:23
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】加碘食盐中含有碘酸钾(KIO3),现以电解法制备碘酸钾,实验装置如图所示。先将一定量的碘溶于过量氢氧化钾溶液,发生反应:3I2 +6KOH=5KI + KIO3+3H2O,将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区,开始电解。下列说法正确的是
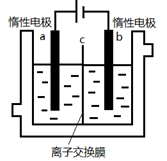
| A.b电极是负极 |
| B.装置中的离子交换膜是阳离子交换膜 |
| C.阳极电极反应:4OH--4e-═2H2O+O2↑ |
| D.a极区的KI最终转变为KIO3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.标准状况下,11.2L  和22.4L NO在密闭容器中充分混合后,气体分子总数小于 和22.4L NO在密闭容器中充分混合后,气体分子总数小于 |
B.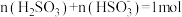 的 的 溶液中,含有 溶液中,含有 的数目等于 的数目等于 |
C.1L  的纯水中含有 的纯水中含有 的数目为 的数目为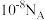 |
D.电解精炼铜时,若阳极质量减少64g,则阴极得到电子的数目为2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列有关电解的说法正确的是
| A.惰性电极电解硝酸银溶液不可能在电极上生成银,因为银可以溶于硝酸 |
| B.25℃,惰性电极电解氢氧化钠溶液,溶液pH不变,因为实质是电解水 |
| C.惰性电极电解足量硫酸铜溶液一段时间加入氧化铜固体可使电解质恢复到电解前 |
| D.惰性电极电解淀粉碘化钾溶液,可看到阴极区域溶液变蓝 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.电解 溶液,阴极增重 溶液,阴极增重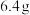 时,外电路中通过电子的数目为 时,外电路中通过电子的数目为 |
B. 浓硫酸与足量的 浓硫酸与足量的 共热,转移电子的数目为 共热,转移电子的数目为 |
C.标准状况下,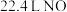 和 和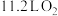 充分反应后产物分子的数目为 充分反应后产物分子的数目为 |
D. 中含 中含 键的数目一定为 键的数目一定为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定)。欲使溶液恢复到起始状态,可向溶液中加入( )
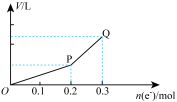

| A.0.1 mol CuO | B.0.1 mol CuCO3 |
| C.0.1 mol Cu(OH)2 | D.0.05 mol Cu2(OH)2CO3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】0.4mol CuSO4和0.4mol NaCl溶于水,配成1L溶液,用惰性电极进行电解,当—个电极得到0.3molCu时,另一个电极上生成的气体在标准状况下的体积是
| A.5.6L | B.6.72L |
| C.1.344L | D.11.2L |
您最近一年使用:0次
【推荐1】把两支惰性电极插入500mL硝酸银溶液中,通电电解,当电解液的pH从6.0变为3.0时(设电解时阴极没有氢气析出,且电解液在电解前后体积变化可以忽略),电极上应析出银的质量是
| A.27mg | B.54mg | C.108mg | D.216mg |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】电渗析法制取八钼酸铵[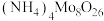 ]的工作原理如图所示(装置进出口未标明),已知当溶液的pH为2~4时,溶液中的Mo元素主要以
]的工作原理如图所示(装置进出口未标明),已知当溶液的pH为2~4时,溶液中的Mo元素主要以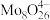 形态存在,下列说法不正确的是
形态存在,下列说法不正确的是

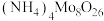 ]的工作原理如图所示(装置进出口未标明),已知当溶液的pH为2~4时,溶液中的Mo元素主要以
]的工作原理如图所示(装置进出口未标明),已知当溶液的pH为2~4时,溶液中的Mo元素主要以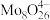 形态存在,下列说法不正确的是
形态存在,下列说法不正确的是
A.b极上的电极反应为: |
B.III室中发生反应: |
| C.电解完成后,可从II室中回收氨水 |
D.生成0.1mol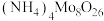 ,IV室溶液质量理论上增加21.6g ,IV室溶液质量理论上增加21.6g |
您最近一年使用:0次

 将
将 转化为
转化为 沉淀。图3为某含
沉淀。图3为某含 污水在氮磷联合脱除过程中溶液pH变化。
污水在氮磷联合脱除过程中溶液pH变化。
 氧化
氧化 的离子方程式为
的离子方程式为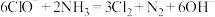



 等基本化工原料。已知相同时间内产生气体P、Q物质的量之比为2:1(BPM为双极膜,在直流电场的作用下,可作为
等基本化工原料。已知相同时间内产生气体P、Q物质的量之比为2:1(BPM为双极膜,在直流电场的作用下,可作为 和
和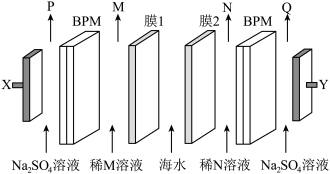
 计)23.4g
计)23.4g


