电化学原理在探究物质性质和实际生产中应用广泛,据此回答下列问题。
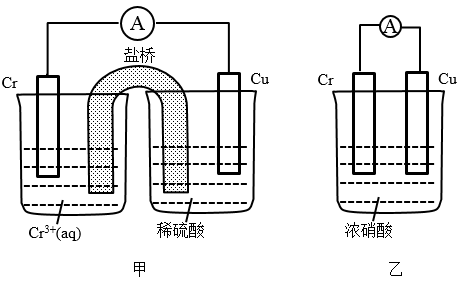
(1)在如图装置中,观察到装置甲铜电极上产生大量的无色气体;而装置乙中铜电极上无气体产生,铬电极上产生大量红棕色气体。由装置甲知铬的金属活动性比铜__ (填“强”或“弱”);由装置乙知常温下铬在浓硝酸中出现__ 现象。
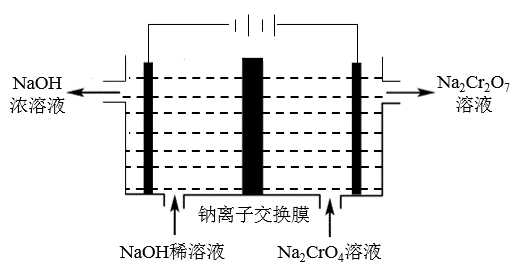
(2)工业上使用如图装置,以石墨作电极电解Na2CrO4溶液,使Na2CrO4转化为Na2Cr2O7,其转化原理为__ 。
(3)CrO3和K2Cr2O7均易溶于水,它们是工业废水造成铬污染的主要原因。要将Cr(Ⅵ)转化为Cr(Ⅲ)常见的处理方法是电解法和铁氧磁体法。
①电解法:将含Cr2O 的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极产物和Cr2O
的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极产物和Cr2O 发生反应,则阳极的电极反应式为
发生反应,则阳极的电极反应式为__ 。阴极上Cr2O 、H+、Fe3+都可能放电。若Cr2O
、H+、Fe3+都可能放电。若Cr2O 放电,则阴极的电极反应式为
放电,则阴极的电极反应式为__ ;若H+放电,则阴极区形成Fe(OH)3和Cr(OH)3沉淀。
②铁氧磁体法:在含Cr(Ⅵ)的废水中加入绿矾,在pH<4时发生反应使Cr(Ⅵ)转化为Cr(Ⅲ),调节溶液pH为6~8,使溶液中的Fe(Ⅱ)、Fe(Ⅲ)、Cr(Ⅲ)析出组成相当于Fe(Ⅱ)[Fe(Ⅲ)x•Cr(Ⅲ)2-x]O4(铁氧磁体)的沉淀,则铁氧磁体中x=___ 。
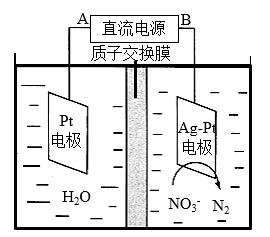
(4)电解法还可用于处理酸性硝酸盐污水,设计如图电解池。若电解过程中转移了0.1mol电子,则质子交换膜两侧电解液的质量变化差(△m左−△m右)为___ g。

(1)在如图装置中,观察到装置甲铜电极上产生大量的无色气体;而装置乙中铜电极上无气体产生,铬电极上产生大量红棕色气体。由装置甲知铬的金属活动性比铜
(2)工业上使用如图装置,以石墨作电极电解Na2CrO4溶液,使Na2CrO4转化为Na2Cr2O7,其转化原理为

(3)CrO3和K2Cr2O7均易溶于水,它们是工业废水造成铬污染的主要原因。要将Cr(Ⅵ)转化为Cr(Ⅲ)常见的处理方法是电解法和铁氧磁体法。
①电解法:将含Cr2O
 的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极产物和Cr2O
的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极产物和Cr2O 发生反应,则阳极的电极反应式为
发生反应,则阳极的电极反应式为 、H+、Fe3+都可能放电。若Cr2O
、H+、Fe3+都可能放电。若Cr2O 放电,则阴极的电极反应式为
放电,则阴极的电极反应式为②铁氧磁体法:在含Cr(Ⅵ)的废水中加入绿矾,在pH<4时发生反应使Cr(Ⅵ)转化为Cr(Ⅲ),调节溶液pH为6~8,使溶液中的Fe(Ⅱ)、Fe(Ⅲ)、Cr(Ⅲ)析出组成相当于Fe(Ⅱ)[Fe(Ⅲ)x•Cr(Ⅲ)2-x]O4(铁氧磁体)的沉淀,则铁氧磁体中x=
(4)电解法还可用于处理酸性硝酸盐污水,设计如图电解池。若电解过程中转移了0.1mol电子,则质子交换膜两侧电解液的质量变化差(△m左−△m右)为

20-21高二上·湖南长沙·期中 查看更多[2]
湖南师范大学附属中学2020-2021学年高二上学期期中考试化学试题(已下线)专题4.2.1 电解原理(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)
更新时间:2020-12-24 14:30:10
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】根据氧化还原反应Cu + 2Ag+ = Cu2+ + 2Ag设计一个原电池?并判断正负极、写出各电极电极反应方程和反应的类型(在方框内画出原电池装置图)____
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】利用反应Cu+2Ag+=2Ag+Cu2+设计了如图所示的原电池。回答下列问题:
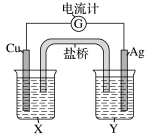
(1)该原电池的负极材料是__________ ,发生________ (填“氧化”或“还原”)反应。
(2)X是__________ ,Y是__________ 。
(3)正极上出现的现象是____________ 。
(4)在外电路中,电子从________ (填写电极材料)极流向________ 极。

(1)该原电池的负极材料是
(2)X是
(3)正极上出现的现象是
(4)在外电路中,电子从
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】分别按图甲、乙所示装置进行实验,两个烧杯里的溶液为同浓度的稀硫酸,甲中为电流表。请回答下列问题:

(1)下列叙述正确的是___________ (填字母)。
A.两烧杯中铜片表面均无气泡产生 B.甲中铜片作正极,乙中铜片作负极
C.两烧杯溶液中 浓度均减小 D.甲产生气泡的速率比乙慢
浓度均减小 D.甲产生气泡的速率比乙慢
(2)甲装置中的能量转化形式:___________ 能转化为___________ 能,乙装置中的能量转化形式:___________ 能转化为___________ 能。
(3)某同学发生甲装置中不仅铜片上有气泡产生,且锌片上也产生了气泡,原因可能是___________ 。
(4)在甲装置中,若把稀硫酸换成CuSO4溶液,试写出铜电极的电极反应:___________ 。

(1)下列叙述正确的是
A.两烧杯中铜片表面均无气泡产生 B.甲中铜片作正极,乙中铜片作负极
C.两烧杯溶液中
 浓度均减小 D.甲产生气泡的速率比乙慢
浓度均减小 D.甲产生气泡的速率比乙慢(2)甲装置中的能量转化形式:
(3)某同学发生甲装置中不仅铜片上有气泡产生,且锌片上也产生了气泡,原因可能是
(4)在甲装置中,若把稀硫酸换成CuSO4溶液,试写出铜电极的电极反应:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】野外生存是特种兵的必修科目。某节目中模拟野外生存,用一个柠檬、一排铜钉和一排锌钉制作的水果电池用于野外生火。某同学感到好奇自己制作了一个这样的“超级柠檬电池”。


(1)该电池的电池反应离子方程式为___________ 。
(2)若用铁片代替锌片,LED灯___________ (填“能”或“不能”,下同)亮。若用铁片代替铜片,LED灯___________ 亮。
(3)若用银片代替锌片,LED灯___________ (填“能”或“不能”)亮。
(4)由上面分析可知构成原电池的条件有___________ 。


(1)该电池的电池反应离子方程式为
(2)若用铁片代替锌片,LED灯
(3)若用银片代替锌片,LED灯
(4)由上面分析可知构成原电池的条件有
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、SO2等气体,严重污染空气。对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
Ⅰ.脱硝:
已知:H2的燃烧热为285.8kJ·mol-1
N2(g)+2O2(g)=2NO2(g) ΔH=+133kJ·mol-1
H2O(g)=H2O(l) ΔH=-44kJ·mol-1
催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为:____________ 。
Ⅱ.脱碳:
(1)向2L密闭容器中加入2molCO2和6molH2,在适当的催化剂作用下,发生反应:
CO2(g)+3H2(g) CH3OH(l)+H2O(l)
CH3OH(l)+H2O(l)
①该反应自发进行的条件是_____________ (填“低温”、“高温”或“任意温度”)
②下列叙述能说明此反应达到平衡状态的是____________ 。(填字母)
a.混合气体的平均式量保持不变 b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等 d.混合气体的密度保持不变
e.1molCO2生成的同时有3mol H—H键断裂
③CO2的浓度随时间(0~t2)变化如下图所示,在t2时将容器容积缩小一倍,t3时达到平衡,t4时降低温度,t5时达到平衡,请画出t2~t6 CO2浓度随时间的变化。_____________
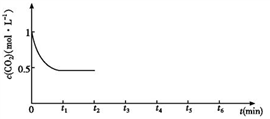
⑵改变温度,使反应CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH﹤0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
CH3OH(g)+H2O(g) ΔH﹤0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
①达到平衡时,反应Ⅰ、Ⅱ对比:平衡常数K(I)______ K(II)(填“﹥”“﹤”或“=”下同);平衡时CH3OH的浓度c(I)____ c(II)。
②对反应Ⅰ,前10min内的平均反应速率v(CH3OH)=_______ 。在其他条件不变的情况下,若30min时只改变温度T2℃,此时H2的物质的量为3.2mol,则T1___ T2(填“>”、“<”或“=”)。若30min时只向容器中再充入1molCO2(g)和1molH2O(g),则平衡_____ 移动(填“正向”“逆向”或“不”)。
⑶利用人工光合作用可将CO2转化为甲酸,反应原理为2CO2+2H2O=2HCOOH+O2,
装置如图所示:
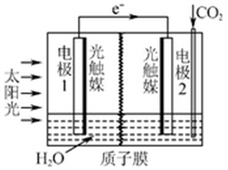
①电极2的电极反应式是____________ ;
②在标准状况下,当电极2室有11.2L CO2反应。 理论上电极1室液体质量_____ (填“增加”或“减少”______ g。
Ⅰ.脱硝:
已知:H2的燃烧热为285.8kJ·mol-1
N2(g)+2O2(g)=2NO2(g) ΔH=+133kJ·mol-1
H2O(g)=H2O(l) ΔH=-44kJ·mol-1
催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为:
Ⅱ.脱碳:
(1)向2L密闭容器中加入2molCO2和6molH2,在适当的催化剂作用下,发生反应:
CO2(g)+3H2(g)
 CH3OH(l)+H2O(l)
CH3OH(l)+H2O(l)①该反应自发进行的条件是
②下列叙述能说明此反应达到平衡状态的是
a.混合气体的平均式量保持不变 b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等 d.混合气体的密度保持不变
e.1molCO2生成的同时有3mol H—H键断裂
③CO2的浓度随时间(0~t2)变化如下图所示,在t2时将容器容积缩小一倍,t3时达到平衡,t4时降低温度,t5时达到平衡,请画出t2~t6 CO2浓度随时间的变化。

⑵改变温度,使反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH﹤0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
CH3OH(g)+H2O(g) ΔH﹤0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:| 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
| 反应Ⅰ:恒温恒容 | 0min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 | ||||
| 反应Ⅱ:绝热恒容 | 0min | 0 | 0 | 2 | 2 |
①达到平衡时,反应Ⅰ、Ⅱ对比:平衡常数K(I)
②对反应Ⅰ,前10min内的平均反应速率v(CH3OH)=
⑶利用人工光合作用可将CO2转化为甲酸,反应原理为2CO2+2H2O=2HCOOH+O2,
装置如图所示:

①电极2的电极反应式是
②在标准状况下,当电极2室有11.2L CO2反应。 理论上电极1室液体质量
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】原电池的生活示例——水果电池
(1)水果电池中,水果的作用是_______ 。
(2)水果电池中,选择电极材料时应注意两电极不能相同,其中有一电极为活泼金属如Al、Fe等,另一电极可以是Cu片或_______ 等。
(3)原电池实验
(1)水果电池中,水果的作用是
(2)水果电池中,选择电极材料时应注意两电极不能相同,其中有一电极为活泼金属如Al、Fe等,另一电极可以是Cu片或
(3)原电池实验
| 电极材料 | 实验现象 | 解释 |
| 锌片、铜片 | 锌、铜、稀硫酸构成原电池, | |
| 锌片、石墨棒 | 锌、石墨、稀硫酸构成原电池, | |
| 铜片、石墨棒 | 铜片、石墨棒表面均无明显现象,电流表指针 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】原电池是将________ 能转化为________ 能的装置。在Al和Cu做电极材料,稀盐酸做电解质溶液的原电池中,Al为________ 极,电极反应式为________ ;Cu为________ 极,电极反应式为________ ;电池总反应式为________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】回答下列问题:
(1)反应NaOH+HCl=NaCl+H2O,能否设计成原电池?
_______ (填“能”或“否”)。
(2)依反应2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图1所示。

请回答下列问题:
①电极X的材料是_______ ;电解质溶液Y是_______ 溶液。
②银电极为电池的_______ 极,发生的电极反应式为_______ ;X电极上发生的电极反应式为_______ 。
(1)反应NaOH+HCl=NaCl+H2O,能否设计成原电池?
(2)依反应2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图1所示。

请回答下列问题:
①电极X的材料是
②银电极为电池的
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】研究化学反应中的能量变化,能更好地利用化学反应为生产和生活服务。
Ⅰ.反应Zn+H2SO4(稀)=ZnSO4+H2↑的能量变化如图所示。
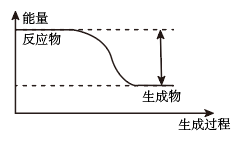
(1)该反应为___________ (填“吸热”或“放热”)反应。
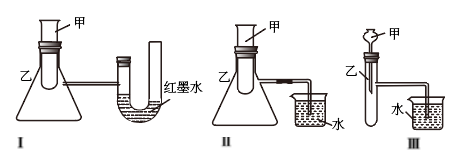
(2)如图三个装置中,不能证明“锌与稀硫酸反应是吸热反应还是放热反应”的是_____ (填序号)
Ⅱ.图是某兴趣小组设计的原电池示意图
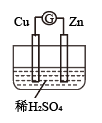
(3)下列实验叙述合理的是_______ (填序号)
A.Cu极有H2产生 B.锌作负极,发生还原反应
C.H+向Zn极移动 D.电子由Zn经导线流向Cu
(4)请写出该电池的正极反应式_________
(5)若有1mol电子流过导线,则理论上在标准状况下,产生H2的体积为______ L
(6)将稀H2SO4换成CuSO4溶液,电极质量增加的是______ (填“锌极”或“铜极”)。
Ⅰ.反应Zn+H2SO4(稀)=ZnSO4+H2↑的能量变化如图所示。

(1)该反应为
(2)如图三个装置中,不能证明“锌与稀硫酸反应是吸热反应还是放热反应”的是

Ⅱ.图是某兴趣小组设计的原电池示意图

(3)下列实验叙述合理的是
A.Cu极有H2产生 B.锌作负极,发生还原反应
C.H+向Zn极移动 D.电子由Zn经导线流向Cu
(4)请写出该电池的正极反应式
(5)若有1mol电子流过导线,则理论上在标准状况下,产生H2的体积为
(6)将稀H2SO4换成CuSO4溶液,电极质量增加的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】电解原理在化学工业中广泛的应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
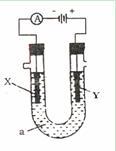
(1)若X、Y都是惰性电极,a是饱和CuSO4溶液,实验开始时,同时在两边各滴入石蕊试液,则①Y电极上的电极反应式为_________________
②在Y电极附近观察到的现象是_____________________________
(2)若X、Y都是铜电极,a是浓度均为2mol·L-1的AgNO3与Cu(NO3)2的混合溶液1L,电解一段时间后X电极上有12.8g铜析出,此时直流电源已输出____ mol电子。
(3)用石墨电极电解100mLH2SO4和CuSO4混合液,通电一段时间后,两极各出现气体3.36L(标准状况),求原来溶液中CuSO4的浓度_________________ 。

(1)若X、Y都是惰性电极,a是饱和CuSO4溶液,实验开始时,同时在两边各滴入石蕊试液,则①Y电极上的电极反应式为
②在Y电极附近观察到的现象是
(2)若X、Y都是铜电极,a是浓度均为2mol·L-1的AgNO3与Cu(NO3)2的混合溶液1L,电解一段时间后X电极上有12.8g铜析出,此时直流电源已输出
(3)用石墨电极电解100mLH2SO4和CuSO4混合液,通电一段时间后,两极各出现气体3.36L(标准状况),求原来溶液中CuSO4的浓度
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】如图所示,A、B、C三个装置中的烧杯分别盛有足量的CuCl2溶液。

(1)A、B、C三个装置中属于原电池的是______ (填标号,下同),属于电解池的是_______ 。
(2)A池中Zn发生______ (填“氧化”或“还原”)反应,Cu电极反应式为_______ 。
(3)B池中C是_____ 极,Pt极发生的电极反应为______ 。
(4)C池反应过程中,溶液浓度______ (填“变大”“变小”或“不变”)。

(1)A、B、C三个装置中属于原电池的是
(2)A池中Zn发生
(3)B池中C是
(4)C池反应过程中,溶液浓度
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】实验室用石墨电极电解加有酚酞的饱和NaCl溶液,装置如图1所示。氯碱工业用图2所示装置制备NaOH等工业原料。

Ⅰ.实验室电解饱和食盐水(图1)
(1)a为电解池的_________ 极,a处的电极反应式为___________ 。
(2)b处的电极反应式为___________ ,观察到的实验现象是____________ 。
(3)该电解池中发生的总反应的离子方程式为____________ 。
(4)下列与电解饱和食盐水有关的说法,正确的是___________ (填字母)。
A. 通电使NaCl发生电离
B. 在溶液中,阴离子向电极a移动
C. 电解熔融NaCl与电解NaCl溶液所得产物相同
Ⅱ.氯碱工业(图2)
(5)利用实验室装置制备NaOH,不仅有安全隐患,而且存在Cl2与NaOH的副反应,氯碱工业采用改进后的装置,如图2所示。
① 气体X和气体Y被阳离子交换膜分隔开,避免混合爆炸。气体X是____ ,气体Y是______ 。
②阳离子交换膜避免了Cl2与NaOH发生反应,可得到NaOH浓溶液,简述NaOH浓溶液的生成过程______ 。

Ⅰ.实验室电解饱和食盐水(图1)
(1)a为电解池的
(2)b处的电极反应式为
(3)该电解池中发生的总反应的离子方程式为
(4)下列与电解饱和食盐水有关的说法,正确的是
A. 通电使NaCl发生电离
B. 在溶液中,阴离子向电极a移动
C. 电解熔融NaCl与电解NaCl溶液所得产物相同
Ⅱ.氯碱工业(图2)
(5)利用实验室装置制备NaOH,不仅有安全隐患,而且存在Cl2与NaOH的副反应,氯碱工业采用改进后的装置,如图2所示。
① 气体X和气体Y被阳离子交换膜分隔开,避免混合爆炸。气体X是
②阳离子交换膜避免了Cl2与NaOH发生反应,可得到NaOH浓溶液,简述NaOH浓溶液的生成过程
您最近一年使用:0次



