某铁的氧化物粉末可能含有FeO、 中的一种或两种。某兴趣小组同学利用以下装置测定铁的氧化物的组成,请回答下列问题:
中的一种或两种。某兴趣小组同学利用以下装置测定铁的氧化物的组成,请回答下列问题:
(已知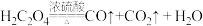 )
)

(1)装置甲的作用是______________________________ 。
(2)装置丁中的实验现象是______________________________________ 。
(3)若丙中铁的氧化物的化学式为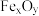 ,则丙中反应的化学方程式为
,则丙中反应的化学方程式为________ 。若丙中铁的氧化物质量为 3. 92 g,且完全反应,丁中生成沉淀的质量为13. 79 g,试确定该氧化物中x:y=_________ 。
(4)实验评价:该装置存在缺点__________ ,改进的方法________ 。
 中的一种或两种。某兴趣小组同学利用以下装置测定铁的氧化物的组成,请回答下列问题:
中的一种或两种。某兴趣小组同学利用以下装置测定铁的氧化物的组成,请回答下列问题:(已知
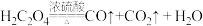 )
)
(1)装置甲的作用是
(2)装置丁中的实验现象是
(3)若丙中铁的氧化物的化学式为
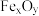 ,则丙中反应的化学方程式为
,则丙中反应的化学方程式为(4)实验评价:该装置存在缺点
更新时间:2020-12-06 21:27:34
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】铁黄(FeOOH)是重要的化工产品。某科研小组在实验室进行铁黄制备研究。
已知:①铁黄制备原理4FeSO4+O2+6H2O 4FeOOH↓+4H2SO4。
4FeOOH↓+4H2SO4。
②为促进生成的铁黄沉淀有序生长,实验时需加入少量已制铁黄作为晶种。
(1)FeOOH可表示为xFe2O3•yH2O,其中 =
=____ 。
(2)铁皮处理:取一定量铁皮,用稀硫酸除去表面铁锈。该除锈反应的化学方程式为_____ 。
(3)制备铁黄:在如图所示装置的三颈烧瓶内进行制备。

步骤一:加入一定量除锈后的碎铁皮
步骤二:加入含有少量铁黄晶种的悬浊液;
步骤三:滴加少量FeSO4溶液;
步骤四:控制合适条件,边搅拌边鼓入空气,充分反应48小时,得到大量FeOOH沉淀。
①将三颈烧瓶中所得FeOOH沉淀分离出来的实验操作是____ (填操作名称)。
②为提高产品纯度,需洗涤分离出的沉淀。洗涤前沉淀表面吸附的阴离子为____ (填离子符号)。
③实验中仅滴加少量 FeSO4溶液,就能得到大量 FeOOH沉淀,其原因是____ 。
已知:①铁黄制备原理4FeSO4+O2+6H2O
 4FeOOH↓+4H2SO4。
4FeOOH↓+4H2SO4。②为促进生成的铁黄沉淀有序生长,实验时需加入少量已制铁黄作为晶种。
(1)FeOOH可表示为xFe2O3•yH2O,其中
 =
=(2)铁皮处理:取一定量铁皮,用稀硫酸除去表面铁锈。该除锈反应的化学方程式为
(3)制备铁黄:在如图所示装置的三颈烧瓶内进行制备。

步骤一:加入一定量除锈后的碎铁皮
步骤二:加入含有少量铁黄晶种的悬浊液;
步骤三:滴加少量FeSO4溶液;
步骤四:控制合适条件,边搅拌边鼓入空气,充分反应48小时,得到大量FeOOH沉淀。
①将三颈烧瓶中所得FeOOH沉淀分离出来的实验操作是
②为提高产品纯度,需洗涤分离出的沉淀。洗涤前沉淀表面吸附的阴离子为
③实验中仅滴加
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】碱式碳酸钴[Cox(OH)y(CO3)z,相对分子质量为365]常用作电子材料、磁性材料的添加剂.碱式碳酸钴中的Co的化合价类似与Fe3O4中Fe的化合价,其中高价态具有强氧化性,而低价态在溶液中能稳定存在,受热时可分解生成三种氧化物。为了确定其组成,某化学兴趣小组同学设计了如图所示的装置进行实验:

(1)请完成下列实验步骤:
①称取一定量的样品置于硬质玻璃管内,称量乙、丙装置的质量;
②按如图所示装置组装好仪器,并_______________ ;
③加热甲中玻璃管,当乙装置中________ (填实验现象),停止加热;
④打开活塞a,缓缓通入空气数分钟后,称量乙、丙装置的质量;
⑤计算。
(2)步骤④中缓缓通入空气数分钟的目的是____________ 。
(3)上述实验装置中存在一个明显缺陷。为解决这一问题,可在_____ (填装置连接位置)增加一个_____ 装置(填字母)。
A.盛有浓硫酸的洗气瓶B.盛有无水氯化钙的U形管
C.盛有P2O5的干燥管D.盛有碱石灰的干燥管
(4)若按正确装置进行实验,测得乙装置增重0.36g,丙装置增重0.88g,则该碱式碳酸钴的化学式为_________ 。
(5)该碱式碳酸钴与浓盐酸反应时,起酸性作用的HCl与被氧化的HCl的物质的量之比为_________ 。

(1)请完成下列实验步骤:
①称取一定量的样品置于硬质玻璃管内,称量乙、丙装置的质量;
②按如图所示装置组装好仪器,并
③加热甲中玻璃管,当乙装置中
④打开活塞a,缓缓通入空气数分钟后,称量乙、丙装置的质量;
⑤计算。
(2)步骤④中缓缓通入空气数分钟的目的是
(3)上述实验装置中存在一个明显缺陷。为解决这一问题,可在
A.盛有浓硫酸的洗气瓶B.盛有无水氯化钙的U形管
C.盛有P2O5的干燥管D.盛有碱石灰的干燥管
(4)若按正确装置进行实验,测得乙装置增重0.36g,丙装置增重0.88g,则该碱式碳酸钴的化学式为
(5)该碱式碳酸钴与浓盐酸反应时,起酸性作用的HCl与被氧化的HCl的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】图中X、Y、Z为单质,G为混合物,其他为化合物,它们之间存在如下转化关系(部分产物已略去)。其中,A俗称磁性氧化铁;E是不溶于水的酸性氧化物,能与氢氟酸反应。

请回答下列问题:
(1)D的化学式为_____ 。
(2)一定条件下,Z与H2反应生成ZH4,ZH4的电子式为_______ 。
(3)写出A和D的稀溶液反应生成G的离子方程式:_____________ 。
(4)写出E与NaOH溶液反应转化为M的化学方程式:_____________ 。

请回答下列问题:
(1)D的化学式为
(2)一定条件下,Z与H2反应生成ZH4,ZH4的电子式为
(3)写出A和D的稀溶液反应生成G的离子方程式:
(4)写出E与NaOH溶液反应转化为M的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】氨气与灼热的氧化铜反应生成铜、氮气和水。利用下图所示实验装置可测定氨分子的组成(图中夹持、固定装置部分均略去)。回答下列问题:

(1)写出氨气与氧化铜反应的化学方程式:__________________________________ 。
(2)在A的锥形瓶中放入NaOH固体的目的是________________________________ 。
(3)在干燥管B中不能选用的干燥剂是_____ (填序号);
(4)E装置中盛装浓硫酸的目的是:__________________________ ;
(5)待实验完毕后,若实验测得N2的体积(折算成标准状况)a L,干燥管D增重b g, 则氨分子中氮、氢的原子个数比为(用含a、b字母的代数式表示)_____________ 。
(6)实验室可用下图所示装置(缺少收集装置,夹持固定装置略去)制备并收集NH3
①在图中方框内画出用烧瓶收集甲的仪器装置简图___________ 。
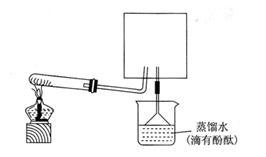
②烧杯中溶液由无色变为红色,其原因是(用电离方程式表示)__________________ 。

(1)写出氨气与氧化铜反应的化学方程式:
(2)在A的锥形瓶中放入NaOH固体的目的是
(3)在干燥管B中不能选用的干燥剂是
| A.碱石灰 | B.生石灰 | C.五氧化二磷 | D.氢氧化钠 |
(5)待实验完毕后,若实验测得N2的体积(折算成标准状况)a L,干燥管D增重b g, 则氨分子中氮、氢的原子个数比为(用含a、b字母的代数式表示)
(6)实验室可用下图所示装置(缺少收集装置,夹持固定装置略去)制备并收集NH3
①在图中方框内画出用烧瓶收集甲的仪器装置简图

②烧杯中溶液由无色变为红色,其原因是(用电离方程式表示)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】氧化还原法、沉淀法等是常用于治理水体污染的重要化学方法。
(1)还原法处理含铬废水:铝粉可将废水中的 还原为
还原为 。如图1所示,废水的不同初始
。如图1所示,废水的不同初始 对
对 去除效果有重要影响。
去除效果有重要影响。
①酸性条件下,铝粉去除 反应的离子方程式:
反应的离子方程式:___________ 。
②实验证明,若初始 过低,
过低, 的去除效果也不理想,其原因可能是
的去除效果也不理想,其原因可能是___________ 。

(2)室温下向 中逐滴加入
中逐滴加入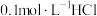 。溶液中含碳元素微粒的物质的量随
。溶液中含碳元素微粒的物质的量随 变化的图像如下图2(
变化的图像如下图2( 因有逸出未画出)。
因有逸出未画出)。
①在 的过程中,反应的离子反应方程式为
的过程中,反应的离子反应方程式为___________ ;B点溶液中
___________  。
。
②配制 溶液时,下列操作会导致溶液浓度偏低的是
溶液时,下列操作会导致溶液浓度偏低的是___________ 。
a、洗涤后容量瓶未干燥
b、将烧杯中的溶液沿玻璃棒注入容量瓶后立即加水定容
c、定容时俯视刻度线
d、摇匀后加水至液面与刻度线相切
③为确定试样 的组成,某同学做如下实验:
的组成,某同学做如下实验:
A.取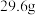 的试样,用酒精灯对其充分加热至恒重,冷却后称其质量为
的试样,用酒精灯对其充分加热至恒重,冷却后称其质量为 。残留在试管中的固体是
。残留在试管中的固体是___________ (填化学式)。
B.另取质量为 的试样加水溶解后配成
的试样加水溶解后配成 溶液,逐滴加入
溶液,逐滴加入 ,至
,至 时,消耗
时,消耗 溶液
溶液 ,继续滴加
,继续滴加 至反应完全时,又消耗
至反应完全时,又消耗 溶液
溶液 ,则试样中
,则试样中 的质量分数为
的质量分数为___________ 。
(1)还原法处理含铬废水:铝粉可将废水中的
 还原为
还原为 。如图1所示,废水的不同初始
。如图1所示,废水的不同初始 对
对 去除效果有重要影响。
去除效果有重要影响。①酸性条件下,铝粉去除
 反应的离子方程式:
反应的离子方程式:②实验证明,若初始
 过低,
过低, 的去除效果也不理想,其原因可能是
的去除效果也不理想,其原因可能是
(2)室温下向
 中逐滴加入
中逐滴加入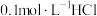 。溶液中含碳元素微粒的物质的量随
。溶液中含碳元素微粒的物质的量随 变化的图像如下图2(
变化的图像如下图2( 因有逸出未画出)。
因有逸出未画出)。①在
 的过程中,反应的离子反应方程式为
的过程中,反应的离子反应方程式为
 。
。②配制
 溶液时,下列操作会导致溶液浓度偏低的是
溶液时,下列操作会导致溶液浓度偏低的是a、洗涤后容量瓶未干燥
b、将烧杯中的溶液沿玻璃棒注入容量瓶后立即加水定容
c、定容时俯视刻度线
d、摇匀后加水至液面与刻度线相切
③为确定试样
 的组成,某同学做如下实验:
的组成,某同学做如下实验:A.取
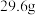 的试样,用酒精灯对其充分加热至恒重,冷却后称其质量为
的试样,用酒精灯对其充分加热至恒重,冷却后称其质量为 。残留在试管中的固体是
。残留在试管中的固体是B.另取质量为
 的试样加水溶解后配成
的试样加水溶解后配成 溶液,逐滴加入
溶液,逐滴加入 ,至
,至 时,消耗
时,消耗 溶液
溶液 ,继续滴加
,继续滴加 至反应完全时,又消耗
至反应完全时,又消耗 溶液
溶液 ,则试样中
,则试样中 的质量分数为
的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】二氧化氯( )是国际上公认的安全、无毒的绿色消毒剂。常温下
)是国际上公认的安全、无毒的绿色消毒剂。常温下 为黄绿色气体,其熔为-59.5℃,沸为11.0℃,极易溶于水,不与水反应,其水溶液在温度超过95℃时易发生爆炸。某研究性学习小组拟用如图所示装置制取并收集
为黄绿色气体,其熔为-59.5℃,沸为11.0℃,极易溶于水,不与水反应,其水溶液在温度超过95℃时易发生爆炸。某研究性学习小组拟用如图所示装置制取并收集 (加热和夹持装置均省略)。
(加热和夹持装置均省略)。

(1)已知: 浓溶液经稀硫酸酸化生成NaCl,并出
浓溶液经稀硫酸酸化生成NaCl,并出 。则装置A中发生反应的离子方程式为
。则装置A中发生反应的离子方程式为_________________________________________________________ 。
(2)制取 时要控制温度在56~80℃,原因是
时要控制温度在56~80℃,原因是_________________________ 。
(3)B装置的作用是_____________________________ 。
(4)D装置的NaOH溶液吸收尾气中的 ,生成物质的量之比为1∶1的两种盐,一种为
,生成物质的量之比为1∶1的两种盐,一种为 ,另一种为
,另一种为_____________ (填化学式)。
(5)为测定某 溶液中
溶液中 的含量,进行了下列实验:
的含量,进行了下列实验:
步骤1:量取 溶液10.00mL,稀释成100mL试样,取
溶液10.00mL,稀释成100mL试样,取 mL试样加入锥形瓶中;
mL试样加入锥形瓶中;
步骤2:调节试样的pH≤2.0,加入足量的KI晶体,振荡后,静置片刻;
步骤3:加入几滴淀粉溶液,用c
 标准溶液滴定至终,消耗
标准溶液滴定至终,消耗 标准溶液
标准溶液 mL。
mL。
已知: ;
;
①由大苏打( )晶体配制250mL c
)晶体配制250mL c 
 标准溶液,在下列图示中一定不需要的仪器为
标准溶液,在下列图示中一定不需要的仪器为__________________________ (写出名称)。

②步骤1中量取 溶液所用的仪器为
溶液所用的仪器为_____________ (填“酸式”或“碱式”)滴定管。
③步骤3中判断达到滴定终的方法是_______________________ 。
④原 溶液的物质的量浓度为
溶液的物质的量浓度为_____________  (用含字母的代数式表示)。
(用含字母的代数式表示)。
 )是国际上公认的安全、无毒的绿色消毒剂。常温下
)是国际上公认的安全、无毒的绿色消毒剂。常温下 为黄绿色气体,其熔为-59.5℃,沸为11.0℃,极易溶于水,不与水反应,其水溶液在温度超过95℃时易发生爆炸。某研究性学习小组拟用如图所示装置制取并收集
为黄绿色气体,其熔为-59.5℃,沸为11.0℃,极易溶于水,不与水反应,其水溶液在温度超过95℃时易发生爆炸。某研究性学习小组拟用如图所示装置制取并收集 (加热和夹持装置均省略)。
(加热和夹持装置均省略)。
(1)已知:
 浓溶液经稀硫酸酸化生成NaCl,并出
浓溶液经稀硫酸酸化生成NaCl,并出 。则装置A中发生反应的离子方程式为
。则装置A中发生反应的离子方程式为(2)制取
 时要控制温度在56~80℃,原因是
时要控制温度在56~80℃,原因是(3)B装置的作用是
(4)D装置的NaOH溶液吸收尾气中的
 ,生成物质的量之比为1∶1的两种盐,一种为
,生成物质的量之比为1∶1的两种盐,一种为 ,另一种为
,另一种为(5)为测定某
 溶液中
溶液中 的含量,进行了下列实验:
的含量,进行了下列实验:步骤1:量取
 溶液10.00mL,稀释成100mL试样,取
溶液10.00mL,稀释成100mL试样,取 mL试样加入锥形瓶中;
mL试样加入锥形瓶中;步骤2:调节试样的pH≤2.0,加入足量的KI晶体,振荡后,静置片刻;
步骤3:加入几滴淀粉溶液,用c

 标准溶液滴定至终,消耗
标准溶液滴定至终,消耗 标准溶液
标准溶液 mL。
mL。已知:
 ;
;
①由大苏打(
 )晶体配制250mL c
)晶体配制250mL c 
 标准溶液,在下列图示中一定不需要的仪器为
标准溶液,在下列图示中一定不需要的仪器为
②步骤1中量取
 溶液所用的仪器为
溶液所用的仪器为③步骤3中判断达到滴定终的方法是
④原
 溶液的物质的量浓度为
溶液的物质的量浓度为 (用含字母的代数式表示)。
(用含字母的代数式表示)。
您最近一年使用:0次



