“绿水青山,就是金山银山”,工业排放的废水要检测合格才能排放,某化工生产基地排放的废水中可能含有以下离子中的若干种:K+、 、Mg2+、Cu2+、Cl-、
、Mg2+、Cu2+、Cl-、 、
、 ,相关专业人士现各取100 mL无色溶液三份进行如下实验:①向第一份加入AgNO3溶液,有白色沉淀产生;②第二份经实验测得溶液中含
,相关专业人士现各取100 mL无色溶液三份进行如下实验:①向第一份加入AgNO3溶液,有白色沉淀产生;②第二份经实验测得溶液中含 0.04 mol;③向第三份加入足量BaCl2溶液,得到沉淀6.27 g,经足量盐酸洗涤后,剩余2.33 g。
0.04 mol;③向第三份加入足量BaCl2溶液,得到沉淀6.27 g,经足量盐酸洗涤后,剩余2.33 g。
试回答下列问题:
(1)该溶液中肯定不存在的离子有_______ 。
(2)可能存在的离子是_______ ,判断该离子存在与否的实验操作是_______ 。
(3)若存在K+,则c(K+)至少为_______ mol∙L−1,说明理由_________ 。(若不存在K+此空可以不填)
 、Mg2+、Cu2+、Cl-、
、Mg2+、Cu2+、Cl-、 、
、 ,相关专业人士现各取100 mL无色溶液三份进行如下实验:①向第一份加入AgNO3溶液,有白色沉淀产生;②第二份经实验测得溶液中含
,相关专业人士现各取100 mL无色溶液三份进行如下实验:①向第一份加入AgNO3溶液,有白色沉淀产生;②第二份经实验测得溶液中含 0.04 mol;③向第三份加入足量BaCl2溶液,得到沉淀6.27 g,经足量盐酸洗涤后,剩余2.33 g。
0.04 mol;③向第三份加入足量BaCl2溶液,得到沉淀6.27 g,经足量盐酸洗涤后,剩余2.33 g。试回答下列问题:
(1)该溶液中肯定不存在的离子有
(2)可能存在的离子是
(3)若存在K+,则c(K+)至少为
更新时间:2020-12-25 16:26:26
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】实验室现有BaCl2、NaNO3、HNO3、HCl、NaHCO3、AgNO3六种溶液,现从中任取四种溶液,编号为A、B、C、D并进行相关实验。其中A属于盐类且与能B反应生气体,B、C、D间反应现象的记录如表。回答下列问题:
(1)根据实验现象及已知条件,可推断出四种溶液中溶质的化学式:A_______ ;B_______ ;C_______ ;D_______ 。
(2)按要求写出下列反应的化学方程式:
①A和B的反应:_______ 。
②B和D的反应:_______ 。
③C和D的反应:_______ 。
| 溶液 | B | C | D |
| B | —— | 不反应 | ↓ |
| C | 不反应 | —— | ↓ |
| D | ↓ | ↓ | —— |
(2)按要求写出下列反应的化学方程式:
①A和B的反应:
②B和D的反应:
③C和D的反应:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】有五瓶损坏标签的试剂,分别盛有AgNO3溶液、稀硝酸、盐酸、氯化钡溶液、碳酸钾溶液,为了确定各瓶中是什么试剂,将它们任意编号为A、B、C、D、E,用小试管各盛少量多次进行两两混合反应,反应现象为:A与B、A与E产生沉淀,B与D、B与E产生沉淀,C与E、D与E产生气体,而C与D无反应现象。
(1)由此,可判定各试剂瓶中所盛试剂为:(填写溶质的化学式)
A_______ 、B_______ 、C_______ 、D_______ 、E_______
(2)请写出下列离子方程式:
A与E:_______ 。
B与E:_______ 。
C与E:_______ 。
(1)由此,可判定各试剂瓶中所盛试剂为:(填写溶质的化学式)
A
(2)请写出下列离子方程式:
A与E:
B与E:
C与E:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】回答下列问题:
(1)某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了如图实验,如图Ⅰ~Ⅳ所示。
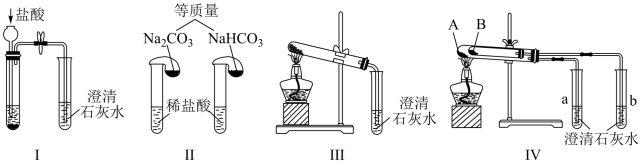
①只根据图Ⅰ、Ⅱ所示实验,能够达到实验目的的是_______ (填装置序号);
②图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为_______ 、_______ ;与实验Ⅲ相比,实验Ⅳ的优点是_______ (填字母);
A.Ⅳ比Ⅲ复杂
B. Ⅳ比Ⅲ安全
C. Ⅳ比Ⅲ操作简便
D. Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行
③若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管 中装入的固体最好是
中装入的固体最好是_______ (填化学式)。
(2)已知 和
和 两支试管所盛的溶液中共含有
两支试管所盛的溶液中共含有 、
、 、
、 、
、 、
、 、
、 六种离子,向试管
六种离子,向试管 的溶液中滴入酚酞试液呈粉红色。请回答下列问题:
的溶液中滴入酚酞试液呈粉红色。请回答下列问题:
①试管 的溶液中所含的上述离子有
的溶液中所含的上述离子有_______ ;
②若向某试管中滴入稀盐酸产生沉淀,则该试管为_______ (填“ ”或“
”或“ ”);
”);
③若向试管 的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是
的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是_______ (填化学式);
④若向由试管 溶液中的阳离子组成的碳酸氢盐溶液中,滴入少量
溶液中的阳离子组成的碳酸氢盐溶液中,滴入少量 溶液,则发生反应的离子方程式为
溶液,则发生反应的离子方程式为_______ 。
(1)某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了如图实验,如图Ⅰ~Ⅳ所示。

①只根据图Ⅰ、Ⅱ所示实验,能够达到实验目的的是
②图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为
A.Ⅳ比Ⅲ复杂
B. Ⅳ比Ⅲ安全
C. Ⅳ比Ⅲ操作简便
D. Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行
③若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管
 中装入的固体最好是
中装入的固体最好是(2)已知
 和
和 两支试管所盛的溶液中共含有
两支试管所盛的溶液中共含有 、
、 、
、 、
、 、
、 、
、 六种离子,向试管
六种离子,向试管 的溶液中滴入酚酞试液呈粉红色。请回答下列问题:
的溶液中滴入酚酞试液呈粉红色。请回答下列问题:①试管
 的溶液中所含的上述离子有
的溶液中所含的上述离子有②若向某试管中滴入稀盐酸产生沉淀,则该试管为
 ”或“
”或“ ”);
”);③若向试管
 的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是
的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是④若向由试管
 溶液中的阳离子组成的碳酸氢盐溶液中,滴入少量
溶液中的阳离子组成的碳酸氢盐溶液中,滴入少量 溶液,则发生反应的离子方程式为
溶液,则发生反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】已知:CO2+Ca(OH)2=CaCO3↓+H2O,CaCO3+CO2+H2O=Ca(HCO3)2,且Ca(HCO3)2易溶于水。试根据如图所示装置回答下列问题:(提示:溶液导电能力与溶液中离子浓度成正比)
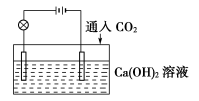
(1)通入CO2前,灯泡________ (填“亮”或“不亮”)。
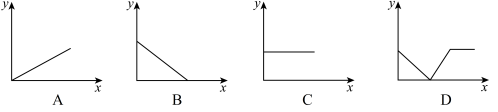
(2)下列四个图中,________ (填字母)能比较准确地反映出溶液的导电能力和通入CO2气体量的关系(x轴表示CO2通入的量,y轴表示导电能力)。

(1)通入CO2前,灯泡
(2)下列四个图中,

您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】1000mL某待测液中除含有0.2 mol·L−1的Na+外,还可能含有下列离子中的一种或多种:
现进行如下实验操作(所加试剂均过量):已知NH + OH-
+ OH-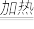 NH3 +H2O↑
NH3 +H2O↑

(1)写出生成白色沉淀B的离子方程式:______________________________ 。
(2)待测液中肯定不存在的离子是_____________ 。
(3)待测液中一定含有的阴离子是__________ ,可能含有的阴离子是__________ 。
(4)判断原溶液中K+是否存在,________________ (填“是”或 “否”),若存在,求 其物质的量浓度的最小值,若不存在,请说明理由_____________________________________ 。
| 阳离子 | K+、NH 、Fe3+、Ba2+ 、Fe3+、Ba2+ |
| 阴离子 | Cl-、 、 、 、 、 |
 + OH-
+ OH-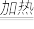 NH3 +H2O↑
NH3 +H2O↑
(1)写出生成白色沉淀B的离子方程式:
(2)待测液中肯定不存在的离子是
(3)待测液中一定含有的阴离子是
(4)判断原溶液中K+是否存在,
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】某无色透明溶液中可能大量存在Na+、Mg2+、Cu2+、Ca2+、SO 、OH-、CO
、OH-、CO 和Cl-中的几种。回答下列问题:
和Cl-中的几种。回答下列问题:
(1)不做任何实验就可以肯定原溶液中不存在的离子是_______ 。
(2)取少量溶液滴入紫色石蕊溶液,溶液呈蓝色,原溶液中一定不存在的离子是_______ 。
(3)取少许溶液滴入BaCl2溶液,有白色沉淀产生,加入稀硝酸,白色沉淀完全溶解。原溶液一定不存在的离子是_______ ;写出白色沉淀溶解的离子方程式:_______ 。
(4)由上述过程可知,不能确定是否存在的离子是_______ ,若要确定该离子,应进行的实验为_______ (写出操作过程和实验现象)。
(5)取原溶液20 mL,逐滴加入0.2 mol∙L−1的Ca(OH)2溶液至恰好完全反应,这时消耗的Ca(OH)2溶液的体积为50 mL。用原溶液配制100 mL0.1 mol∙L−1的Na2CO3溶液,应取用的原溶液的体积为_______ mL。
 、OH-、CO
、OH-、CO 和Cl-中的几种。回答下列问题:
和Cl-中的几种。回答下列问题:(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量溶液滴入紫色石蕊溶液,溶液呈蓝色,原溶液中一定不存在的离子是
(3)取少许溶液滴入BaCl2溶液,有白色沉淀产生,加入稀硝酸,白色沉淀完全溶解。原溶液一定不存在的离子是
(4)由上述过程可知,不能确定是否存在的离子是
(5)取原溶液20 mL,逐滴加入0.2 mol∙L−1的Ca(OH)2溶液至恰好完全反应,这时消耗的Ca(OH)2溶液的体积为50 mL。用原溶液配制100 mL0.1 mol∙L−1的Na2CO3溶液,应取用的原溶液的体积为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】(1)向含有等物质的量的SO32-、Fe2+、Br-、I-的溶液中,通入标准状况下的Cl2,通入Cl2的体积和溶液中相关离子的物质的量关系如图所示。
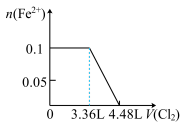
①原溶液中各离子的物质的量是_________ mol
②通入C12 3.36L时,溶液中发生反应的离子方程式有_________ 、_________ 。
(2) 某溶液中仅含下表中的5种离子(不考虑水的电离及离子的水解),且各离子的物质的量均为0.01mol。
a若向溶液中加入KSCN溶液,无明显变化
b若向溶液中加入过量的盐酸,有气体生成,溶液中阴离子种类不变
c若向溶液中加入BaCl2溶液,有白色沉淀生成.
试回答下列问题:
①原溶液中所含的阴离子是_________ ;
②若向原溶液中加入足量NaOH溶液,充分反应后静置一段时间,过滤、洗涤、灼烧,最终所得固体是_________ (写化学式);
③若向原溶液中加入过量盐酸,写出该过程中发生反应的离子方程式_________ 。

①原溶液中各离子的物质的量是
②通入C12 3.36L时,溶液中发生反应的离子方程式有
(2) 某溶液中仅含下表中的5种离子(不考虑水的电离及离子的水解),且各离子的物质的量均为0.01mol。
| 阴离子 | SO42-、NO3-、Cl- |
| 阳离子 | Fe3+、Fe2+、NH4+、Cu2+、Al3+ |
a若向溶液中加入KSCN溶液,无明显变化
b若向溶液中加入过量的盐酸,有气体生成,溶液中阴离子种类不变
c若向溶液中加入BaCl2溶液,有白色沉淀生成.
试回答下列问题:
①原溶液中所含的阴离子是
②若向原溶液中加入足量NaOH溶液,充分反应后静置一段时间,过滤、洗涤、灼烧,最终所得固体是
③若向原溶液中加入过量盐酸,写出该过程中发生反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐2】某工业废水中含有大量的氯化亚铁、较多的氯化铜和少量的氯化钠。为减少污染并变废为宝,该工厂计划从废水中回收氯化亚铁和金属铜,请根据以下流程图,回答下列问题:
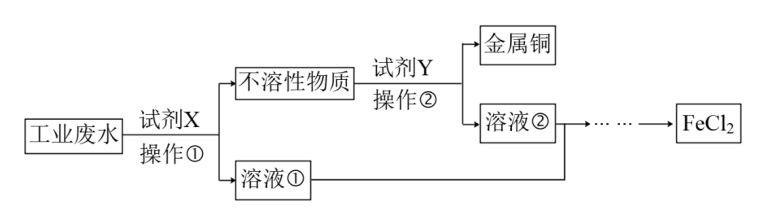
(1)不溶性物质的主要成分为___________ 。
(2)溶液②中溶质为___________ 。
(3)若鉴别溶液②中含有的主要金属阳离子时,应滴加的试剂依次为___________ ,请写出该鉴别过程中属于氧化还原反应的离子方程式___________ 。
(4)回收的氯化亚铁溶于水被氧化后得到氯化铁溶液,氯化铁溶液可用于腐蚀印刷电路板上的铜,向腐蚀后的溶液中加入一定量铁粉,充分反应。
①对反应后的溶液分析正确的是___________ 。
a.溶液中一定含有Fe2+
b.若有固体剩余,固体中一定含有铁
c.若有铁剩余,溶液中可能含有Cu2+
d.溶液若有Fe3+剩余,则一定没有固体析出
②在含有4molFeCl2的溶液中加入4molNa2O2,现象是___________ 。已知反应物恰好完全反应且反应转移6mol电子,发生反应的总的离子方程式:___________ 。

(1)不溶性物质的主要成分为
(2)溶液②中溶质为
(3)若鉴别溶液②中含有的主要金属阳离子时,应滴加的试剂依次为
(4)回收的氯化亚铁溶于水被氧化后得到氯化铁溶液,氯化铁溶液可用于腐蚀印刷电路板上的铜,向腐蚀后的溶液中加入一定量铁粉,充分反应。
①对反应后的溶液分析正确的是
a.溶液中一定含有Fe2+
b.若有固体剩余,固体中一定含有铁
c.若有铁剩余,溶液中可能含有Cu2+
d.溶液若有Fe3+剩余,则一定没有固体析出
②在含有4molFeCl2的溶液中加入4molNa2O2,现象是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】化合物X由3种元素组成.某兴趣小组按如下流程进行实验:

已知 焰色反应呈黄色,其中有两种元素质量分数相同;固体A由两种酸式盐组成。请回答:
焰色反应呈黄色,其中有两种元素质量分数相同;固体A由两种酸式盐组成。请回答:
(1)组成X的元素有______ ,X的化学式是______ 。
(2)X与潮湿空气转化为A的化学方程式是______ 。
(3)用一个化学方程式表示A与足量 溶液的反应
溶液的反应______ 。
(4)碱性条件下,X能够还原废水中的 ,有同学预测该反应可能生成多种酸根离子,设计实验确定产物中的酸根离子
,有同学预测该反应可能生成多种酸根离子,设计实验确定产物中的酸根离子________ (假设反应物无剩余);若上述检验得出产物中只有一种酸根离子,反应的离子方程式________ 。

已知
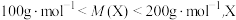 焰色反应呈黄色,其中有两种元素质量分数相同;固体A由两种酸式盐组成。请回答:
焰色反应呈黄色,其中有两种元素质量分数相同;固体A由两种酸式盐组成。请回答:(1)组成X的元素有
(2)X与潮湿空气转化为A的化学方程式是
(3)用一个化学方程式表示A与足量
 溶液的反应
溶液的反应(4)碱性条件下,X能够还原废水中的
 ,有同学预测该反应可能生成多种酸根离子,设计实验确定产物中的酸根离子
,有同学预测该反应可能生成多种酸根离子,设计实验确定产物中的酸根离子
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按如下图所示步骤进行操作。回答下列问题:

(1)试剂Ⅰ的化学式为_______ 。
(2)试剂Ⅱ的化学式为_______ ,②中加入试剂Ⅱ的目的是除去A中的____ ,检验该离子已经除尽的方法是________________________________________________________ 。
(3)③中发生反应的化学方程式为_________________________________________________ 。
(4)由E得到KCl晶体的实验操作是_______________ 。

(1)试剂Ⅰ的化学式为
(2)试剂Ⅱ的化学式为
(3)③中发生反应的化学方程式为
(4)由E得到KCl晶体的实验操作是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】某溶液的溶质可能由下列离子组成:Cl-、SO42-、CO32-、H+、 Ba2+、Na+,某同学进行了如下实验:
(1)向溶液中加入过量的BaCl2溶液,有白色沉淀产生,过滤;
(2)向(1)中滤液里加入AgNO3溶液,有白色沉淀产生;
(3)将(1)中的沉淀加入稀盐酸中,沉淀部分消失,有气体产生。
依据以上实验可以推断,原溶液中一定含有__________ ;一定没有____________________ ;可能含有__________________ 。
(1)向溶液中加入过量的BaCl2溶液,有白色沉淀产生,过滤;
(2)向(1)中滤液里加入AgNO3溶液,有白色沉淀产生;
(3)将(1)中的沉淀加入稀盐酸中,沉淀部分消失,有气体产生。
依据以上实验可以推断,原溶液中一定含有
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】有一白色固体粉末,可能含有NaCl、Na2SO4、Na2CO3、KNO3、BaCl2、CuSO4中的一种或几种,按以下步骤进行实验:
①将该固体粉末放入足量水中得到无色溶液和白色不溶物。
②过滤,在不溶物中加入足量稀盐酸,有气泡产生,充分反应后仍有不溶物存在。
③取②的滤液于试管中,加入Cu粉,微热,一段时间后试管口出现红棕色。
根据以上实验现象判断
(1)混合物中一定没有____________ ;可能有____________ 。
(2)写出②中反应的化学方程式:_______________ 。
(3)写出③中溶液里反应的离子方程式:_______________ 。
①将该固体粉末放入足量水中得到无色溶液和白色不溶物。
②过滤,在不溶物中加入足量稀盐酸,有气泡产生,充分反应后仍有不溶物存在。
③取②的滤液于试管中,加入Cu粉,微热,一段时间后试管口出现红棕色。
根据以上实验现象判断
(1)混合物中一定没有
(2)写出②中反应的化学方程式:
(3)写出③中溶液里反应的离子方程式:
您最近一年使用:0次



