如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
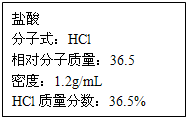
(1)该浓盐酸的物质的量浓度为_______ mol/L
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是_______ 。
A.溶液中HCl的物质的量 B.溶液的浓度 C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.3mol/L稀盐酸。
①该学生需要量取_______ mL上述浓盐酸进行配制。
②配制溶液中所需的玻璃仪器有:烧杯、玻璃棒、_______ 、_______ 、胶头滴管。
③配制过程中,其正确的操作顺序是(用字母表示,每个字母只能用一次)_______ ;
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓盐酸的体积,慢慢沿杯壁注入盛有少量水(约30mL)的烧杯中,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1~2cm处
④在配制过程中,下列实验下列实验操作,造成溶液浓度偏低的是_______ 。
A.用量筒量取浓盐酸时俯视观察凹液面
B.用量筒量取浓盐酸后,洗涤量筒2~3次,洗涤液也转移到容量瓶
C.溶液注入容量瓶前没有恢复到室温就进行定容
D.摇匀后发现液面低于刻度线,再用胶头滴管加水至刻度线

(1)该浓盐酸的物质的量浓度为
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是
A.溶液中HCl的物质的量 B.溶液的浓度 C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.3mol/L稀盐酸。
①该学生需要量取
②配制溶液中所需的玻璃仪器有:烧杯、玻璃棒、
③配制过程中,其正确的操作顺序是(用字母表示,每个字母只能用一次)
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓盐酸的体积,慢慢沿杯壁注入盛有少量水(约30mL)的烧杯中,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1~2cm处
④在配制过程中,下列实验下列实验操作,造成溶液浓度偏低的是
A.用量筒量取浓盐酸时俯视观察凹液面
B.用量筒量取浓盐酸后,洗涤量筒2~3次,洗涤液也转移到容量瓶
C.溶液注入容量瓶前没有恢复到室温就进行定容
D.摇匀后发现液面低于刻度线,再用胶头滴管加水至刻度线
更新时间:2020-12-28 11:48:23
|
相似题推荐
解答题-实验探究题
|
容易
(0.94)
解题方法
【推荐1】实验室需用500 mL 0.1 mol/L NaOH溶液,现用NaOH固体配制该溶液。请回答下列问题:
(1)配制时需要使用的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管、_______ 。
(2)用托盘天平准确称取_______ g NaOH固体。
(3)配制溶液时,有以下操作步骤:
①将容量瓶盖紧,振荡摇匀
②用托盘天平准确称量所需的NaOH,放入烧杯中,再加入适量水,用玻璃棒慢慢搅拌,使其溶解
③用适量水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶中并摇匀
④改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
⑤将已冷却的溶液沿玻璃棒注入容量瓶中
⑥继续往容量瓶内小心加水,直到液面接近刻度线1~2cm处
这些操作步骤的正确顺序为_______ (填序号)
A.②⑤③⑥④①B.②⑤③④⑥①C.②⑤③①⑥④
(4)定容时的操作正确,将容量瓶的玻璃塞盖紧,颠倒摇匀后发现溶液的液面稍低于刻度线,其原因可能是_______ ;取出10 mL该NaOH溶液稀释至20 mL,稀释后的NaOH溶液的物质的量浓度为_______ mol/L。
(5)下列操作会造成所配溶液的浓度偏高的是_______ (填序号)。
①定容时俯视刻度线
②称量固体时所用的砝码生锈
③溶解NaOH的烧杯未洗涤
④溶解时有溶液溅出烧杯
(1)配制时需要使用的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管、
(2)用托盘天平准确称取
(3)配制溶液时,有以下操作步骤:
①将容量瓶盖紧,振荡摇匀
②用托盘天平准确称量所需的NaOH,放入烧杯中,再加入适量水,用玻璃棒慢慢搅拌,使其溶解
③用适量水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶中并摇匀
④改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
⑤将已冷却的溶液沿玻璃棒注入容量瓶中
⑥继续往容量瓶内小心加水,直到液面接近刻度线1~2cm处
这些操作步骤的正确顺序为
A.②⑤③⑥④①B.②⑤③④⑥①C.②⑤③①⑥④
(4)定容时的操作正确,将容量瓶的玻璃塞盖紧,颠倒摇匀后发现溶液的液面稍低于刻度线,其原因可能是
(5)下列操作会造成所配溶液的浓度偏高的是
①定容时俯视刻度线
②称量固体时所用的砝码生锈
③溶解NaOH的烧杯未洗涤
④溶解时有溶液溅出烧杯
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
【推荐2】现用98%的浓H2SO4(密度为1.84g/cm3)配制成浓度为0.5mol/L的稀硫酸500mL。简要回答下列问题。
(1)所需浓硫酸的体积为____ mL,量取时发现量筒不干净,用水冲洗后直接量取将会使所配溶液浓度_____ 。(填偏大、偏小或无影响,下同)
(2)将浓硫酸沿烧杯内壁慢慢注入盛水的烧杯中,不断搅拌的目的是____ ,若搅拌过程中有液体溅出,会使所配溶液浓度______ 。
(3)在转入容量瓶前烧杯中的液体应____ ,否则会使浓度______ 。
(4)定容时,若仰视则会使最终结果______ ;在定容过程中的正确操作应该是_____ 。
(1)所需浓硫酸的体积为
(2)将浓硫酸沿烧杯内壁慢慢注入盛水的烧杯中,不断搅拌的目的是
(3)在转入容量瓶前烧杯中的液体应
(4)定容时,若仰视则会使最终结果
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
【推荐3】某学生需要用0.5mol·L-1的NaCl溶液80mL ,并到实验室进行配制。试回答下列各题。
(1)经计算,应该用托盘天平称取NaCl固体_______ g。
(2)若用NaCl固体配制溶液,需使用的玻璃仪器有_______
(3)配制过程有以下操作:A.移液,B.称量,C.洗涤,D.定容,E.溶解,F。摇匀。其正确的操作顺序应是_______ (填序号)。
(4)下列操作会导致所得溶液浓度偏低的是_______ (填序号)。
A.定容时仰视容量瓶刻度线
B.定容时俯视容量瓶刻度线
C.将溶解冷却的溶液转入容量瓶后就直接转入定容操作
D.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处
(1)经计算,应该用托盘天平称取NaCl固体
(2)若用NaCl固体配制溶液,需使用的玻璃仪器有
(3)配制过程有以下操作:A.移液,B.称量,C.洗涤,D.定容,E.溶解,F。摇匀。其正确的操作顺序应是
(4)下列操作会导致所得溶液浓度偏低的是
A.定容时仰视容量瓶刻度线
B.定容时俯视容量瓶刻度线
C.将溶解冷却的溶液转入容量瓶后就直接转入定容操作
D.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
解题方法
【推荐1】托盘天平、容量瓶、量筒是常见的中学化学计量仪器,熟知这些仪器的使用是定量研究化学的基础。
(1)其中标示出使用温度的仪器是________________ 。
(2)下列操作中,容量瓶所不具备的功能有________________ (填序号)。
A.配制一定体积准确浓度的标准溶液 B.贮存溶液
C.测量容量瓶规格以下的任意体积的溶液 D.准确稀释某一浓度的溶液
E.量取一定体积的液体 F.用来加热溶解固体溶质
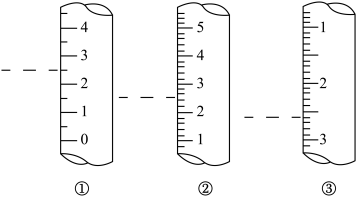
(3)如图是某些仪器的刻度部分示意图,图中各仪器虚线为所示读数。其中为量筒的是________________ (填编号,),读数为_____ mL。
(4)实验室用98%的浓硫酸配制(浓硫酸的密1.84g/mL)450mL 0.1 mol·L-1的硫酸。回答下列问题
① 配制中应选用的玻璃仪器有_________________ ,应量取________ mL 98%的浓硫酸。
② 量筒在使用前已洗干净但不干燥,对结果是否造成影响________ (填“是”或“否”),某同学认为将量筒内的浓硫酸倒出之后,应将量筒洗涤—下并将洗涤液倒入烧杯中,最后转移到容量瓶中,你认为他的做法______ (填“对”或“错”)。
③对浓硫酸稀释过程中遇到下列情况,使所配制的硫酸浓度大于 0.1mol/L有______ (填序号)
A.未经冷却趁热将溶液注入容量瓶中
B.摇匀后发现液面低于刻度线,再加水至刻度线
C.容量瓶中原有少量蒸馏水
D.定容时俯视观察液面
(1)其中标示出使用温度的仪器是
(2)下列操作中,容量瓶所不具备的功能有
A.配制一定体积准确浓度的标准溶液 B.贮存溶液
C.测量容量瓶规格以下的任意体积的溶液 D.准确稀释某一浓度的溶液
E.量取一定体积的液体 F.用来加热溶解固体溶质
(3)如图是某些仪器的刻度部分示意图,图中各仪器虚线为所示读数。其中为量筒的是

(4)实验室用98%的浓硫酸配制(浓硫酸的密1.84g/mL)450mL 0.1 mol·L-1的硫酸。回答下列问题
① 配制中应选用的玻璃仪器有
② 量筒在使用前已洗干净但不干燥,对结果是否造成影响
③对浓硫酸稀释过程中遇到下列情况,使所配制的硫酸浓度大于 0.1mol/L有
A.未经冷却趁热将溶液注入容量瓶中
B.摇匀后发现液面低于刻度线,再加水至刻度线
C.容量瓶中原有少量蒸馏水
D.定容时俯视观察液面
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
【推荐2】现用质量分数为98%、密度为1.84 g·cm-3的浓硫酸来配制480 mL 0.5 mol·L-1的稀硫酸。可供选择的仪器如下图
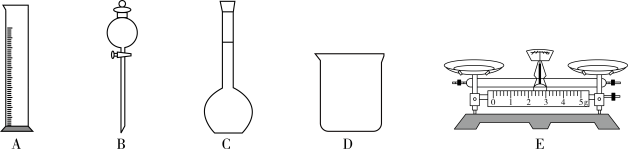
请回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是___________ (填序号),配制上述溶液还需用到的玻璃仪器是_______________ (填仪器名称)。
(2)使用容量瓶之前必须进行的操作是______________________________ 。
(3)经计算,需浓硫酸的体积为_____ mL(小数点后保留 1位小数)。现有 ①10 mL
②50 mL ③100 mL三种规格的量筒,你选用的量筒是____ (填序号)。
(4)配制溶液时,一般可分为以下几个步骤:
①量取 ②计算 ③稀释 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 其正确的操作顺序为:②→①→③→_________ (填序号)。
(5)在配制过程中,其他操作都准确,下列操作使所配溶液浓度偏高的是_______ (填序号)
①洗涤量取浓硫酸的量筒,并将洗涤液转移到容量瓶中
②稀释后的硫酸溶液未等冷却至室温就转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
⑤定容时俯视刻度线

请回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是
(2)使用容量瓶之前必须进行的操作是
(3)经计算,需浓硫酸的体积为
②50 mL ③100 mL三种规格的量筒,你选用的量筒是
(4)配制溶液时,一般可分为以下几个步骤:
①量取 ②计算 ③稀释 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 其正确的操作顺序为:②→①→③→
(5)在配制过程中,其他操作都准确,下列操作使所配溶液浓度偏高的是
①洗涤量取浓硫酸的量筒,并将洗涤液转移到容量瓶中
②稀释后的硫酸溶液未等冷却至室温就转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
⑤定容时俯视刻度线
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
解题方法
【推荐3】实验室用CuSO4固体配制250mL0.25mol/LCuSO4溶液。
(1)用到的仪器有:电子天平、药匙、量筒、烧杯、胶头滴管、玻璃棒和___________ 。
(2)请将以下配置溶液的操作步骤补充完整。
a.计算:计算需要CuSO4固体___________ g。
b.称量:根据计算结果,称量CuSO4固体。
c.溶解:将固体放入烧杯中完全溶解。
d.转移、洗涤:冷却至室温后,将烧杯中的溶液沿___________ 注入容量瓶中,并洗涤烧杯和玻璃棒,将洗涤液也都注入容量瓶。
e.定容、摇匀:将蒸馏水注入容量瓶,当液面离刻度线1-2cm时改用___________ 滴加蒸馏水至溶液的凹液面与刻度线相切。盖好瓶塞,反复上下颠倒,摇匀。
f.贴标签:将配置好的溶液倒入试剂瓶中,贴好标签。
(3)下列操作中,会造成所配制溶液的物质的量浓度偏小的是___________ (填字母)。
a.定容时,俯视刻度线 b.配置过程中忘记洗涤烧杯和玻璃棒
c.转移时有少量溶液洒出 d.配制溶液时未冷却
(4)若用胆矾晶体配制该CuSO4溶液过程中实验操作无任何差错,但配制的浓度总是大于0.25mol/L,分析其原因可能是___________ 。
(1)用到的仪器有:电子天平、药匙、量筒、烧杯、胶头滴管、玻璃棒和
(2)请将以下配置溶液的操作步骤补充完整。
a.计算:计算需要CuSO4固体
b.称量:根据计算结果,称量CuSO4固体。
c.溶解:将固体放入烧杯中完全溶解。
d.转移、洗涤:冷却至室温后,将烧杯中的溶液沿
e.定容、摇匀:将蒸馏水注入容量瓶,当液面离刻度线1-2cm时改用
f.贴标签:将配置好的溶液倒入试剂瓶中,贴好标签。
(3)下列操作中,会造成所配制溶液的物质的量浓度偏小的是
a.定容时,俯视刻度线 b.配置过程中忘记洗涤烧杯和玻璃棒
c.转移时有少量溶液洒出 d.配制溶液时未冷却
(4)若用胆矾晶体配制该CuSO4溶液过程中实验操作无任何差错,但配制的浓度总是大于0.25mol/L,分析其原因可能是
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
【推荐1】现用质量分数为98%、密度为1.84 g·cm-3的浓硫酸来配制480 mL 0.5 mol·L-1的稀硫酸。可供选择的仪器如下图

请回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是___________ (填序号),配制上述溶液还需用到的玻璃仪器是_______________ (填仪器名称)。
(2)使用容量瓶之前必须进行的操作是______________________________ 。
(3)经计算,需浓硫酸的体积为_____ mL(小数点后保留 1位小数)。现有 ①10 mL
②50 mL ③100 mL三种规格的量筒,你选用的量筒是____ (填序号)。
(4)配制溶液时,一般可分为以下几个步骤:
①量取 ②计算 ③稀释 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 其正确的操作顺序为:②→①→③→_________ (填序号)。
(5)在配制过程中,其他操作都准确,下列操作使所配溶液浓度偏高的是_______ (填序号)
①洗涤量取浓硫酸的量筒,并将洗涤液转移到容量瓶中
②稀释后的硫酸溶液未等冷却至室温就转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
⑤定容时俯视刻度线

请回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是
(2)使用容量瓶之前必须进行的操作是
(3)经计算,需浓硫酸的体积为
②50 mL ③100 mL三种规格的量筒,你选用的量筒是
(4)配制溶液时,一般可分为以下几个步骤:
①量取 ②计算 ③稀释 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 其正确的操作顺序为:②→①→③→
(5)在配制过程中,其他操作都准确,下列操作使所配溶液浓度偏高的是
①洗涤量取浓硫酸的量筒,并将洗涤液转移到容量瓶中
②稀释后的硫酸溶液未等冷却至室温就转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
⑤定容时俯视刻度线
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
【推荐2】用18.4mol/L的浓硫酸配制lmol/L稀硫酸100mL,其操作有以下各步:
①用量筒量取若干mL浓硫酸
②洗涤烧杯和玻璃棒2-3次,将洗涤液转入容量瓶中
③将稀释、冷却后的硫酸倒入100 mL容量瓶中
④将浓硫酸倒入盛有水的烧杯中稀释、冷却
⑤加水至液面接近刻度线1~2cm处,定容,摇匀
完成下列填空:
⑴第①步操作中应用量筒量取_______ mL浓硫酸;应选择______ mL量筒(填5、10或50)
⑵本实验用到的基本仪器已有烧杯、量筒、玻璃棒,还缺少的仪器是_______ 、_______ 。(可以不填写满)
⑶正确的操作顺序是(用序号填写)____________________________________________ 。
⑷定容时,如果俯视刻度线,配制的硫酸浓度将偏_______ (填大或小)。
①用量筒量取若干mL浓硫酸
②洗涤烧杯和玻璃棒2-3次,将洗涤液转入容量瓶中
③将稀释、冷却后的硫酸倒入100 mL容量瓶中
④将浓硫酸倒入盛有水的烧杯中稀释、冷却
⑤加水至液面接近刻度线1~2cm处,定容,摇匀
完成下列填空:
⑴第①步操作中应用量筒量取
⑵本实验用到的基本仪器已有烧杯、量筒、玻璃棒,还缺少的仪器是
⑶正确的操作顺序是(用序号填写)
⑷定容时,如果俯视刻度线,配制的硫酸浓度将偏
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
【推荐3】欲配制500 mL 0.5 mol/L的NaOH溶液,试回答下列问题。
(1)计算:需要NaOH固体的质量为_______ 。
(2)某学生用托盘天平称量小烧杯的质量(烧杯中盛NaOH),称量前把游码放在标尺的零刻度,天平静止时发现指针在分度盘的偏右位置,此时左边的托盘将_______ (填“高于”或“低于”)右边的托盘,欲使天平平衡,所进行的操作为_______ 。假定最终称量小烧杯的质量为_______ (填“32.6 g”或“32.61 g”)。
(3)在标尺(图)上画出游码位置(画“△”表示)___________ 。
(1)计算:需要NaOH固体的质量为
(2)某学生用托盘天平称量小烧杯的质量(烧杯中盛NaOH),称量前把游码放在标尺的零刻度,天平静止时发现指针在分度盘的偏右位置,此时左边的托盘将
(3)在标尺(图)上画出游码位置(画“△”表示)
您最近一年使用:0次



