甲醇是一种重要的化工原料和新型燃料。如图是甲醇燃料电池工作的示意图,工作一段时间后,断开K:
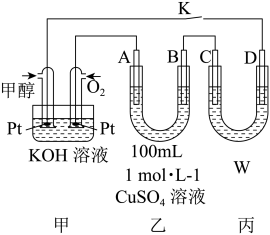
(1)甲中负极的电极反应式为______________________ 。
(2)若丙中C为铝,D为石墨,W溶液为稀H2SO4,则能是铝的表面生成一层致密的氧化膜,则C的电极反应式为_____________________ 。
(3)若A、B、C、D均为石墨,W溶液为饱和氯化钠溶液;
a.丙中电解的总化学方程式为____________________________ 。
b.工作一段时间后,向乙中所得溶液加入0.05 mol Cu2(OH)2CO3后恰好使电解质溶液复原,则转移电子的物质的量为_______________ 。
c.丙中为使两极产物不发生反应,可以在两极之间放置_______ (“阴”或“阳”)离子交换膜。
(4)若把乙装置改为精炼铜装置(粗铜含Al、Zn、Ag、Pt、Au等杂质),下列说法正确的是__________
A.电解过程中,阳极减少的质量与阴极增加的质量相等
B.A为粗铜,发生氧化反应
C.CuSO4溶液的浓度保持不变
D.杂质都将以单质的形式沉淀到池底

(1)甲中负极的电极反应式为
(2)若丙中C为铝,D为石墨,W溶液为稀H2SO4,则能是铝的表面生成一层致密的氧化膜,则C的电极反应式为
(3)若A、B、C、D均为石墨,W溶液为饱和氯化钠溶液;
a.丙中电解的总化学方程式为
b.工作一段时间后,向乙中所得溶液加入0.05 mol Cu2(OH)2CO3后恰好使电解质溶液复原,则转移电子的物质的量为
c.丙中为使两极产物不发生反应,可以在两极之间放置
(4)若把乙装置改为精炼铜装置(粗铜含Al、Zn、Ag、Pt、Au等杂质),下列说法正确的是
A.电解过程中,阳极减少的质量与阴极增加的质量相等
B.A为粗铜,发生氧化反应
C.CuSO4溶液的浓度保持不变
D.杂质都将以单质的形式沉淀到池底
更新时间:2021-01-09 11:17:41
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】电池在生产和生活中应用极其广泛,根据电化学原理回答下列问题。
(1)微型纽扣电池总反应为Ag2O+Zn+H2O=Zn(OH)2+2Ag,电解质溶液为KOH溶液,则负极材料为_______ ,正极的电极反应式为_______ 。
(2)甲醇(CH3OH)燃料电池为绿色化学电源,以NaOH溶液为电解质溶液时,负极的电极反应式为_______ ,该电池工作时,外电路每流过1mol e-,消耗标准状况下的O2_______ L。
(3)ClO2是高效无毒的灭菌剂,目前已开发出用电解法制取ClO2的新工艺,简易装置如图所示:
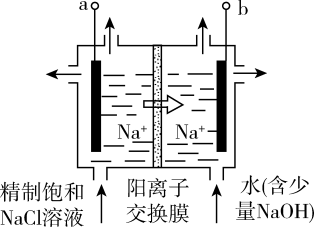
若用上述甲醇燃料电池进行电解,则甲醇燃料电池的负极应连接该装置的_______ 电极(填字母),阳极产生ClO2的电极反应式为_______ 。
(1)微型纽扣电池总反应为Ag2O+Zn+H2O=Zn(OH)2+2Ag,电解质溶液为KOH溶液,则负极材料为
(2)甲醇(CH3OH)燃料电池为绿色化学电源,以NaOH溶液为电解质溶液时,负极的电极反应式为
(3)ClO2是高效无毒的灭菌剂,目前已开发出用电解法制取ClO2的新工艺,简易装置如图所示:

若用上述甲醇燃料电池进行电解,则甲醇燃料电池的负极应连接该装置的
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】据报道,摩托罗拉公司开发了一种以甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月。下图是一个电化学过程的示意图。已知甲池的总反应式为:2CH3OH+3O2+4KOH 2K2CO3+6H2O
2K2CO3+6H2O

请填空:
(1)放电时:负极的电极反应式为_____________________________________________ 。
(2)充电时:①原电池的负极与电源_________ 极相连。
②阳极的电极反应为__________________ 。
(3)在此过程中若完全反应,乙池中B极的质量升高648g,则甲池中理论上消耗O2_________ L(标准状况下)。
 2K2CO3+6H2O
2K2CO3+6H2O
请填空:
(1)放电时:负极的电极反应式为
(2)充电时:①原电池的负极与电源
②阳极的电极反应为
(3)在此过程中若完全反应,乙池中B极的质量升高648g,则甲池中理论上消耗O2
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电源。氢氧燃料电池的突出优点是把化学能直接转化为电能,而不经过热能中间形成,发生的反应为:2H2+O2=2H2O。
(1)碱性氢氧燃料电池的电解质溶液为KOH溶液,则负极反应式为__________________ 。
(2)如把KOH改为稀硫酸作导电物质,则正极反应式为___________________________ ,
反应后溶液中的pH值_______________ (填“增大”或“减小”或“不变”)。
(3)如把H2改为CH3OH,KOH作导电物质,则负极反应式为________________________ 。
(1)碱性氢氧燃料电池的电解质溶液为KOH溶液,则负极反应式为
(2)如把KOH改为稀硫酸作导电物质,则正极反应式为
反应后溶液中的pH值
(3)如把H2改为CH3OH,KOH作导电物质,则负极反应式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流表的指针发生了偏转。

请回答下列问题:
(1)乙池为___________ (填“原电池”“电解池”“电镀池”),A电极的电极反应式为:___________ 。
(2)丙池中F电极为___________ (填“正极”、“负极”、“阴极”或“阳极”),写出电解时总反应的离子方程式___________ 。
(3)当乙池中C极质量变化10.8 g时,甲池中B电极理论上消耗O2的体积为___________ mL(标准状况)。
(4)一段时间后,断开电键K。下列物质能使乙池恢复到反应前浓度的是___________ (填选项字母)。
A.Cu B.CuO C.Cu(OH)2 D.Cu2(OH)2CO3
(5)若丙池通电一段时间后,向所得的溶液中加入0.1 mol Cu2(OH)2CO3后恰好恢复到电解前的浓度和PH(不考虑CO2的溶解),则电解过程中转移的电子___________ mol, 若电解后溶液的体积为400ml,则所得溶液中氢离子的浓度___________ 。

请回答下列问题:
(1)乙池为
(2)丙池中F电极为
(3)当乙池中C极质量变化10.8 g时,甲池中B电极理论上消耗O2的体积为
(4)一段时间后,断开电键K。下列物质能使乙池恢复到反应前浓度的是
A.Cu B.CuO C.Cu(OH)2 D.Cu2(OH)2CO3
(5)若丙池通电一段时间后,向所得的溶液中加入0.1 mol Cu2(OH)2CO3后恰好恢复到电解前的浓度和PH(不考虑CO2的溶解),则电解过程中转移的电子
您最近半年使用:0次
填空题
|
适中
(0.65)
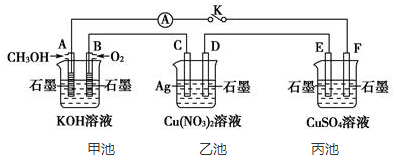
【推荐2】某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的开关K时,观察到电流表的指针发生了偏转。
请回答下列问题:
(1)甲池为__________ (填“原电池”“电解池”或“电镀池”),A电极的电极反应式为_________ 。
(2)丙池中F电极为______ (填“正极”“负极”“阴极”或“阳极”),该池的总反应方程式为___________ 。
(3)当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为_______ mL(标准状况)。
(4)已知丙池中的溶液为400 mL,合上开关K,一段时间后,丙池中,阳极共收集到气体224mL(标况下),则此时溶液的pH为_______________ 。(假设溶液体积保持不变)
请回答下列问题:
(1)甲池为
(2)丙池中F电极为
(3)当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为
(4)已知丙池中的溶液为400 mL,合上开关K,一段时间后,丙池中,阳极共收集到气体224mL(标况下),则此时溶液的pH为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如图是一个电化学过程的示意图,请按要求回答下列问题
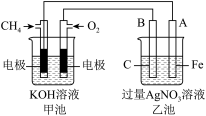
(1)甲池是_______ 装置(填“原电池”或“电解池”)
(2)写出电极反应式:通入CH4的电极_______ 。
(3)反应一段时间后,甲池中消耗1.6g甲烷,则乙池中某电极的质量增_______ g。
(4)反应一段时间后,乙池中溶液成分发生了变化,想要完全恢复到电解前可加入的物质是____
(5)某工厂烟气中主要含SO2,可用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如下图所示(电极材料为石墨)。
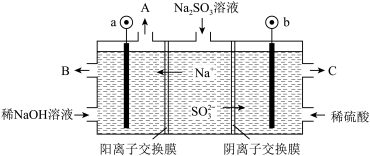
①图中a极要连接电源的_______ (填“正”或“负”)极,C口流出的物质是_______ 。
② 放电的电极反应式为
放电的电极反应式为_______ 。

(1)甲池是
(2)写出电极反应式:通入CH4的电极
(3)反应一段时间后,甲池中消耗1.6g甲烷,则乙池中某电极的质量增
(4)反应一段时间后,乙池中溶液成分发生了变化,想要完全恢复到电解前可加入的物质是
(5)某工厂烟气中主要含SO2,可用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如下图所示(电极材料为石墨)。

①图中a极要连接电源的
②
 放电的电极反应式为
放电的电极反应式为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】电解法转化 CO2可实现 CO2资源化利用。电解 CO2制甲酸(HCOOH)的原理示意图如下:(已知 HCOOH 中 C 的化合价为+2 价)
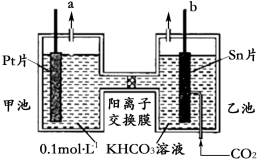
请回答:
(1)a 端连电源的___________ 极。
(2)甲池中放出的气体是___________ ,发生的电极反应式为:___________ 。
(3)电解过程中,产生 HCOO-的电极反应式为:___________ 。电路中转移 0.1mol电子,理论上需消耗CO2___________ L(标准状况)。
(4)电解过程中 K+的移动方向是___________ ,其原因是___________ 。

请回答:
(1)a 端连电源的
(2)甲池中放出的气体是
(3)电解过程中,产生 HCOO-的电极反应式为:
(4)电解过程中 K+的移动方向是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学兴趣小组的同学用如下图所示装置研究有关电化学的问题。当闭合K时,观察到电流表的指针发生了偏移。
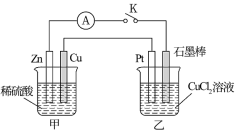
请回答下列问题:
(1)乙装置的名称是________ ;Zn为________ 极。
(2)写出电极反应:Cu极:______________________ ;石墨棒极:______________________ 。
(3)当甲中产生0.1mol气体时,乙中产生的气体在标准状况下的体积应为________________ 。
(4)若乙中溶液不变,将其电极都换成铜电极,闭合K一段时间后,乙中溶液的颜色________ (填“变深”、“变浅”或“无变化”)。
(5)若乙中电极不变,将其溶液换成NaCl溶液,闭合K一段时间后,甲中溶液的pH将________ (填“增大”、“减小”或“不变”,下同);乙中溶液的pH将________ 。
(6)若乙中电极不变,将其溶液换成饱和Na2SO4溶液,闭合K一段时间,当阴极上有a mol气体生成时,同时有w g Na2SO4·10H2O析出,假设温度不变,剩余溶液中溶质的质量分数应为________ (用含w、a的表达式表示,不必化简)。

请回答下列问题:
(1)乙装置的名称是
(2)写出电极反应:Cu极:
(3)当甲中产生0.1mol气体时,乙中产生的气体在标准状况下的体积应为
(4)若乙中溶液不变,将其电极都换成铜电极,闭合K一段时间后,乙中溶液的颜色
(5)若乙中电极不变,将其溶液换成NaCl溶液,闭合K一段时间后,甲中溶液的pH将
(6)若乙中电极不变,将其溶液换成饱和Na2SO4溶液,闭合K一段时间,当阴极上有a mol气体生成时,同时有w g Na2SO4·10H2O析出,假设温度不变,剩余溶液中溶质的质量分数应为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题:
(1)若两池中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲池中的____________ 棒,乙池中的____________ 棒。
②乙池中阳极的电极反应式是___________________ 。
(2)若两池中均为饱和NaCl溶液:
①写出乙池中总反应的离子方程式_________________ 。
②甲池中碳极上电极反应式是_____________________ ,
③若乙池转移0.02 mol e-后停止实验,溶液体积是200 mL,则溶液混合均匀后的pH=____ 。

(1)若两池中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲池中的
②乙池中阳极的电极反应式是
(2)若两池中均为饱和NaCl溶液:
①写出乙池中总反应的离子方程式
②甲池中碳极上电极反应式是
③若乙池转移0.02 mol e-后停止实验,溶液体积是200 mL,则溶液混合均匀后的pH=
您最近半年使用:0次
【推荐1】我国要在2030年前实现碳达峰、2060年前实现碳中和的目标,CO2的捕集与转化是研究的重要课题。
(1)CO2和CH4重整可制合成气CO和H2,其热化学反应方程式为CO2(g)+CH4(g)=2CO(g)+2H2(g) ΔH=+247 kJ·mol-1。
已知下列热化学反应方程式:
反应1:C(s)+2H2(g)=CH4(g) ΔH1
反应2:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2=-40.0 kJ·mol-1
反应3:C(s)+H2O(g)=CO(g)+H2(g) ΔH3=+132.0 kJ·mol-1
则ΔH1=___________ kJ·mol-1。
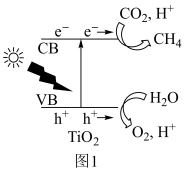
(2)光催化还原法实现CO2甲烷化可能的反应机理如图1所示。该过程可描述为:光照条件下,催化剂TiO2的价带(VB)中的电子激发至导带(CB)中,价带中形成电子空穴(h+),___________ 。
(3)一种电化学法将CO2转化为乙烯的原理如图2所示。
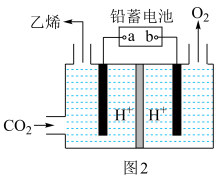
①阴极上的电极反应式为___________ 。
②以铅蓄电池为电源,每生成0.5 mol乙烯,理论上产生O2的物质的量为___________ 。
(1)CO2和CH4重整可制合成气CO和H2,其热化学反应方程式为CO2(g)+CH4(g)=2CO(g)+2H2(g) ΔH=+247 kJ·mol-1。
已知下列热化学反应方程式:
反应1:C(s)+2H2(g)=CH4(g) ΔH1
反应2:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2=-40.0 kJ·mol-1
反应3:C(s)+H2O(g)=CO(g)+H2(g) ΔH3=+132.0 kJ·mol-1
则ΔH1=
(2)光催化还原法实现CO2甲烷化可能的反应机理如图1所示。该过程可描述为:光照条件下,催化剂TiO2的价带(VB)中的电子激发至导带(CB)中,价带中形成电子空穴(h+),

(3)一种电化学法将CO2转化为乙烯的原理如图2所示。

①阴极上的电极反应式为
②以铅蓄电池为电源,每生成0.5 mol乙烯,理论上产生O2的物质的量为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是乙醇燃料电池工作时的示意图,乙池中M、N两个电极的材料是石墨和铁中的一种,工作时M、N两个电极的质量都不减少,请回答:

(1)甲池中通入乙醇的铂电极名称是______ ,通入 的铂电极反应式为
的铂电极反应式为__________________ ;
(2)乙池属于______ (填“原电池”或“电解池”),工作时,乙池中电子流出的电极是______ (填“M”或“N”):
(3)若乙池中某电极析出金属银4.32g时,甲池中理论上消耗氧气为______ L(标准状况下);
(4)如要用电解方法精炼粗铜,乙池电解液选用 溶液,则N电极的材料是
溶液,则N电极的材料是______ ,反应一段时间以后, 溶液的浓度
溶液的浓度______ 。(填“增大”“减小”“不变”)

(1)甲池中通入乙醇的铂电极名称是
 的铂电极反应式为
的铂电极反应式为(2)乙池属于
(3)若乙池中某电极析出金属银4.32g时,甲池中理论上消耗氧气为
(4)如要用电解方法精炼粗铜,乙池电解液选用
 溶液,则N电极的材料是
溶液,则N电极的材料是 溶液的浓度
溶液的浓度
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】乙烷(C2H6)作为一种新能源在化学领域应用广泛,请回答下列问题:(如图所示,装置I为乙烷燃料电池(电解质溶液为KOH溶液),通过装置II实现铁棒上镀铜。

①a处应通入______ (填“C2H6”或“O2”),a处电极上发生的电极反应式是____________________________________ 。
②电镀结束后,装置I中溶液的pH______ (填写“变大”“变小”或“不变”,下同),装置II中Cu2+的物质的量浓度______ 。
③电镀结束后,装置I溶液中的阴离子除了OH-以外还含有___________ (忽略水解);在此过程中若完全反应,装置II中阴极质量变化12.8 g,则装置I中理论上消耗乙烷________ L(标准状况下)。

①a处应通入
②电镀结束后,装置I中溶液的pH
③电镀结束后,装置I溶液中的阴离子除了OH-以外还含有
您最近半年使用:0次



