汽车尾气中的氮氧化物是城市空气的主要污染物之一,如何降低汽车尾气污染已成为环保领域的热点。
回答下列问题:
(1)科技工作者用甲烷将氮氧化物还原为 N2和 H2O,涉及的反应如下:
CH4(g)+4NO2(g) =4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ/mol
CH4(g)+2NO2(g) =CO2(g)+2H2O(g)+N2(g) ΔH2=-867 kJ/mol
则 CH4(g)还原 NO(g)生成 N2(g)的热化学方程式为___________ 。
(2)使用氢能源可以减少汽车尾气中有害气体的排放。利用甲醇与水蒸气反应可以制备氢气:CH3OH(g)+H2O(g) =CO2(g)+3H2(g) ΔH,该反应过程中的能量变化如图:
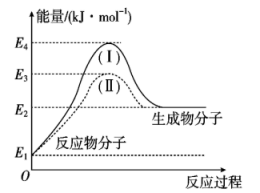
①ΔH___________ 0(填“>”“=”或“<”)。
②途径(Ⅰ)的活化能 E=___________ 。
③途径(Ⅰ)变为途径(Ⅱ):改变的条件是___________ ,反应热(ΔH)___________ (填“增大”“减小”或“不变”)。
回答下列问题:
(1)科技工作者用甲烷将氮氧化物还原为 N2和 H2O,涉及的反应如下:
CH4(g)+4NO2(g) =4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ/mol
CH4(g)+2NO2(g) =CO2(g)+2H2O(g)+N2(g) ΔH2=-867 kJ/mol
则 CH4(g)还原 NO(g)生成 N2(g)的热化学方程式为
(2)使用氢能源可以减少汽车尾气中有害气体的排放。利用甲醇与水蒸气反应可以制备氢气:CH3OH(g)+H2O(g) =CO2(g)+3H2(g) ΔH,该反应过程中的能量变化如图:

①ΔH
②途径(Ⅰ)的活化能 E=
③途径(Ⅰ)变为途径(Ⅱ):改变的条件是
20-21高二上·湖北十堰·期末 查看更多[4]
湖北省十堰市2020-2021学年高二上学期期末考试化学试题(已下线)2.1.3 活化能(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)第07讲 活化能(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)(已下线)2.3.3 化学反应速率综合分析-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修1)
更新时间:2021-01-28 10:36:55
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)高炉冶铁过程中,甲烷在催化反应室中产生水煤气(CO和H2)还原氧化铁,有关反应为:
CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH=+260 kJ·mol-1 ①
2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1 ②
则CH4与O2反应生成CO和H2的热化学方程式为______
(2)0.3 mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态的三氧化二硼和液态水,放出649.5 kJ热量,其表示乙硼烷(B2H6)燃烧热的热化学方程式为:__________
(3)含Ba(OH)2 1 mol的稀溶液与足量稀盐酸反应,放出114.6 kJ的热量,表示该反应中和热的热化学方程式为:__________
(4)2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。

图中A、C分别表示_______ 、_______ ,E的大小对该反应的反应热有无影响?______ 。图中ΔH=________ kJ·mol-1。
CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH=+260 kJ·mol-1 ①
2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1 ②
则CH4与O2反应生成CO和H2的热化学方程式为
(2)0.3 mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态的三氧化二硼和液态水,放出649.5 kJ热量,其表示乙硼烷(B2H6)燃烧热的热化学方程式为:
(3)含Ba(OH)2 1 mol的稀溶液与足量稀盐酸反应,放出114.6 kJ的热量,表示该反应中和热的热化学方程式为:
(4)2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。

图中A、C分别表示
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知: 时,1mol相关物质的相对能量如图所示。
时,1mol相关物质的相对能量如图所示。

(1)写出C2H4完全燃烧生成气态水的热化学方程式___________ 。
(2)H2的燃烧热ΔH=___________ 。
(3)相同条件下,C2H4的稳定性比C2H6___________ (填“强”“弱”或“相同”),等物质的量的C2H4和C2H6完全燃烧放热较多的是___________ 。
(4) 是
是___________ 反应(填“吸热”或“放热”)。
(5)已知键能是指气态分子中1mol化学键解离成气态原子所吸收的能量,相关的化学键键能如下。
已知: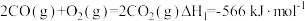 ;则a =
;则a =___________ 。
 时,1mol相关物质的相对能量如图所示。
时,1mol相关物质的相对能量如图所示。
(1)写出C2H4完全燃烧生成气态水的热化学方程式
(2)H2的燃烧热ΔH=
(3)相同条件下,C2H4的稳定性比C2H6
(4)
 是
是(5)已知键能是指气态分子中1mol化学键解离成气态原子所吸收的能量,相关的化学键键能如下。
| 化学键 | C O(CO) O(CO) | O=O | C=O |
| 键能(KJ/mol) | a | 500 | 1075 |
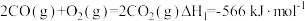 ;则a =
;则a =
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】2SO2(g)+O2(g) 2SO3(g) ΔH反应过程的能量变化如图所示,已知1 mol SO2(g)被氧化为1 mol SO3(g)的ΔH=-98 kJ/mol。回答下列问题:
2SO3(g) ΔH反应过程的能量变化如图所示,已知1 mol SO2(g)被氧化为1 mol SO3(g)的ΔH=-98 kJ/mol。回答下列问题:
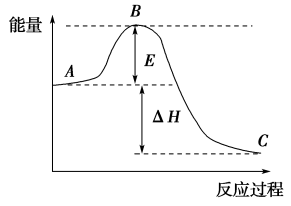
(1)图中A、C分别表示:_____ 、______ 。E的大小对该反应的反应热有无影响?_______ 。该反应通常用V2O5作催化剂,加V2O5会使图中B点_____ (填“升高” “降低”),理由是________ 。
(2)图中ΔH=________ kJ/mol。
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自己被还原为四价钒化合物;四价钒化合物再被氧气氧化生成V2O5。写出该催化循环机理的两步化学方程式:___________ ,________ 。
(4)已知单质硫的燃烧热为296 kJ/mol,计算由S(s)生成3 mol SO3(g)的总反应的ΔH=________ kJ/mol。
 2SO3(g) ΔH反应过程的能量变化如图所示,已知1 mol SO2(g)被氧化为1 mol SO3(g)的ΔH=-98 kJ/mol。回答下列问题:
2SO3(g) ΔH反应过程的能量变化如图所示,已知1 mol SO2(g)被氧化为1 mol SO3(g)的ΔH=-98 kJ/mol。回答下列问题:
(1)图中A、C分别表示:
(2)图中ΔH=
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自己被还原为四价钒化合物;四价钒化合物再被氧气氧化生成V2O5。写出该催化循环机理的两步化学方程式:
(4)已知单质硫的燃烧热为296 kJ/mol,计算由S(s)生成3 mol SO3(g)的总反应的ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氢气、碳氧化物是合成可再生能源甲醇的基础原料,具有重要的应用前景。
(1)已知H2(g)、CO(g)和CH4(g)的燃烧热分别为285.8 kJ/mol、283.0 kJ/mol和890.0 kJ/mol。一定条件下,CO与H2合成燃烧的热化学方程式为:CO(g)+3H2(g)=CH4(g)+H2O(l) △H,则△H=___ ;该反应能自发进行的原因是___ 。
(2)工业上一般采用下列两种反应合成甲醇:
反应A:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
反应B:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
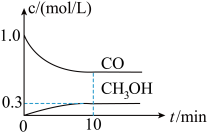
①一定温度下,在体积可变的恒压密闭容器中加入4 mol H2和一定量的CO发生反应A,开始时容器体积为2 L,CO和CH3OH(g)的浓度随时间变化如图1所示,10 min时达到平衡,则反应A的化学平衡常数为_______ 。(结果保留一位小数)。
②恒温恒容条件下,在密闭容器中通入等物质的量的CO2和H2,下列描述能说明反应B已经达到平衡状态的是___ (填序号)。
A. 容器内CO2的体积分数不再变化
B. 当CO2和H2转化率的比值不再变化
C. 当水分子中断裂2NA个O-H键,同时氢分子中断裂3NA个H-H键
D. 容器内混合气体的平均相对分子质量达到34.5,且保持不变
(1)已知H2(g)、CO(g)和CH4(g)的燃烧热分别为285.8 kJ/mol、283.0 kJ/mol和890.0 kJ/mol。一定条件下,CO与H2合成燃烧的热化学方程式为:CO(g)+3H2(g)=CH4(g)+H2O(l) △H,则△H=
(2)工业上一般采用下列两种反应合成甲醇:
反应A:CO(g)+2H2(g)
 CH3OH(g)
CH3OH(g)反应B:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)①一定温度下,在体积可变的恒压密闭容器中加入4 mol H2和一定量的CO发生反应A,开始时容器体积为2 L,CO和CH3OH(g)的浓度随时间变化如图1所示,10 min时达到平衡,则反应A的化学平衡常数为

②恒温恒容条件下,在密闭容器中通入等物质的量的CO2和H2,下列描述能说明反应B已经达到平衡状态的是
A. 容器内CO2的体积分数不再变化
B. 当CO2和H2转化率的比值不再变化
C. 当水分子中断裂2NA个O-H键,同时氢分子中断裂3NA个H-H键
D. 容器内混合气体的平均相对分子质量达到34.5,且保持不变
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】我国2020年颁布的能源法中,首次将氢能纳入能源定义。在工业市场中,甲烷水蒸气重整制氢是目前工业制氢最为成熟的方法,被广泛应用于氢气的工业生产。甲烷水蒸气重整反应体系中主要存在的反应方程式有:
反应1: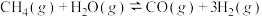
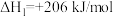
反应2: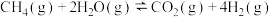

反应3:

(1)
_______  。
。
(2)反应1在_______ 下自发进行(填“高温”,“低温”或“任意温度”)。
(3)一定温度下,向某容积为1L的恒容容器中充入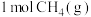 和
和 ,发生上述反应,tmin后反应达到平衡。达到平衡时,容器中CO为mmol,CO2为nmol。
,发生上述反应,tmin后反应达到平衡。达到平衡时,容器中CO为mmol,CO2为nmol。
①tmin内CH4的消耗速率为___  。(用含m,n,t的代数式表示,下同)。反应1的平衡常数Kc=
。(用含m,n,t的代数式表示,下同)。反应1的平衡常数Kc=__ 。
②保持容器体积和投料量不变,分别在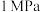 和
和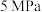 下进行上述反应,测得容器中CO和CH4的含量随温度的变化如下图所示。
下进行上述反应,测得容器中CO和CH4的含量随温度的变化如下图所示。
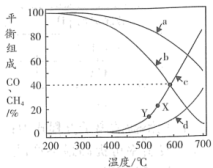
5MPa时,表示CO和CH4平衡组成随温度变化关系的曲线分别是_______ 和_______ 。X点平衡组成含量高于Y点的原因是_______ 。
(4)熔融盐燃料电池具有较高的能量转化效率,某CO熔融盐燃料电池用 、
、 作电解质,则工作时负极上电极反应式为
作电解质,则工作时负极上电极反应式为_______ ;当有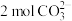 发生定向移动时,电路中转移的电子数目为
发生定向移动时,电路中转移的电子数目为_______ (用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
反应1:
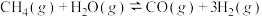
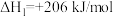
反应2:
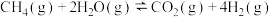

反应3:


(1)

 。
。(2)反应1在
(3)一定温度下,向某容积为1L的恒容容器中充入
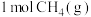 和
和 ,发生上述反应,tmin后反应达到平衡。达到平衡时,容器中CO为mmol,CO2为nmol。
,发生上述反应,tmin后反应达到平衡。达到平衡时,容器中CO为mmol,CO2为nmol。①tmin内CH4的消耗速率为
 。(用含m,n,t的代数式表示,下同)。反应1的平衡常数Kc=
。(用含m,n,t的代数式表示,下同)。反应1的平衡常数Kc=②保持容器体积和投料量不变,分别在
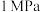 和
和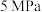 下进行上述反应,测得容器中CO和CH4的含量随温度的变化如下图所示。
下进行上述反应,测得容器中CO和CH4的含量随温度的变化如下图所示。
5MPa时,表示CO和CH4平衡组成随温度变化关系的曲线分别是
(4)熔融盐燃料电池具有较高的能量转化效率,某CO熔融盐燃料电池用
 、
、 作电解质,则工作时负极上电极反应式为
作电解质,则工作时负极上电极反应式为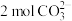 发生定向移动时,电路中转移的电子数目为
发生定向移动时,电路中转移的电子数目为 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】I.为了研究化学反应A+B=C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。
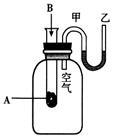
试回答下列问题:
(1)该反应为_______ 反应(填“放热”或“吸热”)。
(2)A和B的总能量比C和D的总能量_______ (填“高”或“低”)。
(3)物质中的化学能通过化学反应转化成_______ 释放出来。
(4)反应物化学键断裂吸收的能量_______ (填“高”或“低”)于生成物化学键形成放出的能量。
(5)写出一个符合题中条件的化学方程式:_____________________ 。
Ⅱ.同素异形体相互转化的反应热相当小,而且转化速率较慢,有时还很不完全,测定反应热很困难。现在可根据盖斯定律提出的“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的”观点来计算反应热。
已知:
P4(白磷,s)+5O2(g)= P4O10(s) ΔH=−2983.2 kJ·mol−1 ①
P(红磷,s)+ O2(g)=
O2(g)= 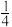 P4O10(s) △H=−738.5 kJ·mol−1 ②
P4O10(s) △H=−738.5 kJ·mol−1 ②
则白磷转化为红磷的热化学方程式为______________ 。相同状况下,能量状态较低的是_______ ;白磷的稳定性比红磷_______ (填“高”或“低”)。

试回答下列问题:
(1)该反应为
(2)A和B的总能量比C和D的总能量
(3)物质中的化学能通过化学反应转化成
(4)反应物化学键断裂吸收的能量
(5)写出一个符合题中条件的化学方程式:
Ⅱ.同素异形体相互转化的反应热相当小,而且转化速率较慢,有时还很不完全,测定反应热很困难。现在可根据盖斯定律提出的“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的”观点来计算反应热。
已知:
P4(白磷,s)+5O2(g)= P4O10(s) ΔH=−2983.2 kJ·mol−1 ①
P(红磷,s)+
 O2(g)=
O2(g)= 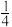 P4O10(s) △H=−738.5 kJ·mol−1 ②
P4O10(s) △H=−738.5 kJ·mol−1 ②则白磷转化为红磷的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】在等压下化学反应所吸收或放出的热量,称为化学反应的焓变。回答下列问题:
(1)25℃、101kPa时,1g氨气完全燃烧放出18.6kJ的热量,则 △H=
△H=_______ kJ∙mol-1。
(2) 反应过程的能量变化如图所示。
反应过程的能量变化如图所示。
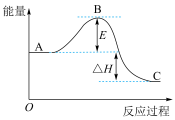
已知:0.5molSO2(g)被氧化为0.5molSO3(g)的△H=-49.5 kJ∙mol-1。则:
①E的大小对该反应的反应热_______ (填“有”或“无”)影响;该反应通常用V2O5作催化剂,加V2O5会使图中B点_______ (填“升高”或“降低”)。
②SO2氧化为SO3的热化学方程式为_______ 。
(3)已知: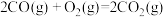 △H=-566 kJ∙mol-1 ①
△H=-566 kJ∙mol-1 ①
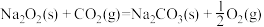 △H=-226 kJ∙mol-1②
△H=-226 kJ∙mol-1②
则CO(g)与Na2O2(s)反应放出509kJ热量时,电子转移数目为_______ 。
(4)常压下,某铝热反应的温度与能量变化如图所示:
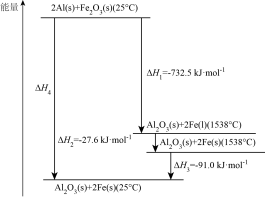
①101.3kPa、1538℃, △H=
△H=_______ kJ∙mol-1。
②101.3kPa、25℃时,该铝热反应的热化学方程式为_______ 。
(1)25℃、101kPa时,1g氨气完全燃烧放出18.6kJ的热量,则
 △H=
△H=(2)
 反应过程的能量变化如图所示。
反应过程的能量变化如图所示。
已知:0.5molSO2(g)被氧化为0.5molSO3(g)的△H=-49.5 kJ∙mol-1。则:
①E的大小对该反应的反应热
②SO2氧化为SO3的热化学方程式为
(3)已知:
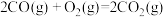 △H=-566 kJ∙mol-1 ①
△H=-566 kJ∙mol-1 ①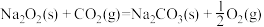 △H=-226 kJ∙mol-1②
△H=-226 kJ∙mol-1②则CO(g)与Na2O2(s)反应放出509kJ热量时,电子转移数目为
(4)常压下,某铝热反应的温度与能量变化如图所示:

①101.3kPa、1538℃,
 △H=
△H=②101.3kPa、25℃时,该铝热反应的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】将二氧化碳资源化是实现“碳中和”目标的重要手段。回答下列问题:
利用 和重整技术可获得合成气(主要成分为CO和
和重整技术可获得合成气(主要成分为CO和 ),反应如下:
),反应如下:
I:

Ⅱ:
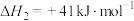
反应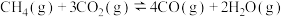 的
的
___________  ,该反应活化能
,该反应活化能 (正)
(正)___________  (逆)(填“>”“<”或“=”)。
(逆)(填“>”“<”或“=”)。
利用
 和重整技术可获得合成气(主要成分为CO和
和重整技术可获得合成气(主要成分为CO和 ),反应如下:
),反应如下:I:


Ⅱ:

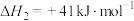
反应
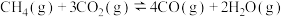 的
的
 ,该反应活化能
,该反应活化能 (正)
(正) (逆)(填“>”“<”或“=”)。
(逆)(填“>”“<”或“=”)。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】下列有关说法正确的是___________ 。
①活化分子间的碰撞一定能发生化学反应
②普通分子有时也能发生有效碰撞
③升高温度会加快反应速率,原因是增加了活化分子的有效碰撞次数
④增大反应物浓度会加快反应速率的原因是单位体积内有效碰撞的次数增多
⑤使用催化剂能提高反应速率,原因是提高了分子的能量,使有效碰撞频率增大
⑥化学反应实质是活化分子有合适取向时的有效碰撞
⑦浓度为1 mol·L-1的盐酸与过量的锌粉反应,若加入适量的CuSO4溶液,能减慢反应速率但又不影响氢气生成量
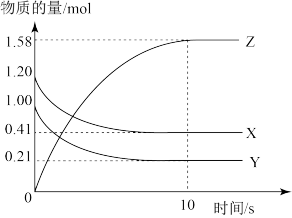
⑧一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图,则反应的化学方程式为X(g)+Y(g) Z(g)
Z(g)
⑨已知4NH3+5O2=4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)(mol·L-1·min-1)表示,则 v(O2)=v(H2O)
v(O2)=v(H2O)
⑩分解水制氢气的工业制法之一是“硫碘循环法”,主要涉及下列反应:①SO2+2H2O+I2=H2SO4+2HI ②2HI H2+I2 ③2H2SO4=2SO2+O2+2H2O,循环过程中产生1 mol O2的同时产生1 mol H2
H2+I2 ③2H2SO4=2SO2+O2+2H2O,循环过程中产生1 mol O2的同时产生1 mol H2
⑪某温度下,在容积一定的密闭容器中进行如下反应:2X(g)+Y(g) Z(g)+W(s) ΔH>0,则升高温度,正反应速率增大,逆反应速率减小
Z(g)+W(s) ΔH>0,则升高温度,正反应速率增大,逆反应速率减小
⑫一定温度下,反应N2(g)+O2(g) 2NO(g)在密闭容器中进行,恒压,充入He不改变化学反应速率
2NO(g)在密闭容器中进行,恒压,充入He不改变化学反应速率
①活化分子间的碰撞一定能发生化学反应
②普通分子有时也能发生有效碰撞
③升高温度会加快反应速率,原因是增加了活化分子的有效碰撞次数
④增大反应物浓度会加快反应速率的原因是单位体积内有效碰撞的次数增多
⑤使用催化剂能提高反应速率,原因是提高了分子的能量,使有效碰撞频率增大
⑥化学反应实质是活化分子有合适取向时的有效碰撞
⑦浓度为1 mol·L-1的盐酸与过量的锌粉反应,若加入适量的CuSO4溶液,能减慢反应速率但又不影响氢气生成量
⑧一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图,则反应的化学方程式为X(g)+Y(g)
 Z(g)
Z(g)
⑨已知4NH3+5O2=4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)(mol·L-1·min-1)表示,则
 v(O2)=v(H2O)
v(O2)=v(H2O)⑩分解水制氢气的工业制法之一是“硫碘循环法”,主要涉及下列反应:①SO2+2H2O+I2=H2SO4+2HI ②2HI
 H2+I2 ③2H2SO4=2SO2+O2+2H2O,循环过程中产生1 mol O2的同时产生1 mol H2
H2+I2 ③2H2SO4=2SO2+O2+2H2O,循环过程中产生1 mol O2的同时产生1 mol H2⑪某温度下,在容积一定的密闭容器中进行如下反应:2X(g)+Y(g)
 Z(g)+W(s) ΔH>0,则升高温度,正反应速率增大,逆反应速率减小
Z(g)+W(s) ΔH>0,则升高温度,正反应速率增大,逆反应速率减小⑫一定温度下,反应N2(g)+O2(g)
 2NO(g)在密闭容器中进行,恒压,充入He不改变化学反应速率
2NO(g)在密闭容器中进行,恒压,充入He不改变化学反应速率
您最近一年使用:0次



