某课外活动小组用如图装置进行实验,试回答下列问题。

(1)若开始时开关K与a连接,则B极的电极反应式为______ 。
(2)若开始时开关K与b连接,则总反应的离子方程式为______ ;关于此实验的说法正确的是______ (填序号)。
A.溶液中 向A极移动
向A极移动
B.从B极处逸出的气体能使湿润的KI淀粉试纸变蓝
C.反应一段时间后通入适量 气体可恢复到电解前电解质的浓度
气体可恢复到电解前电解质的浓度
D.若标准状况下B极产生2.24L气体,则有0.2mol电子发生转移
(3)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
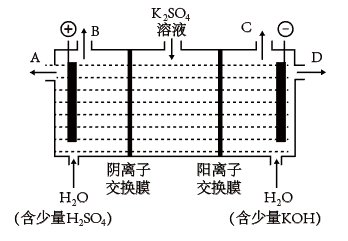
①B出口生成的气体是______ 。
②通电开始后,阴极附近溶液pH会增大,请简述原因______ ;通过阴离子交换膜的离子数______ (填“>”、“<”或“=”)通过阳离子交换膜的离子数。
③若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的电极反应式为______ 。

(1)若开始时开关K与a连接,则B极的电极反应式为
(2)若开始时开关K与b连接,则总反应的离子方程式为
A.溶液中
 向A极移动
向A极移动B.从B极处逸出的气体能使湿润的KI淀粉试纸变蓝
C.反应一段时间后通入适量
 气体可恢复到电解前电解质的浓度
气体可恢复到电解前电解质的浓度D.若标准状况下B极产生2.24L气体,则有0.2mol电子发生转移
(3)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①B出口生成的气体是
②通电开始后,阴极附近溶液pH会增大,请简述原因
③若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的电极反应式为
更新时间:2021-01-31 08:54:39
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务。
(1)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃。
①甲硅烷(SiH4)属于___ (“离子化合物”或“共价化合物”)。
②已知室温下1 g甲硅烷自燃生成SiO2和液态水放出热量44.6 kJ,则甲硅烷自燃的热化学方程式为___________ 。
(2)氢氧燃料电池的总反应为2H2+O2=2H2O,其工作原理如下图所示。

①图中H2从___________ (填“a”或“b”)通入,该电池的正极是___________ (填“M”或“N”)电极,其中在N极发生的电极反应式是___________ 。
②如果在外电路中有1 mol e-发生转移,则消耗标准状况下O2的体积为___________ L。
(1)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃。
①甲硅烷(SiH4)属于
②已知室温下1 g甲硅烷自燃生成SiO2和液态水放出热量44.6 kJ,则甲硅烷自燃的热化学方程式为
(2)氢氧燃料电池的总反应为2H2+O2=2H2O,其工作原理如下图所示。

①图中H2从
②如果在外电路中有1 mol e-发生转移,则消耗标准状况下O2的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)如图利用氧化还原反应设计而成的原电池:

①左边烧杯内发生___________ (填“氧化”或“还原”)反应。
②右边烧杯内的电极反应式是___________ 。
③外电路中电子的流向是___________ 。
④电池总反应离子方程式是___________ 。盐桥M中装有 溶液和琼脂,其作用是
溶液和琼脂,其作用是___________ 。
(2)采用惰性电极,以去离子水和氧气为原料通过电解法制备双氧水的装置如图所示。
①a电极的名称是___________ 极。
②b极的电极反应方程式是___________ 。

(1)如图利用氧化还原反应设计而成的原电池:

①左边烧杯内发生
②右边烧杯内的电极反应式是
③外电路中电子的流向是
④电池总反应离子方程式是
 溶液和琼脂,其作用是
溶液和琼脂,其作用是(2)采用惰性电极,以去离子水和氧气为原料通过电解法制备双氧水的装置如图所示。
①a电极的名称是
②b极的电极反应方程式是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流表的指针发生了偏转。

请回答下列问题:
(1)甲池为_______ (填“原电池”“电解池”或“电镀池”)),通入 电极的电极反应式为
电极的电极反应式为_______ 。
(2)乙池中A(石墨)电极的名称为_______ (填“正极”“负极”“阴极”或“阳极”),乙池中发生的总反应的化学方程式为_______ 。
(3)当乙池中B极质量增加5.40g时,甲池中理论上消耗 的体积为
的体积为_______  (标准状况下)。
(标准状况下)。
(4)若丙中电极不变,将其溶液换成 溶液,电键闭合一段时间后,甲中溶液的
溶液,电键闭合一段时间后,甲中溶液的 将
将_______ (填“增大”“减小”或“不变”,下同);丙中溶液的 将
将_______ 。

请回答下列问题:
(1)甲池为
 电极的电极反应式为
电极的电极反应式为(2)乙池中A(石墨)电极的名称为
(3)当乙池中B极质量增加5.40g时,甲池中理论上消耗
 的体积为
的体积为 (标准状况下)。
(标准状况下)。(4)若丙中电极不变,将其溶液换成
 溶液,电键闭合一段时间后,甲中溶液的
溶液,电键闭合一段时间后,甲中溶液的 将
将 将
将
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在如图所示装置中,石墨电极的电极反应式为___________________ ,如果开始加入的CuSO4足量,则电解一段时间,当电路中转移1.0 mol电子时,要使溶液恢复至原浓度,可向其中加入的物质是____________ (填化学式),其质量为________ g。


您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某课外活动小组用如图所示装置进行实验,试回答下列问题:

(1)若开始时开关K与a连接,则B极的电极反应式为___________ 。
(2)若开始时开关K与b极连接,则B极的电极反应式为___________ ,总反应的离子方程式为___________ 。
(3)若开始时开关K与b连接,下列说法正确的是___________(填字母)。
(4)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用惰性电极及如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阳极反应式为___________ 。
②制得的氢氧化钾溶液从出口___________ (填“A”“B”“C”或“D”)导出。

(1)若开始时开关K与a连接,则B极的电极反应式为
(2)若开始时开关K与b极连接,则B极的电极反应式为
(3)若开始时开关K与b连接,下列说法正确的是___________(填字母)。
| A.溶液中Na+向A极移动 |
| B.从A极处逸出的气体能使湿润的KI-淀粉试纸变蓝 |
| C.反应一段时间后加适量盐酸可恢复到电解前电解质溶液的浓度 |
| D.若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子 |

①该电解槽的阳极反应式为
②制得的氢氧化钾溶液从出口
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图装置甲是某可充电电池的示意图,该电池放电的化学方程式为 ,图中的离子交换膜只允许
,图中的离子交换膜只允许 通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少
通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少 。
。

(1)装置甲的A电极为电池的_______ 极,电解质中 通过离子交换膜向
通过离子交换膜向_____ 迁移(填“左侧”或“右侧”)移动;B电极的电极反应式为________ 。
(2)装置乙中D电极析出的气体体积为______  (标准状况)。若电解质溶液恰好恢复到电解前的浓度和
(标准状况)。若电解质溶液恰好恢复到电解前的浓度和 ,需要向乙装置的电解质溶液中加入
,需要向乙装置的电解质溶液中加入_______ 
_______ 物质(填化学式)。
(3)写出装置丙中总反应的化学反应方程式________ 。
 ,图中的离子交换膜只允许
,图中的离子交换膜只允许 通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少
通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少 。
。
(1)装置甲的A电极为电池的
 通过离子交换膜向
通过离子交换膜向(2)装置乙中D电极析出的气体体积为
 (标准状况)。若电解质溶液恰好恢复到电解前的浓度和
(标准状况)。若电解质溶液恰好恢复到电解前的浓度和 ,需要向乙装置的电解质溶液中加入
,需要向乙装置的电解质溶液中加入
(3)写出装置丙中总反应的化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】如图是一个化学过程的示意图。
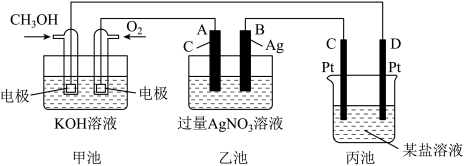
(1)C(Pt)电极的名称是____ 。
(2)写出通入O2的电极上的电极反应式:_______________ 。
(3)写出通入CH3OH的电极上的电极反应式:_________ 。
(4)若丙池是电解饱和食盐水溶液,在____ (填“阳极”或“阴极”)附近滴入酚酞溶液变红。
(5)乙池中反应的化学方程式为____ 。
(6)当乙池中B(Ag)极的质量增加5.40 g时,甲池中理论上消耗O2____ mL(标准状况下);若丙池中饱和食盐水溶液的体积为500 mL,电解后,溶液的pH=_____ 。(25 ℃,假设电解前后溶液的体积无变化)。

(1)C(Pt)电极的名称是
(2)写出通入O2的电极上的电极反应式:
(3)写出通入CH3OH的电极上的电极反应式:
(4)若丙池是电解饱和食盐水溶液,在
(5)乙池中反应的化学方程式为
(6)当乙池中B(Ag)极的质量增加5.40 g时,甲池中理论上消耗O2
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
名校
【推荐2】
右图是一个用铂丝作电极,电解稀的MgSO4溶液的装置,电解液中加有中性红指示剂,此时溶液呈红色。(指示剂的pH变色范围:6.8~8.0,酸色—红色,碱色—黄色)
回答下列问题:
(1)下列关于电解过程中电极附近溶液颜色变化的叙述正确的是________ (填编号);
①A管溶液由红变黄;②B管溶液由红变黄;
③A管溶液不变色;④B管溶液不变色;
(2)写出A管中发生反应的反应式:_________________________________ ;
(3)写出B管中发生反应的反应式:_________________________________ ;
(4)检验a管中气体的方法是_______________________________________ ;
(5)检验b管中气体的方法是____________________________________________ ;
(6)电解一段时间后,切断电源,将电解液倒入烧杯内观察到的现象是_____________________ 。

右图是一个用铂丝作电极,电解稀的MgSO4溶液的装置,电解液中加有中性红指示剂,此时溶液呈红色。(指示剂的pH变色范围:6.8~8.0,酸色—红色,碱色—黄色)
回答下列问题:
(1)下列关于电解过程中电极附近溶液颜色变化的叙述正确的是
①A管溶液由红变黄;②B管溶液由红变黄;
③A管溶液不变色;④B管溶液不变色;
(2)写出A管中发生反应的反应式:
(3)写出B管中发生反应的反应式:
(4)检验a管中气体的方法是
(5)检验b管中气体的方法是
(6)电解一段时间后,切断电源,将电解液倒入烧杯内观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流计的指针发生了偏转。

请回答下列问题:
(1)甲池为________  填“原电池”“电解池”或“电镀池”
填“原电池”“电解池”或“电镀池” ,通入
,通入 电极的电极反应式为
电极的电极反应式为_______________________________ 。
(2)乙池中 石墨
石墨 电极的名称为
电极的名称为________  填“正极”“负极”“阴极”或“阳极”
填“正极”“负极”“阴极”或“阳极” ,总反应式为
,总反应式为__________________________________ 。
(3)当乙池中B极质量增加 时,甲池中理论上消耗
时,甲池中理论上消耗 的体积为
的体积为________  标准状况下
标准状况下
(4)电键闭合一段时间后,甲中溶液的pH将________  填“增大”“减小”或“不变”
填“增大”“减小”或“不变” ;若丙中电极不变,将其溶液换成NaCl溶液,丙中溶液的pH将
;若丙中电极不变,将其溶液换成NaCl溶液,丙中溶液的pH将________  填“增大”“减小”或“不变”
填“增大”“减小”或“不变” 。
。

请回答下列问题:
(1)甲池为
 填“原电池”“电解池”或“电镀池”
填“原电池”“电解池”或“电镀池” ,通入
,通入 电极的电极反应式为
电极的电极反应式为(2)乙池中
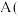 石墨
石墨 电极的名称为
电极的名称为 填“正极”“负极”“阴极”或“阳极”
填“正极”“负极”“阴极”或“阳极” ,总反应式为
,总反应式为(3)当乙池中B极质量增加
 时,甲池中理论上消耗
时,甲池中理论上消耗 的体积为
的体积为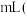 标准状况下
标准状况下
(4)电键闭合一段时间后,甲中溶液的pH将
 填“增大”“减小”或“不变”
填“增大”“减小”或“不变” ;若丙中电极不变,将其溶液换成NaCl溶液,丙中溶液的pH将
;若丙中电极不变,将其溶液换成NaCl溶液,丙中溶液的pH将 填“增大”“减小”或“不变”
填“增大”“减小”或“不变” 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】我国在应对气候变化工作中取得显著成效,承诺2030年实现“碳达峰”,2060年实现“碳中和”。因此将 转化为高附加值产品成为重要的研究课题。
转化为高附加值产品成为重要的研究课题。
Ⅰ.催化还原 制备甲醇
制备甲醇
该过程反应如下:
反应i:
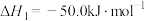
反应ii:

(1)反应的 的
的
_________  。
。
(2)恒温下, 与
与 在恒容密闭容器发生反应i、ii,下列能表明上述反应已达到平衡状态的有_________(填标号)。
在恒容密闭容器发生反应i、ii,下列能表明上述反应已达到平衡状态的有_________(填标号)。
(3)不同条件下,按照 投料,
投料, 的平衡转化率随温度和压强变化如图所示。
的平衡转化率随温度和压强变化如图所示。
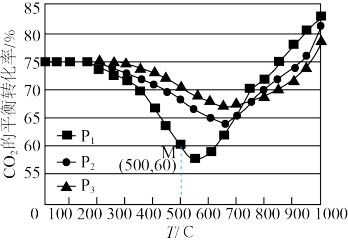
①压强 、
、 、
、 由大到小的顺序是
由大到小的顺序是_________ 。压强为 时,温度高于570℃之后,随着温度升高
时,温度高于570℃之后,随着温度升高 平衡转化率增大的原因是
平衡转化率增大的原因是__________________ 。
②请提出一条可提高 选择性(选择性:生成
选择性(选择性:生成 与消耗
与消耗 的物质的量比)的措施
的物质的量比)的措施_________ 。
③图中 点
点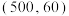 ,此时压强
,此时压强 为
为 ,
, 的选择性为
的选择性为 。则该温度时反应i的平衡常数
。则该温度时反应i的平衡常数
_________ ( )(分压=总压×物质的量分数)。
)(分压=总压×物质的量分数)。
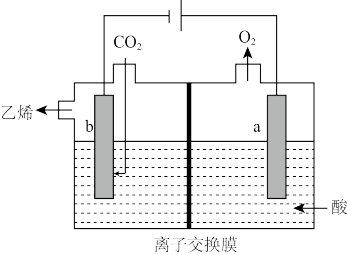
Ⅱ.电化学法还原 制乙烯
制乙烯
(4)其原理如图所示,阴极电极反应式为__________________ 。
 转化为高附加值产品成为重要的研究课题。
转化为高附加值产品成为重要的研究课题。Ⅰ.催化还原
 制备甲醇
制备甲醇该过程反应如下:
反应i:

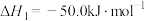
反应ii:


(1)反应的
 的
的
 。
。(2)恒温下,
 与
与 在恒容密闭容器发生反应i、ii,下列能表明上述反应已达到平衡状态的有_________(填标号)。
在恒容密闭容器发生反应i、ii,下列能表明上述反应已达到平衡状态的有_________(填标号)。A.每断裂 键,同时生成 键,同时生成 键 键 |
B.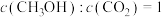 |
| C.混合气体的平均相对分子质量不变 |
| D.混合气体的压强不变 |
 投料,
投料, 的平衡转化率随温度和压强变化如图所示。
的平衡转化率随温度和压强变化如图所示。
①压强
 、
、 、
、 由大到小的顺序是
由大到小的顺序是 时,温度高于570℃之后,随着温度升高
时,温度高于570℃之后,随着温度升高 平衡转化率增大的原因是
平衡转化率增大的原因是②请提出一条可提高
 选择性(选择性:生成
选择性(选择性:生成 与消耗
与消耗 的物质的量比)的措施
的物质的量比)的措施③图中
 点
点 ,此时压强
,此时压强 为
为 ,
, 的选择性为
的选择性为 。则该温度时反应i的平衡常数
。则该温度时反应i的平衡常数
 )(分压=总压×物质的量分数)。
)(分压=总压×物质的量分数)。Ⅱ.电化学法还原
 制乙烯
制乙烯(4)其原理如图所示,阴极电极反应式为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某同学用如图所示装置探究在铝块表面生成氧化膜的实验, 为两种常见金属,它们的硫酸盐可溶于水。当
为两种常见金属,它们的硫酸盐可溶于水。当 闭合时,回答下列问题:
闭合时,回答下列问题:
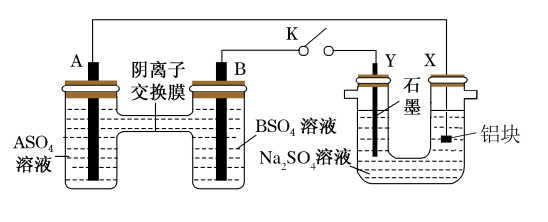
(1)①装置Ⅰ中A电极为_______ (填“正”或“负”)极,发生_______ (填“氧化”或“还原”)反应。
②在阴离子交换膜处_______ (填离子符号)从_______ (填“由右向左”或“由左向右”)移动。
(2)装置Ⅱ中, 电极上的电极反应式为
电极上的电极反应式为_______ 。
(3)当 三个电极的质量变化之比为
三个电极的质量变化之比为 时(忽略
时(忽略 电极上物质的溶解),金属
电极上物质的溶解),金属 的摩尔质量是
的摩尔质量是_______ ,金属B的元素符号是_______ 。
 为两种常见金属,它们的硫酸盐可溶于水。当
为两种常见金属,它们的硫酸盐可溶于水。当 闭合时,回答下列问题:
闭合时,回答下列问题:
(1)①装置Ⅰ中A电极为
②在阴离子交换膜处
(2)装置Ⅱ中,
 电极上的电极反应式为
电极上的电极反应式为(3)当
 三个电极的质量变化之比为
三个电极的质量变化之比为 时(忽略
时(忽略 电极上物质的溶解),金属
电极上物质的溶解),金属 的摩尔质量是
的摩尔质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如图所示,甲、乙两池电极材料都是铁棒与碳棒,请回答下列问题。
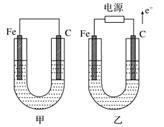
(1)若两池中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲池中的___________ 棒,乙池中的________ 棒。
②乙池中阳极的电极反应式是:_________________ 。
(2)若两池中均为饱和NaCl溶液:
①写出乙池中总反应的离子方程式:____________________ 。
②甲池中碳极的电极反应式是:______________ ,乙池中碳极的电极反应属于_______ (填“氧化反应”或“还原反应”)。
③将湿润的淀粉KI试纸放在乙池中碳极附近,发现试纸变蓝,过一段时间后又发现蓝色褪去,这是因为过量的Cl2又将生成的I2氧化。若反应的Cl2和I2物质的量之比为5∶1,且生成两种酸,该反应的化学方程式为:__________________ 。

(1)若两池中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲池中的
②乙池中阳极的电极反应式是:
(2)若两池中均为饱和NaCl溶液:
①写出乙池中总反应的离子方程式:
②甲池中碳极的电极反应式是:
③将湿润的淀粉KI试纸放在乙池中碳极附近,发现试纸变蓝,过一段时间后又发现蓝色褪去,这是因为过量的Cl2又将生成的I2氧化。若反应的Cl2和I2物质的量之比为5∶1,且生成两种酸,该反应的化学方程式为:
您最近一年使用:0次



